X
Код презентации скопируйте его
Соли аммония
Скачать эту презентациюПрезентация на тему Соли аммония
Скачать эту презентациюCлайд 1
 соли аммония Химические свойства, применение, получение Мамедова Т.И., учитель химии МОУ СОШ №1
соли аммония Химические свойства, применение, получение Мамедова Т.И., учитель химии МОУ СОШ №1
Cлайд 3
 Ион аммония образован только неметаллами. Так же, как и ионы металлов, он образует свои соли. Все соли аммония растворимы в воде. Качественная реакция на ион аммония- действие щелочи при нагревании. В состав пекарского порошка входит гидрокарбонат аммония, поэтому его используют в хлебопечении. Нашатырь используют при паянии. Агроному-почвоведу, а также любому дачнику необходимы знания по химии. Без азота нет белка, без белка нет жизни.
Ион аммония образован только неметаллами. Так же, как и ионы металлов, он образует свои соли. Все соли аммония растворимы в воде. Качественная реакция на ион аммония- действие щелочи при нагревании. В состав пекарского порошка входит гидрокарбонат аммония, поэтому его используют в хлебопечении. Нашатырь используют при паянии. Агроному-почвоведу, а также любому дачнику необходимы знания по химии. Без азота нет белка, без белка нет жизни.
Cлайд 4
 Цели урока сформировать знания о характерных свойствах солей аммония, ознакомить с представителями этих солей и их применением, развивать умения выделять главное, классифицировать, представлять результаты работы.
Цели урока сформировать знания о характерных свойствах солей аммония, ознакомить с представителями этих солей и их применением, развивать умения выделять главное, классифицировать, представлять результаты работы.
Cлайд 5
 Соли аммо ния — соли, содержащие одновалентный ион аммония NH4+; по строению, цвету и другим свойствам они похожи на соответствующие соли калия. Все соли аммония растворимы в воде, полностью диссоциируют в водном растворе.
Соли аммо ния — соли, содержащие одновалентный ион аммония NH4+; по строению, цвету и другим свойствам они похожи на соответствующие соли калия. Все соли аммония растворимы в воде, полностью диссоциируют в водном растворе.
Cлайд 6
 Химические свойства 1. Сильные электролиты (диссоциируют в водных растворах): NH4Cl ↔ NH4 ++ Cl- 2. С кислотами (реакция обмена): (NH4) 2CO3 + 2НCl → 2NH 4Cl + Н2O + CO2 ↑ 2NH4+ + CO32- + 2H+ + 2Cl- → 2NH4+ + 2Cl- + Н2O + CO2 ↑ CO32- + 2H+ → Н2O + CO2 ↑
Химические свойства 1. Сильные электролиты (диссоциируют в водных растворах): NH4Cl ↔ NH4 ++ Cl- 2. С кислотами (реакция обмена): (NH4) 2CO3 + 2НCl → 2NH 4Cl + Н2O + CO2 ↑ 2NH4+ + CO32- + 2H+ + 2Cl- → 2NH4+ + 2Cl- + Н2O + CO2 ↑ CO32- + 2H+ → Н2O + CO2 ↑
Cлайд 7
 Химические свойства 3. C солями (реакция обмена): (NH4)2SO4 + Ba(NO3)2 → BaSO4 ↓ + 2NH4NO3 2NH4+ + SO42- + Ba2+ + 2NO3- → BaSO4 ↓ + 2NH4+ + 2NO3- Ba2+ + SO42- → BaSO4 ↓ 4. При нагревании со щелочами выделяется аммиак (качественная реакция на ион аммония): NH4Cl + NaOH → NaCl + NH3 ↑ + Н2O
Химические свойства 3. C солями (реакция обмена): (NH4)2SO4 + Ba(NO3)2 → BaSO4 ↓ + 2NH4NO3 2NH4+ + SO42- + Ba2+ + 2NO3- → BaSO4 ↓ + 2NH4+ + 2NO3- Ba2+ + SO42- → BaSO4 ↓ 4. При нагревании со щелочами выделяется аммиак (качественная реакция на ион аммония): NH4Cl + NaOH → NaCl + NH3 ↑ + Н2O
Cлайд 8
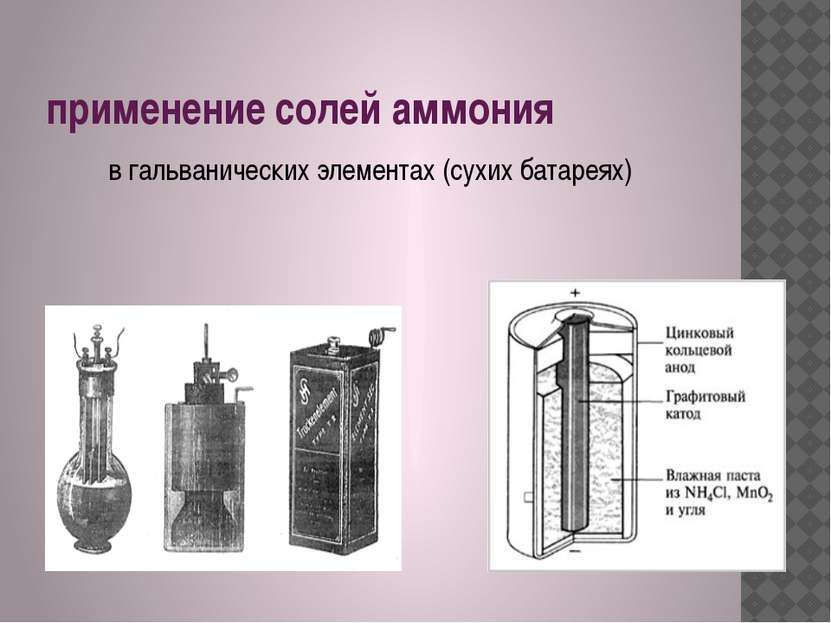
 Применение солей аммония в пиротехнике; в хлебопечении и кондитерской промышленности; в сельском хозяйстве- удобрения; при паянии металлов (нашатырь- хлорид аммония); электролит в сухих элементах (хлорид аммония).
Применение солей аммония в пиротехнике; в хлебопечении и кондитерской промышленности; в сельском хозяйстве- удобрения; при паянии металлов (нашатырь- хлорид аммония); электролит в сухих элементах (хлорид аммония).
Cлайд 9
 применение солей аммония Нитрат аммония NH4NО3 в смеси с порошками алюминия и угля используют в качестве взрывчатого вещества - аммонала , который широко применяют при разработке горных пород.
применение солей аммония Нитрат аммония NH4NО3 в смеси с порошками алюминия и угля используют в качестве взрывчатого вещества - аммонала , который широко применяют при разработке горных пород.
Cлайд 10
 применение солей аммония Гидрокарбонат аммония NH4HCO3 и карбонат аммония (NH4)2CO3 применяют в кондитерском деле, так как они легко разлагаются при нагревании и образуют газы, разрыхляющие тесто и делающие его пышным, например: NH4HCO3 = NH3↑ + Н2O↑ + CO2↑
применение солей аммония Гидрокарбонат аммония NH4HCO3 и карбонат аммония (NH4)2CO3 применяют в кондитерском деле, так как они легко разлагаются при нагревании и образуют газы, разрыхляющие тесто и делающие его пышным, например: NH4HCO3 = NH3↑ + Н2O↑ + CO2↑
Cлайд 12
 применение солей аммония Хлорид аммония NH4Cl используют при паянии, так как он очищает поверхность металла от оксидной плёнки и к ней хорошо пристаёт припой.
применение солей аммония Хлорид аммония NH4Cl используют при паянии, так как он очищает поверхность металла от оксидной плёнки и к ней хорошо пристаёт припой.
Cлайд 15
 получение солей аммония Аммиак (или гидроксид аммония) + кислота. NH3 + HNO3 = NH4NO3 2NH4OH + H2SO4 =(NH4) 2SO4+ 2Н2O
получение солей аммония Аммиак (или гидроксид аммония) + кислота. NH3 + HNO3 = NH4NO3 2NH4OH + H2SO4 =(NH4) 2SO4+ 2Н2O
Cлайд 16
 Задания на развитие творческого мышления. Предложите способ очистки поваренной соли от содержащейся в ней примеси хлорида аммония. Объясните, можно ли смешивать аммиачную селитру (нитрат аммония) с известью?
Задания на развитие творческого мышления. Предложите способ очистки поваренной соли от содержащейся в ней примеси хлорида аммония. Объясните, можно ли смешивать аммиачную селитру (нитрат аммония) с известью?
Cлайд 17
 Заключение Роль азотистых соединений в жизни человека и общества очень велика, а применении разнообразно. Азот – основа жизни на Земле. На Земле постоянно происходят процессы превращения веществ живой и неживой природы. В результате этих превращений неорганические вещества неживой природы – соли аммония могут превращаться в сложные органические вещества – белки. А белки – это основа всего живого В белках содержится 18 % азота. Без азота нет белка, без белка нет жизни!
Заключение Роль азотистых соединений в жизни человека и общества очень велика, а применении разнообразно. Азот – основа жизни на Земле. На Земле постоянно происходят процессы превращения веществ живой и неживой природы. В результате этих превращений неорганические вещества неживой природы – соли аммония могут превращаться в сложные органические вещества – белки. А белки – это основа всего живого В белках содержится 18 % азота. Без азота нет белка, без белка нет жизни!