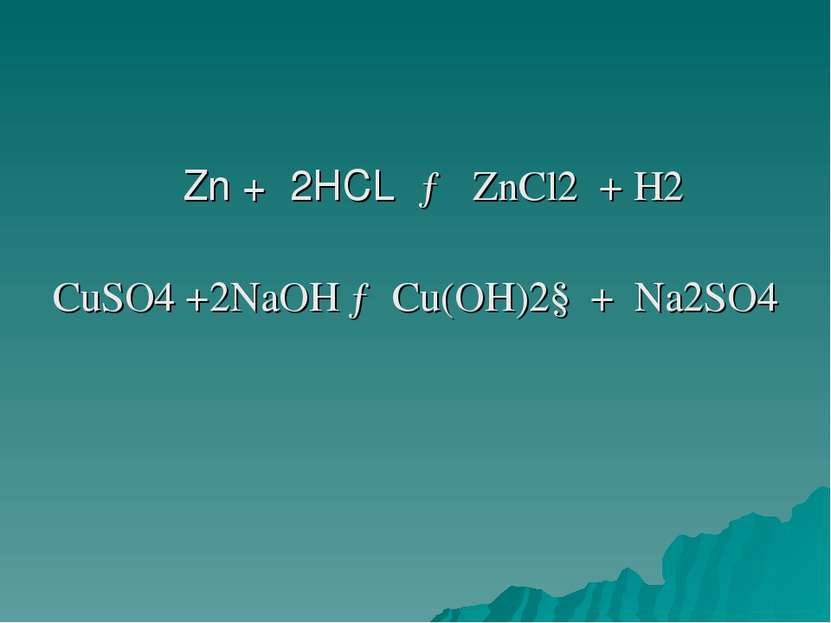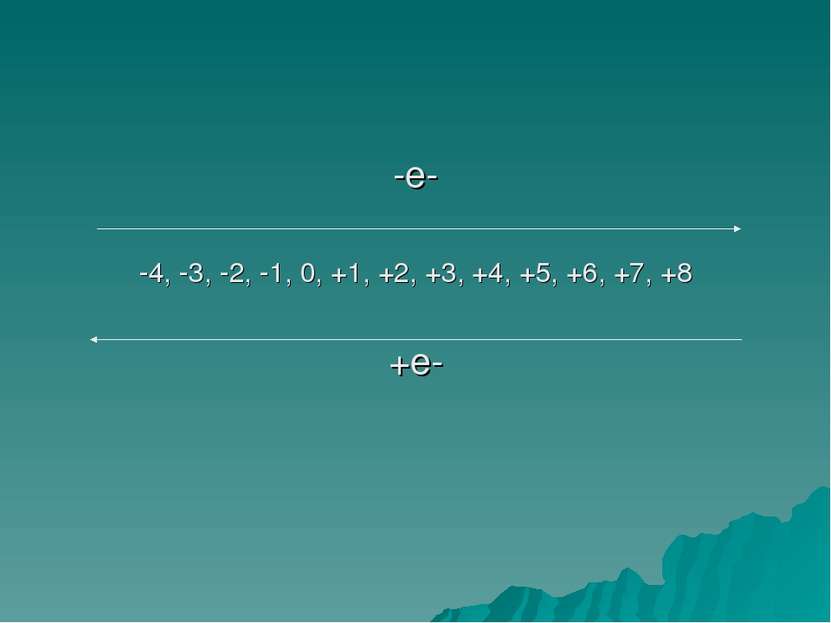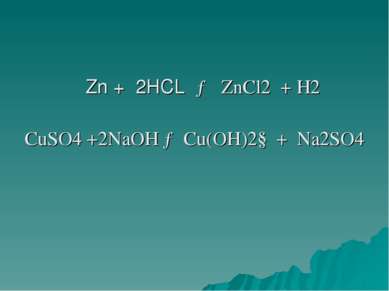X
Код презентации скопируйте его
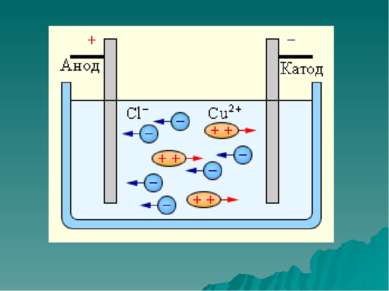
Окислительно-восстановительные реакции
Скачать эту презентациюПрезентация на тему Окислительно-восстановительные реакции
Скачать эту презентациюCлайд 2
 Цели: Обучающие Повторить и расширить знания учащихся о ОВР. Важнейшие окислители и восстановители. Ознакомить с методом составления уравнений окислительно-восстановительных реакций. (Метод электронного баланс.) Влияние среды на протекание окислительно-восстановительных процессов. Воспитательные Создать положительный настрой к обучению и готовность к активной мыслительной деятельности, используя видеоматериалы и метод демонстрационного эксперимента; воспитывать культуру речи и труда. Развивающие Развивать у учащихся познавательный интерес к изучению химии, умение анализировать, сравнивать, делать выводы, самостоятельность учащихся. (ОК 3.: Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность)
Цели: Обучающие Повторить и расширить знания учащихся о ОВР. Важнейшие окислители и восстановители. Ознакомить с методом составления уравнений окислительно-восстановительных реакций. (Метод электронного баланс.) Влияние среды на протекание окислительно-восстановительных процессов. Воспитательные Создать положительный настрой к обучению и готовность к активной мыслительной деятельности, используя видеоматериалы и метод демонстрационного эксперимента; воспитывать культуру речи и труда. Развивающие Развивать у учащихся познавательный интерес к изучению химии, умение анализировать, сравнивать, делать выводы, самостоятельность учащихся. (ОК 3.: Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность)
Cлайд 3
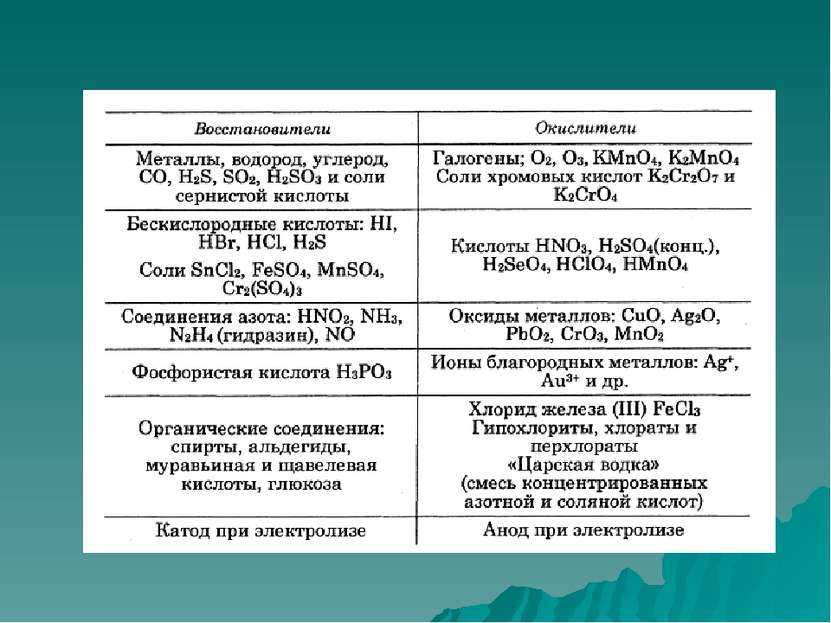
 План лекции Понятие о ОВР Важнейшие окислители и восстановители Классификация ОВР Метод электронного баланса Влияние среды на протекание ОВР
План лекции Понятие о ОВР Важнейшие окислители и восстановители Классификация ОВР Метод электронного баланса Влияние среды на протекание ОВР
Cлайд 5
 Окислительно восстановительные реакции (ОВР) — это реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ.
Окислительно восстановительные реакции (ОВР) — это реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ.
Cлайд 14
 Степень окисления. Элементы с постоянной степенью окисления Элементы с переменной степенью окисления.
Степень окисления. Элементы с постоянной степенью окисления Элементы с переменной степенью окисления.
Cлайд 15
 Определите степень окисления для магния и алюминия. Какие степени окисления возможны для серы? Какие степени окисления возможны для хрома?
Определите степень окисления для магния и алюминия. Какие степени окисления возможны для серы? Какие степени окисления возможны для хрома?
Cлайд 18
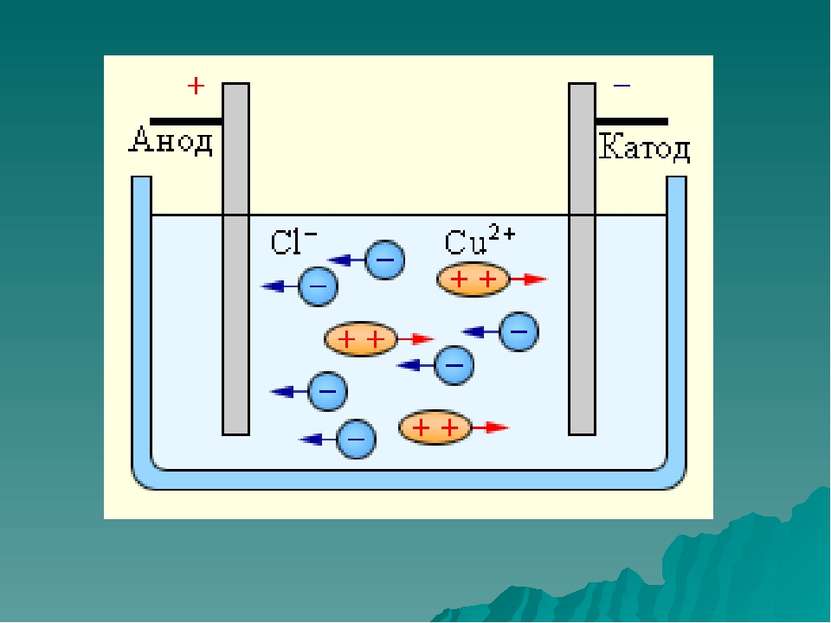
 Восстановитель -элемент, который отдает электроны. Восстановитель окисляется, повышая свою степень окисления. Окисление - процесс отдачи электронов
Восстановитель -элемент, который отдает электроны. Восстановитель окисляется, повышая свою степень окисления. Окисление - процесс отдачи электронов
Cлайд 19
 Окислитель элемент, который присоединяет электроны. Окислитель восстанавливается, понижая свою степень окисления. Восстановление – процесс принятия электронов
Окислитель элемент, который присоединяет электроны. Окислитель восстанавливается, понижая свою степень окисления. Восстановление – процесс принятия электронов
Cлайд 21
 Влияние степени окисления на окислительные и восстановительные свойства элементов. В высшей положительной степени окисления элемент проявляет только окислительные свойства В промежуточной степени окисления и окислительные и восстановительные свойства. В высшей отрицательной степени окисления только восстановительные степени окисления.
Влияние степени окисления на окислительные и восстановительные свойства элементов. В высшей положительной степени окисления элемент проявляет только окислительные свойства В промежуточной степени окисления и окислительные и восстановительные свойства. В высшей отрицательной степени окисления только восстановительные степени окисления.