X
Код презентации скопируйте его
ОСНОВАНИЯ
Скачать эту презентациюПрезентация на тему ОСНОВАНИЯ
Скачать эту презентациюCлайд 1
 ОСНОВАНИЯ Цели: 1) Сформировать понятие об основаниях как классе электролитов; 2) Рассмотреть их классификацию по разным признакам; 3) Представить химические свойства оснований в свете теории электролитической диссоциации.
ОСНОВАНИЯ Цели: 1) Сформировать понятие об основаниях как классе электролитов; 2) Рассмотреть их классификацию по разным признакам; 3) Представить химические свойства оснований в свете теории электролитической диссоциации.
Cлайд 3
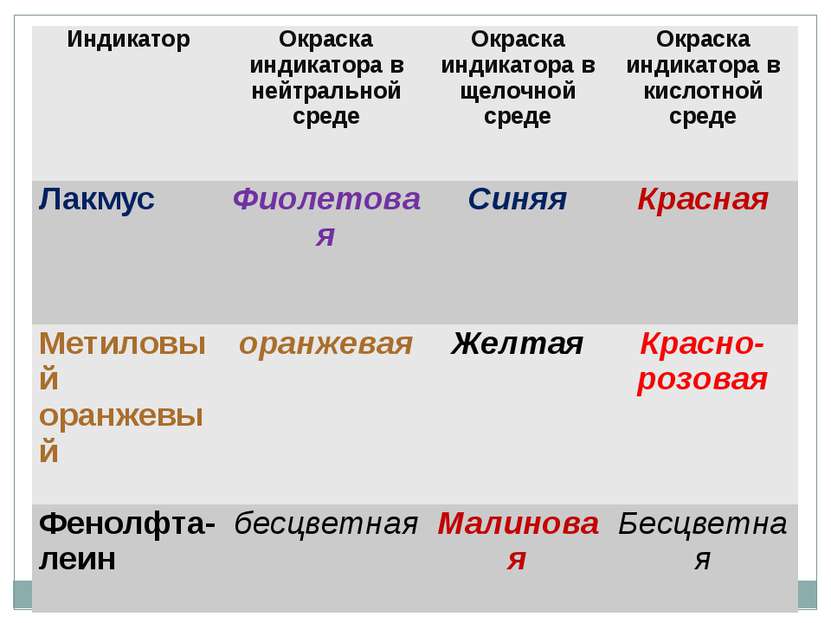
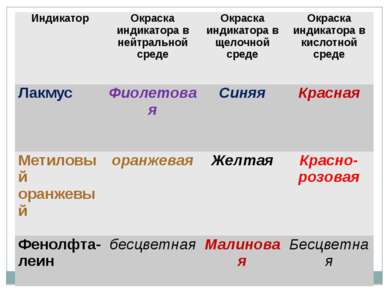 Индикатор Окраска индикатора в нейтральной среде Окраска индикатора в щелочной среде Окраска индикатора в кислотной среде Лакмус Фиолетовая Синяя Красная Метиловый оранжевый оранжевая Желтая Красно-розовая Фенолфта-леин бесцветная Малиновая Бесцветная
Индикатор Окраска индикатора в нейтральной среде Окраска индикатора в щелочной среде Окраска индикатора в кислотной среде Лакмус Фиолетовая Синяя Красная Метиловый оранжевый оранжевая Желтая Красно-розовая Фенолфта-леин бесцветная Малиновая Бесцветная
Cлайд 4
 Основание – это сложное вещество, состоящее из атомов металлов и одной или нескольких гидроксогрупп (-ОН). М(ОН)n Общая формула оснований
Основание – это сложное вещество, состоящее из атомов металлов и одной или нескольких гидроксогрупп (-ОН). М(ОН)n Общая формула оснований
Cлайд 5
 Физические свойства оснований: Щелочи – окрашены в белый цвет Cu(OH)2 – голубой Fe(OH)3 – красно-бурый Cr(OH)3 – серо-зеленый
Физические свойства оснований: Щелочи – окрашены в белый цвет Cu(OH)2 – голубой Fe(OH)3 – красно-бурый Cr(OH)3 – серо-зеленый
Cлайд 6
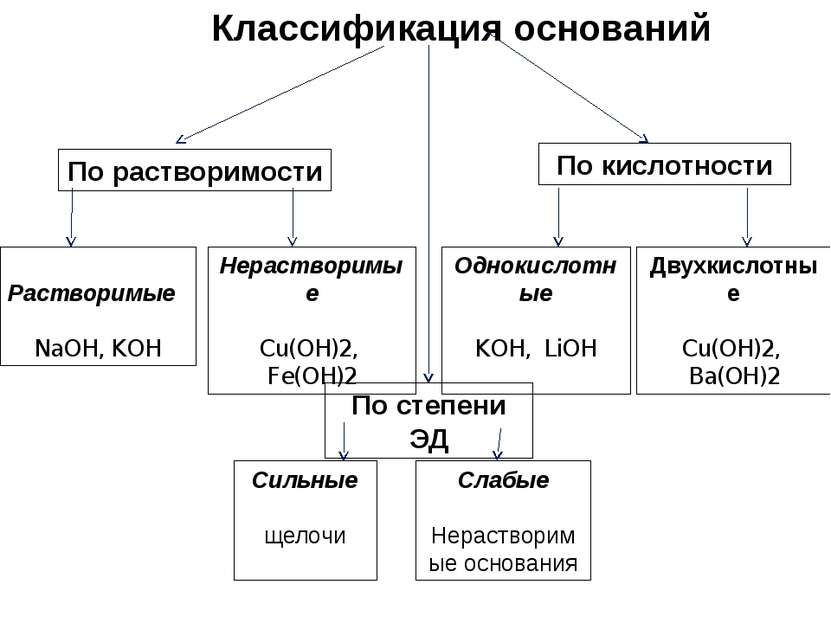
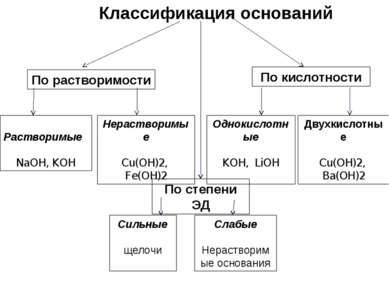 Классификация оснований По растворимости По кислотности По степени ЭД Растворимые NaOH, KOH Нерастворимые Cu(OH)2, Fe(OH)2 Однокислотные KOH, LiOH Двухкислотные Cu(OH)2, Ba(OH)2 Сильные щелочи Слабые Нерастворимые основания
Классификация оснований По растворимости По кислотности По степени ЭД Растворимые NaOH, KOH Нерастворимые Cu(OH)2, Fe(OH)2 Однокислотные KOH, LiOH Двухкислотные Cu(OH)2, Ba(OH)2 Сильные щелочи Слабые Нерастворимые основания