X
Код презентации скопируйте его
Обратимость химических реакций
Скачать эту презентациюПрезентация на тему Обратимость химических реакций
Скачать эту презентациюCлайд 2
 Углубить и обобщить знания о состоянии химического равновесия, условиях его смещения. Дать понятие о константе равновесия. Цель:
Углубить и обобщить знания о состоянии химического равновесия, условиях его смещения. Дать понятие о константе равновесия. Цель:
Cлайд 3
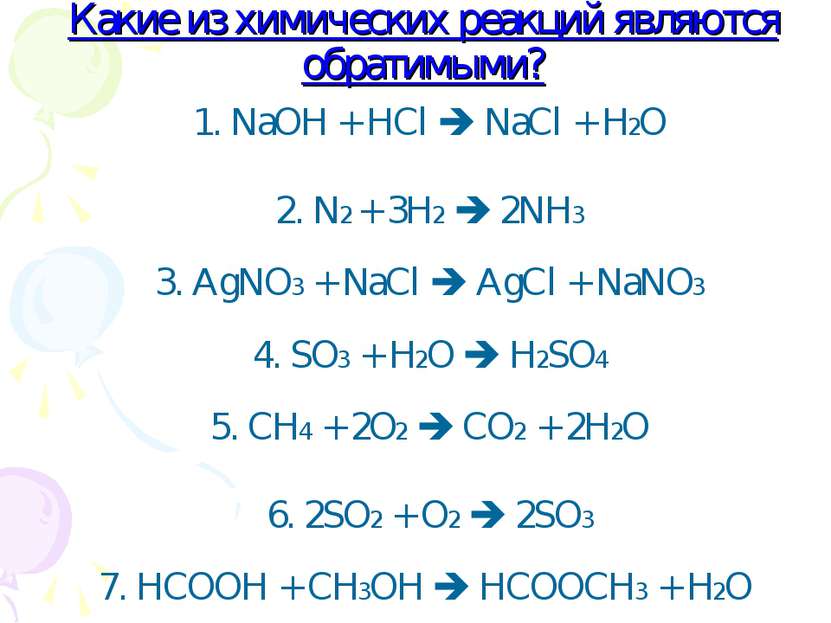
 Какие из химических реакций являются обратимыми? 1. NaOH + HCl NaCl + H2O 2. N2 + 3H2 2NH3 3. AgNO3 + NaCl AgCl + NaNO3 4. SO3 + H2O H2SO4 5. CH4 + 2O2 CO2 + 2H2O 6. 2SO2 + O2 2SO3 7. HCOOH + CH3OH HCOOCH3 + H2O
Какие из химических реакций являются обратимыми? 1. NaOH + HCl NaCl + H2O 2. N2 + 3H2 2NH3 3. AgNO3 + NaCl AgCl + NaNO3 4. SO3 + H2O H2SO4 5. CH4 + 2O2 CO2 + 2H2O 6. 2SO2 + O2 2SO3 7. HCOOH + CH3OH HCOOCH3 + H2O
Cлайд 7
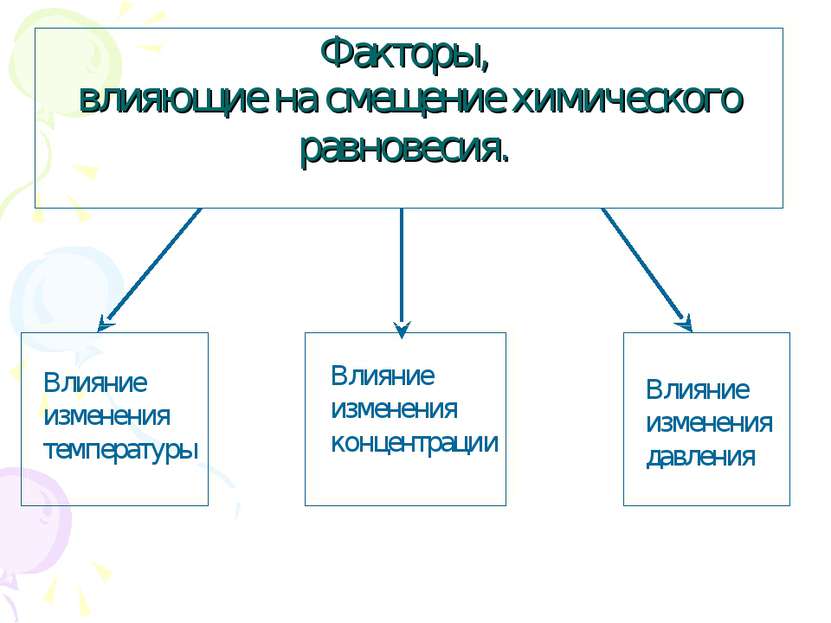
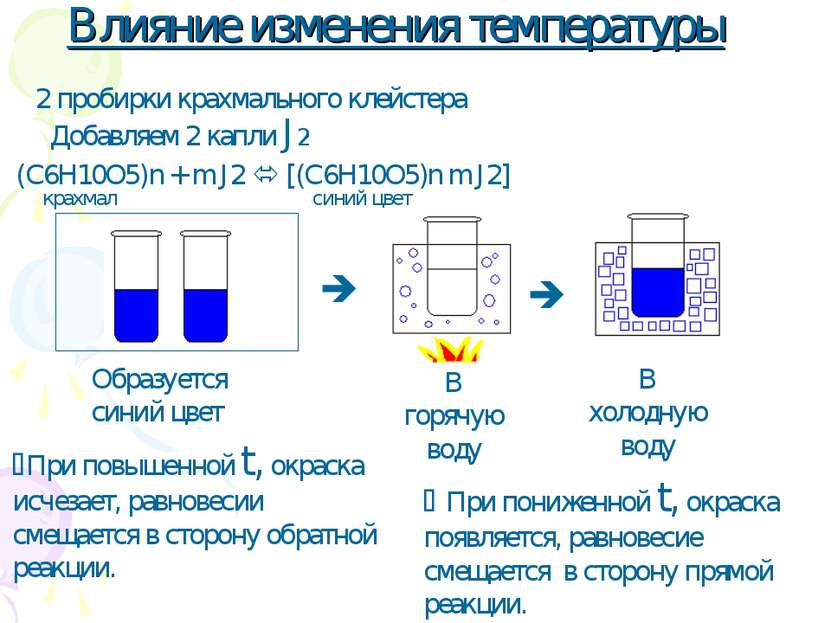
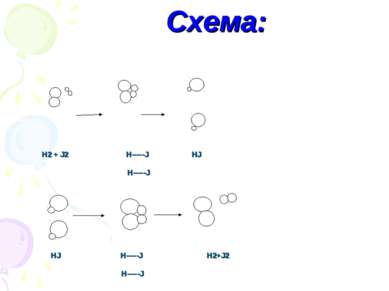
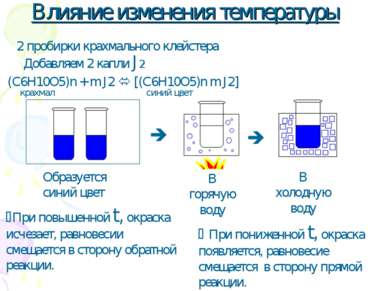 Влияние изменения температуры 2 пробирки крахмального клейстера Добавляем 2 капли J2 При повышенной t, окраска исчезает, равновесии смещается в сторону обратной реакции. При пониженной t, окраска появляется, равновесие смещается в сторону прямой реакции.
Влияние изменения температуры 2 пробирки крахмального клейстера Добавляем 2 капли J2 При повышенной t, окраска исчезает, равновесии смещается в сторону обратной реакции. При пониженной t, окраска появляется, равновесие смещается в сторону прямой реакции.
Cлайд 8
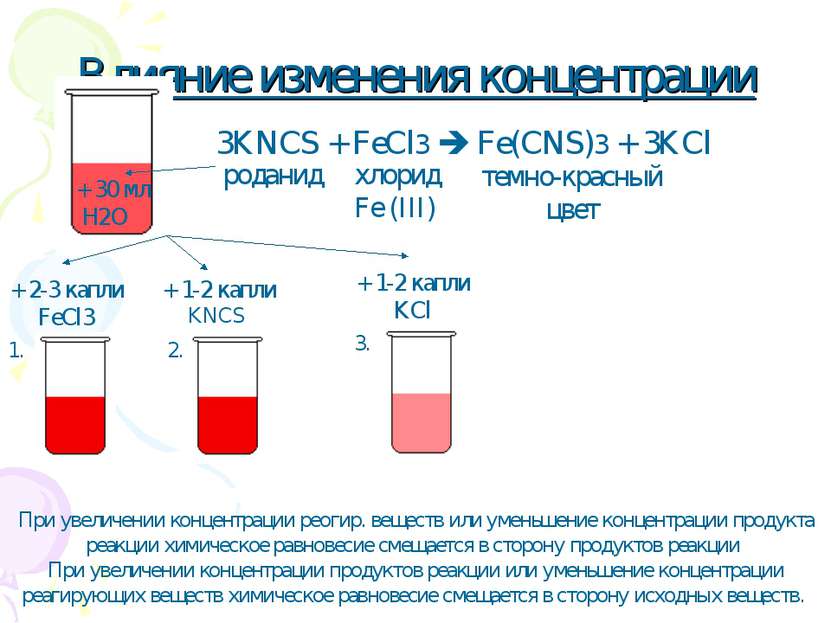
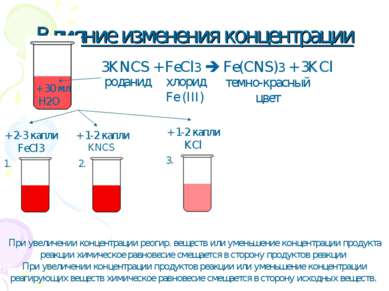 Влияние изменения концентрации + 2-3 капли FeCl3 + 1-2 капли KNCS + 1-2 капли KCl При увеличении концентрации реогир. веществ или уменьшение концентрации продукта реакции химическое равновесие смещается в сторону продуктов реакции При увеличении концентрации продуктов реакции или уменьшение концентрации реагирующих веществ химическое равновесие смещается в сторону исходных веществ.
Влияние изменения концентрации + 2-3 капли FeCl3 + 1-2 капли KNCS + 1-2 капли KCl При увеличении концентрации реогир. веществ или уменьшение концентрации продукта реакции химическое равновесие смещается в сторону продуктов реакции При увеличении концентрации продуктов реакции или уменьшение концентрации реагирующих веществ химическое равновесие смещается в сторону исходных веществ.
Cлайд 9
 Влияние изменения давления 2NO2 N2O4 + Q При расширении цвет газа стал темно-бурым, а равновесие сместилось в сторону обратной реакции. При сжатии цвет газа стал бледно-желтым, а равновесие сместилось в сторону прямой реакции. При увеличении давления равновесие смещается в сторону меньшего объема
Влияние изменения давления 2NO2 N2O4 + Q При расширении цвет газа стал темно-бурым, а равновесие сместилось в сторону обратной реакции. При сжатии цвет газа стал бледно-желтым, а равновесие сместилось в сторону прямой реакции. При увеличении давления равновесие смещается в сторону меньшего объема
Cлайд 13
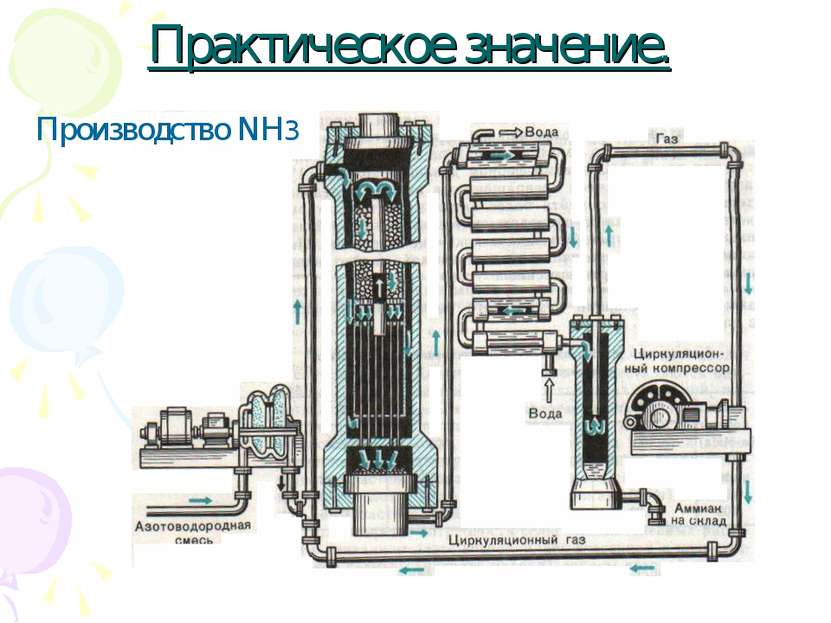
 1.Смещение химического равновесия обеспечивает высокий выход желаемого продукта. 2. Открывает путь к управлению химическими реакциями.
1.Смещение химического равновесия обеспечивает высокий выход желаемого продукта. 2. Открывает путь к управлению химическими реакциями.
Cлайд 14
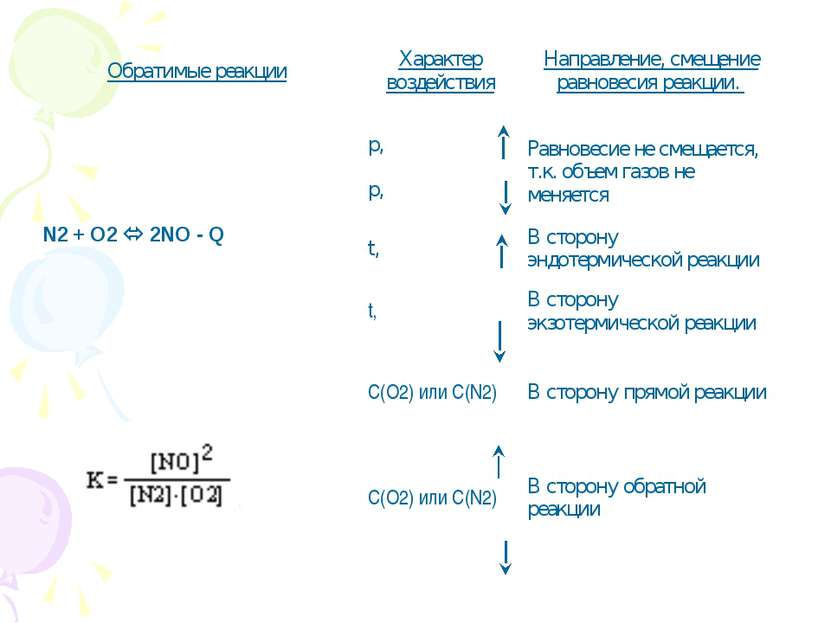
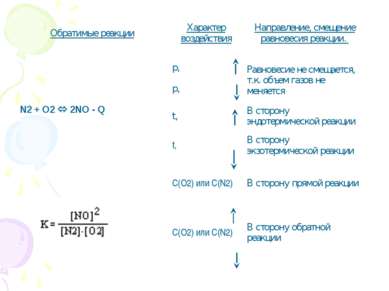 Обратимые реакции Характер воздействия Направление, смещение равновесия реакции. N2 + O2 2NO - Q p, Равновесие не смещается, т.к. объем газов не меняется p, t, В сторону эндотермической реакции t, В сторону экзотермической реакции C(O2) или C(N2) В сторону прямой реакции C(O2) или C(N2) В сторону обратной реакции
Обратимые реакции Характер воздействия Направление, смещение равновесия реакции. N2 + O2 2NO - Q p, Равновесие не смещается, т.к. объем газов не меняется p, t, В сторону эндотермической реакции t, В сторону экзотермической реакции C(O2) или C(N2) В сторону прямой реакции C(O2) или C(N2) В сторону обратной реакции