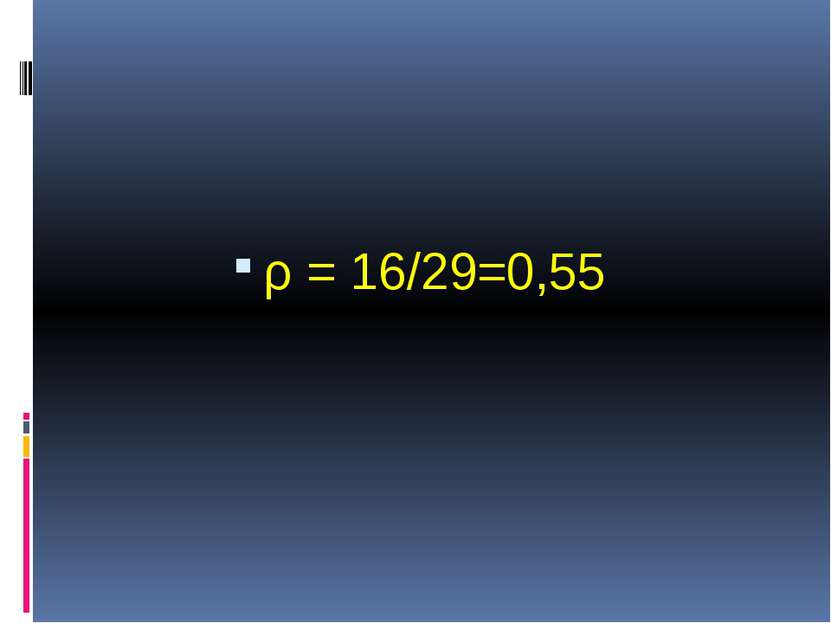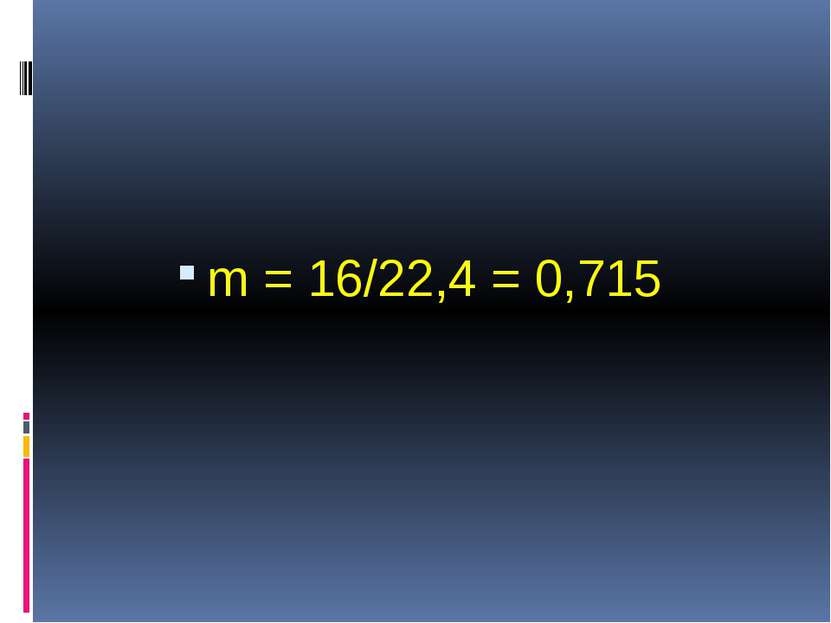X
Код презентации скопируйте его
Метан и его свойства
Скачать эту презентациюПрезентация на тему Метан и его свойства
Скачать эту презентациюCлайд 2
 Предельные углеводороды. Метан. Алканы. Общая формула предельных углеводородов. CnH2n+2 где n≥1. При образовании связей атома углерода с водородом образуется четыре SP3 электрона, взаимно отталкиваясь друг от друга занимает тетраэдрическое положение в пространстве, под углом 109˚28‘, расстояние между атомами 0,154 нм.
Предельные углеводороды. Метан. Алканы. Общая формула предельных углеводородов. CnH2n+2 где n≥1. При образовании связей атома углерода с водородом образуется четыре SP3 электрона, взаимно отталкиваясь друг от друга занимает тетраэдрическое положение в пространстве, под углом 109˚28‘, расстояние между атомами 0,154 нм.
Cлайд 3
 Физические свойства. Метан – газ, без цвета и запаха, легче воздуха (Мr = 16), малорастворим в воде.
Физические свойства. Метан – газ, без цвета и запаха, легче воздуха (Мr = 16), малорастворим в воде.
Cлайд 4
 Химические свойства. Горит. С воздухом образует взрывчатые смеси. СН4 + 2О2 → СО2 + 2Н2О При недостатке кислорода протекает неполное сгорание. СН4 + О2 → С + 2Н2О В присутствии катализаторов (нитрозных газов) могут образоваться метиловый спирт и формальдегид. СН4 + О2 → Н-С=О + Н2О │ Н 2СН4 + О2 → 2Н3С-ОН
Химические свойства. Горит. С воздухом образует взрывчатые смеси. СН4 + 2О2 → СО2 + 2Н2О При недостатке кислорода протекает неполное сгорание. СН4 + О2 → С + 2Н2О В присутствии катализаторов (нитрозных газов) могут образоваться метиловый спирт и формальдегид. СН4 + О2 → Н-С=О + Н2О │ Н 2СН4 + О2 → 2Н3С-ОН
Cлайд 5
 При сильном нагревании получают сажу. СН4 → С + 2Н2 Промежуточный продукт 2СН4 → С2Н4 + 2Н2; 2СН4 → С2Н2 + 3Н2 Ацетилен в 2 раза дешевле полученного из карбида кальция. Конверсией получают чистый водород. Метан стоик при обычных условиях к щелочам, кислотам и окислителям. Он не способен к реакциям присоединения, зато для него характерны реакции замещения.
При сильном нагревании получают сажу. СН4 → С + 2Н2 Промежуточный продукт 2СН4 → С2Н4 + 2Н2; 2СН4 → С2Н2 + 3Н2 Ацетилен в 2 раза дешевле полученного из карбида кальция. Конверсией получают чистый водород. Метан стоик при обычных условиях к щелочам, кислотам и окислителям. Он не способен к реакциям присоединения, зато для него характерны реакции замещения.
Cлайд 6
 На свету с Cl2 или Br2 эта реакция протекает по свободно-радикальному механизму со взрывом. Cl2 → 2Cl* СН4 + Cl*→ СН3* + НCl СН3*+ Cl2 → СН3Cl + Cl* СН3Cl + Cl*→ СН2Cl* + НCl СН2Cl* + Cl2 → СН2Cl2 + Cl* СН2Cl2 + Cl*→ СНCl2 * + НCl СНCl2* + Cl2 → СHCl3 + Cl* СHCl3 + Cl*→ СCl3* + HCl СCl3* + Cl2 → СCl4 + Cl*
На свету с Cl2 или Br2 эта реакция протекает по свободно-радикальному механизму со взрывом. Cl2 → 2Cl* СН4 + Cl*→ СН3* + НCl СН3*+ Cl2 → СН3Cl + Cl* СН3Cl + Cl*→ СН2Cl* + НCl СН2Cl* + Cl2 → СН2Cl2 + Cl* СН2Cl2 + Cl*→ СНCl2 * + НCl СНCl2* + Cl2 → СHCl3 + Cl* СHCl3 + Cl*→ СCl3* + HCl СCl3* + Cl2 → СCl4 + Cl*
Cлайд 7
 Обрыв реакции. Реакция может обрываться, если прореагирует два радикала, типа: СН3* + СН3* → С2Н6; СН3* + Cl*→ СН3Cl; Cl*+ Cl*→ Cl2 Хлористый метил – газ легко сжижающийся, используется как хладоагент. Остальные жидкости применяются как растворители смол, каучуков и д.р. органических веществ. СCl4 используется в огнетушителях, там, где нельзя использовать воду.
Обрыв реакции. Реакция может обрываться, если прореагирует два радикала, типа: СН3* + СН3* → С2Н6; СН3* + Cl*→ СН3Cl; Cl*+ Cl*→ Cl2 Хлористый метил – газ легко сжижающийся, используется как хладоагент. Остальные жидкости применяются как растворители смол, каучуков и д.р. органических веществ. СCl4 используется в огнетушителях, там, где нельзя использовать воду.
Cлайд 8
 Метан в природе. Метан широко распространён в природе, он является главной составной частью многих природных газов. (90-98%). Образуется при сухой перегонке древесины, торфа, кокса, при крекинге нефти. Кроме метана в попутных газах есть этан, пропан, бутан и пентан. Лабораторный способ получения метана. CH3COONa + NaOH → CH4 + Na2CO3 Al4C3 + 12H2O → 3CH4 + 4 Al(OH)3
Метан в природе. Метан широко распространён в природе, он является главной составной частью многих природных газов. (90-98%). Образуется при сухой перегонке древесины, торфа, кокса, при крекинге нефти. Кроме метана в попутных газах есть этан, пропан, бутан и пентан. Лабораторный способ получения метана. CH3COONa + NaOH → CH4 + Na2CO3 Al4C3 + 12H2O → 3CH4 + 4 Al(OH)3
Cлайд 9
 Синтетический способ получения метана. Ni(1200 ˚C) C + 2H2 → CH4; Ni,NiCO3,Co CO + 3H2 → CH4 + H2O; Ni,NiCO3,Co CO2 + 4H2 → CH4 + 2H2O Эти способы получения метана имеют промышленное значение.
Синтетический способ получения метана. Ni(1200 ˚C) C + 2H2 → CH4; Ni,NiCO3,Co CO + 3H2 → CH4 + H2O; Ni,NiCO3,Co CO2 + 4H2 → CH4 + 2H2O Эти способы получения метана имеют промышленное значение.
Cлайд 10
 Применение. Используется как топливо, для получения водорода, этилена, ацетилена, сажи, для получения спирта и формальдегида. Получение синтез-газа который используется в доменном процессе: Ni,MgCO3 CH4 + H2O → CO + 3H2 H2SO4 CH4 + HNO3 → CH3- NO2 + H2O
Применение. Используется как топливо, для получения водорода, этилена, ацетилена, сажи, для получения спирта и формальдегида. Получение синтез-газа который используется в доменном процессе: Ni,MgCO3 CH4 + H2O → CO + 3H2 H2SO4 CH4 + HNO3 → CH3- NO2 + H2O