X
Код презентации скопируйте его
АЛЮМИНИЙ
Скачать эту презентациюПрезентация на тему АЛЮМИНИЙ
Скачать эту презентациюCлайд 2
 Из глины я обыкновенной, И на редкость современный, Не боюсь электротока, Хозяйкам на кухне служу без срока, Бесстрашно в воздухе лечу, Мне все задачи по плечу. Конструкции лёгкие из дюрали, Не перечислить всех регалий, Горжусь своим я именем Зовусь я …
Из глины я обыкновенной, И на редкость современный, Не боюсь электротока, Хозяйкам на кухне служу без срока, Бесстрашно в воздухе лечу, Мне все задачи по плечу. Конструкции лёгкие из дюрали, Не перечислить всех регалий, Горжусь своим я именем Зовусь я …
Cлайд 4
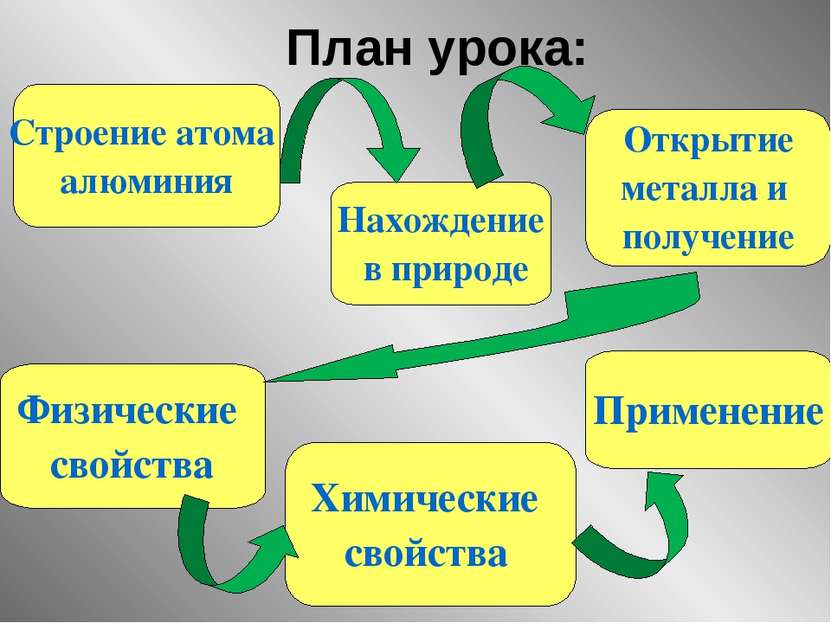
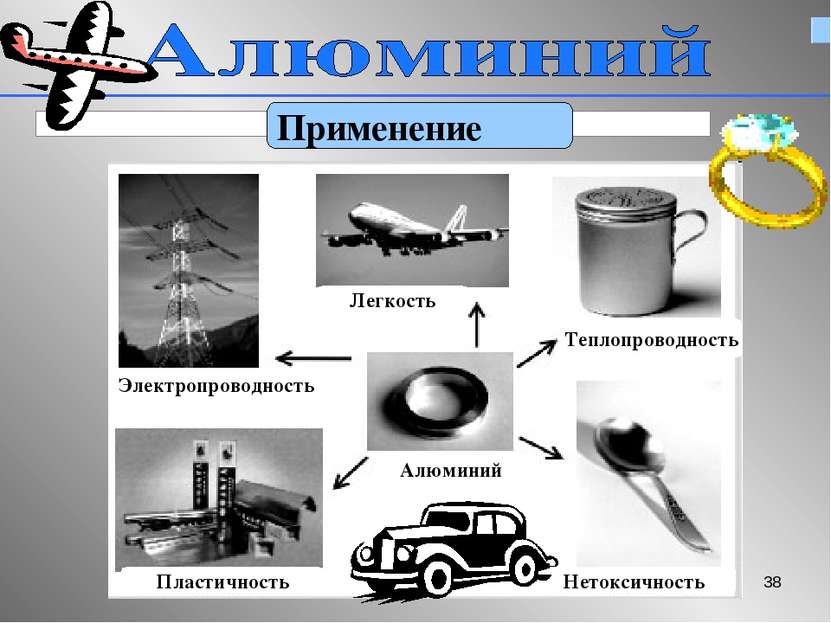
 План урока: Строение атома алюминия Нахождение в природе Открытие металла и получение Физические свойства Химические свойства Применение
План урока: Строение атома алюминия Нахождение в природе Открытие металла и получение Физические свойства Химические свойства Применение
Cлайд 6
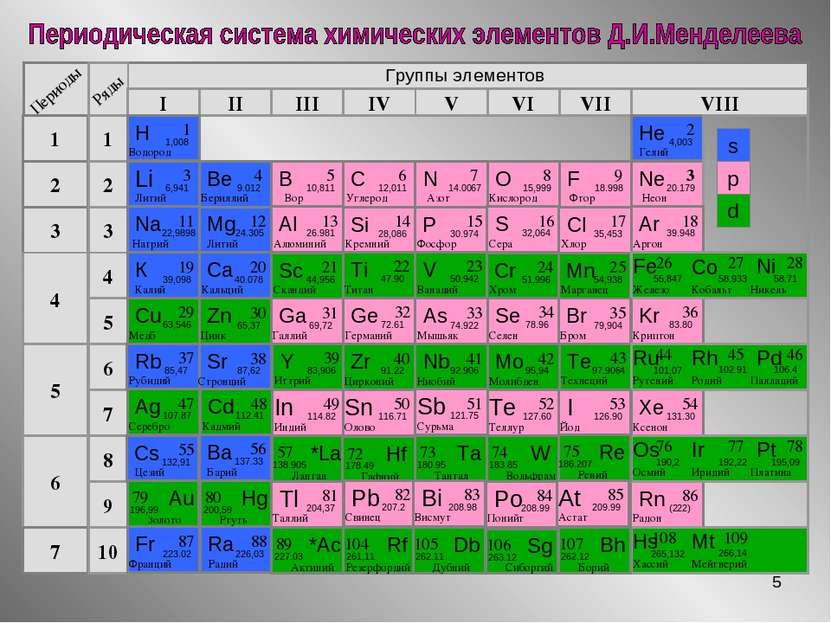
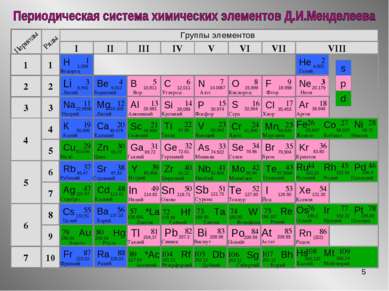
 * Периодическая система химических элементов Д.И.Менделеева Периоды 1 2 3 4 5 6 7 Ряды 1 2 3 4 10 9 8 7 5 6 Группы элементов I II VI V VII III IV VIII Al Характеристика Впервые получен в 1825 году Гансом Эрстедом. В Периодической системе расположен в 3 периоде, IIIА-группе. В природе встречается только в виде соединений. Серебристо-белый, легкий металл. Обладает высокой тепло- и электропроводностью. Валентность: III. Степень окисления: +3. Губарева В.А.
* Периодическая система химических элементов Д.И.Менделеева Периоды 1 2 3 4 5 6 7 Ряды 1 2 3 4 10 9 8 7 5 6 Группы элементов I II VI V VII III IV VIII Al Характеристика Впервые получен в 1825 году Гансом Эрстедом. В Периодической системе расположен в 3 периоде, IIIА-группе. В природе встречается только в виде соединений. Серебристо-белый, легкий металл. Обладает высокой тепло- и электропроводностью. Валентность: III. Степень окисления: +3. Губарева В.А.
Cлайд 10
 * 1. Из истории открытия Впервые Al был получен датским физиком Эрстедом Х. в 1825 г. Название элемента происходит от лат. алюмен, так в древности называли квасцы, которые использовали для крашения тканей (KAl(SO4)2 . 12H2O). Позже в 1827 г. немецкий химик Фридрих Велер получил алюминий следующим способом:
* 1. Из истории открытия Впервые Al был получен датским физиком Эрстедом Х. в 1825 г. Название элемента происходит от лат. алюмен, так в древности называли квасцы, которые использовали для крашения тканей (KAl(SO4)2 . 12H2O). Позже в 1827 г. немецкий химик Фридрих Велер получил алюминий следующим способом:
Cлайд 11
 * 1. Из истории открытия В период открытия алюминия - металл был дороже золота. Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции.
* 1. Из истории открытия В период открытия алюминия - металл был дороже золота. Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции.
Cлайд 12
 В 1852г. килограмм алюминия стоил 1200 долларов – дороже золота! Когда его открыли в 1825 году, он стоил в 1500 раз дороже железа. Даже 30 лет спустя на его слиток, демонстрировавшийся на Всемирной выставке в Париже смотрели как на драгоценность.
В 1852г. килограмм алюминия стоил 1200 долларов – дороже золота! Когда его открыли в 1825 году, он стоил в 1500 раз дороже железа. Даже 30 лет спустя на его слиток, демонстрировавшийся на Всемирной выставке в Париже смотрели как на драгоценность.
Cлайд 13
 К концу XX века алюминий стал намного дешевле , т.к. Чарльз Холл изобрел способ получения алюминия электролизом
К концу XX века алюминий стал намного дешевле , т.к. Чарльз Холл изобрел способ получения алюминия электролизом
Cлайд 14
 Метод Холла позволил получать сравнительно недорогой алюминий в больших масштабах. Если с 1855 до 1890 г. было произведено лишь 200 т алюминия, то за следующее десятилетие по новому методу – уже 28 тысяч тонн! Чарлз Холл разработал электролитический способ получения алюминия
Метод Холла позволил получать сравнительно недорогой алюминий в больших масштабах. Если с 1855 до 1890 г. было произведено лишь 200 т алюминия, то за следующее десятилетие по новому методу – уже 28 тысяч тонн! Чарлз Холл разработал электролитический способ получения алюминия
Cлайд 15
 Метод Чарлза Холла позволял получать сравнительно недорогой алюминий в больших масштабах – началась эпоха алюминия…
Метод Чарлза Холла позволял получать сравнительно недорогой алюминий в больших масштабах – началась эпоха алюминия…
Cлайд 17
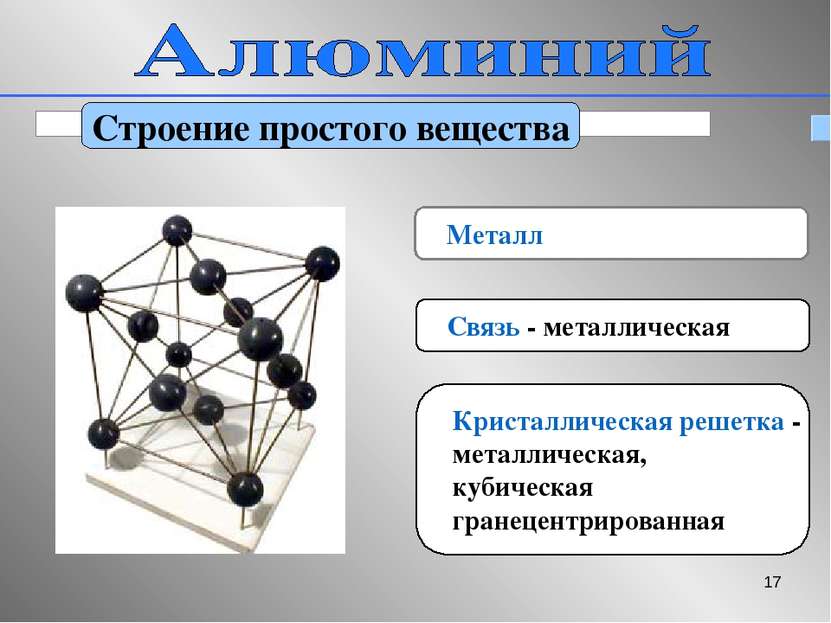
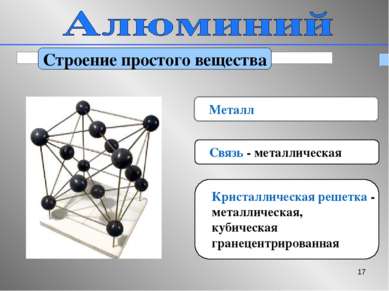 * Строение простого вещества Металл Связь - металлическая Кристаллическая решетка - металлическая, кубическая гранецентрированная
* Строение простого вещества Металл Связь - металлическая Кристаллическая решетка - металлическая, кубическая гранецентрированная
Cлайд 21
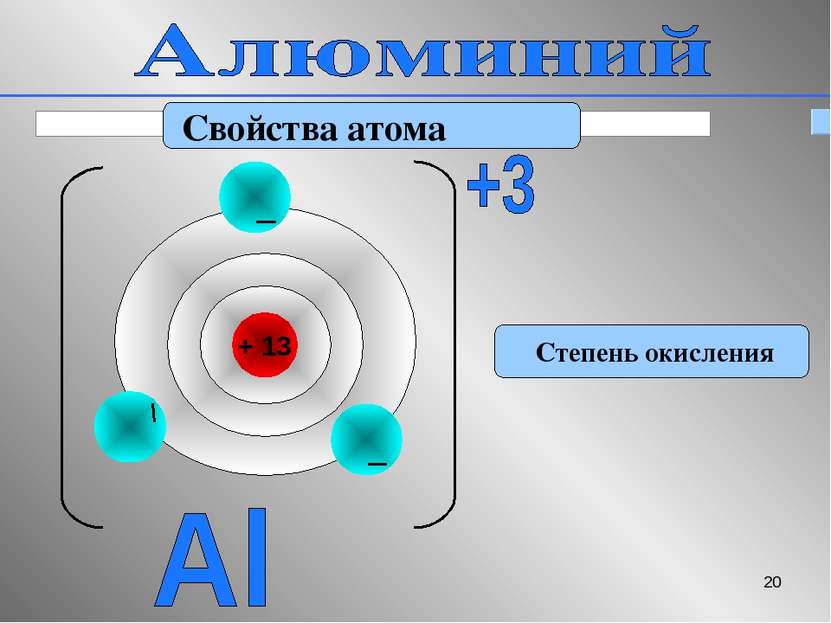
 * Свойства атома Восстановительные Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co, Pb,H2,Cu,Hg,Ag Ослабление восстановительных свойств
* Свойства атома Восстановительные Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co, Pb,H2,Cu,Hg,Ag Ослабление восстановительных свойств
Cлайд 24
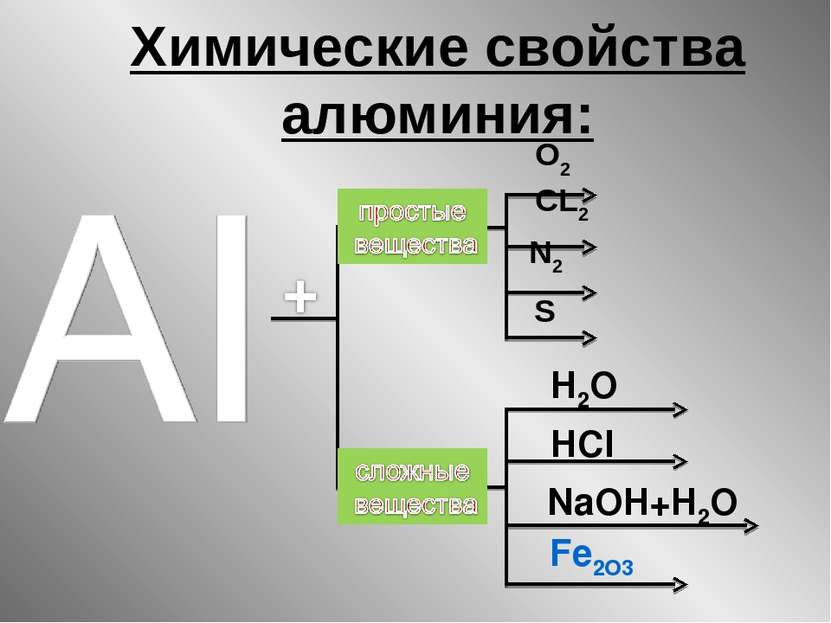
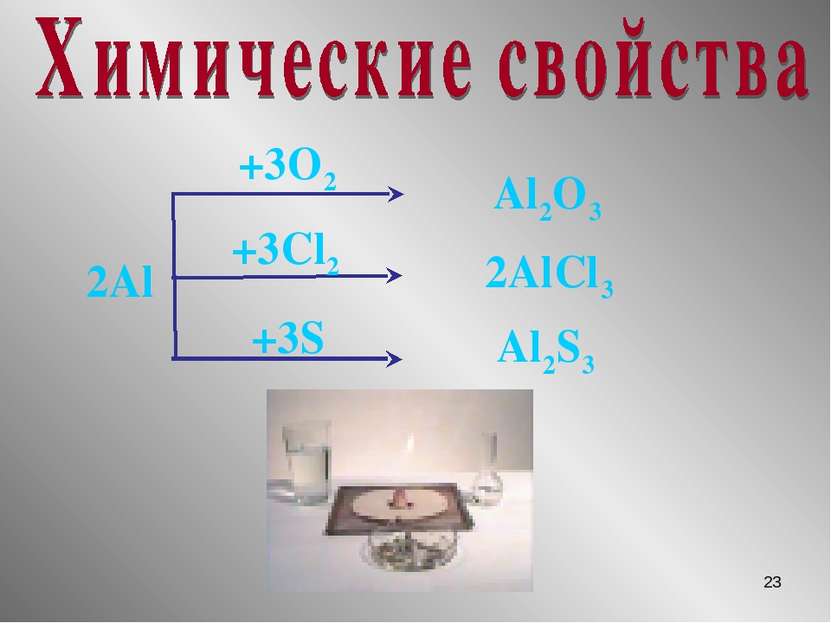
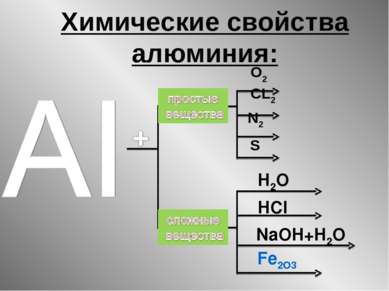
 Химические свойства. С водой: 2Al + 3H2O = 2Al(OH)3 + 3H2 Почему алюминиевую посуду используют в быту? Губарева В.А.
Химические свойства. С водой: 2Al + 3H2O = 2Al(OH)3 + 3H2 Почему алюминиевую посуду используют в быту? Губарева В.А.
Cлайд 25
 Алюминий – очень активный металл. Однако при комнатной температуре на воздухе алюминий не изменяется, поскольку его поверхность покрыта очень прочной тонкой оксидной плёнкой, которая защищает металл от воздействия компонентов воздуха и воды.
Алюминий – очень активный металл. Однако при комнатной температуре на воздухе алюминий не изменяется, поскольку его поверхность покрыта очень прочной тонкой оксидной плёнкой, которая защищает металл от воздействия компонентов воздуха и воды.
Cлайд 26
 Алюминий без защиты Лишенный оксидной пленки, алюминий активно взаимодействует с водой, а на воздухе быстро окисляется, при этом металл нагревается и обрастает белой «бородой» оксида
Алюминий без защиты Лишенный оксидной пленки, алюминий активно взаимодействует с водой, а на воздухе быстро окисляется, при этом металл нагревается и обрастает белой «бородой» оксида
Cлайд 27
 Химические свойства. С кислотами: соляной серной фосфорной 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 3H2SO4 = Al2(SO4)3+ 3H2 Al + H3PO4 = не возможно Губарева В.А.
Химические свойства. С кислотами: соляной серной фосфорной 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 3H2SO4 = Al2(SO4)3+ 3H2 Al + H3PO4 = не возможно Губарева В.А.
Cлайд 28
 НО образуется нерастворимая соль AlPO4. Доступ кислоты H3PO4 к алюминию невозможен. Реакция прекращается. Al + H3PO4 AlPO4 + H2
НО образуется нерастворимая соль AlPO4. Доступ кислоты H3PO4 к алюминию невозможен. Реакция прекращается. Al + H3PO4 AlPO4 + H2
Cлайд 29
 Алюминий – нетипичный металл 2 Аl + 6 HCl = 2 AlCl3 +3 Н2↑ алюминий хлорид 2 Аl + 2NaOH + 6 Н2О = 2 Na[Al(OH)4] + 3 H2↑ натрий алюминат
Алюминий – нетипичный металл 2 Аl + 6 HCl = 2 AlCl3 +3 Н2↑ алюминий хлорид 2 Аl + 2NaOH + 6 Н2О = 2 Na[Al(OH)4] + 3 H2↑ натрий алюминат
Cлайд 30
 Химическая природа Al2O3 Al2O3 – амфотерен Al2O3 + 6 НCl = 2AlCl3 + 3 Н2О Al2O3+2NaOH+6H2O = 2Na[Al(OH)4]+3H2↑
Химическая природа Al2O3 Al2O3 – амфотерен Al2O3 + 6 НCl = 2AlCl3 + 3 Н2О Al2O3+2NaOH+6H2O = 2Na[Al(OH)4]+3H2↑
Cлайд 31
 Почему алюминиевую кастрюлю не рекомендуется мыть с содой ? Раствор соды обладает щелочной реакцией, поэтому алюминий может постепенно просто растворяться, взаимодействуя со щелочью
Почему алюминиевую кастрюлю не рекомендуется мыть с содой ? Раствор соды обладает щелочной реакцией, поэтому алюминий может постепенно просто растворяться, взаимодействуя со щелочью
Cлайд 32
 Химические свойства. С растворами солей: хлоридом железа (III) хлоридом натрия Al + FeCl3 = AlCl3 + Fe Al + NaCl = не возможно Губарева В.А.
Химические свойства. С растворами солей: хлоридом железа (III) хлоридом натрия Al + FeCl3 = AlCl3 + Fe Al + NaCl = не возможно Губарева В.А.
Cлайд 33
 Al + NaCl AlCl3 +Na Но алюминий в электрохимическом ряду напряжений металлов: K Ca Na Mg Al Zn Fe Pb H2 Cu Ag Hg Pt находится правее натрия, а значит его восстановительные свойства меньше, чем у натрия. Следовательно, алюминий не может вытеснить натрий из его солей.
Al + NaCl AlCl3 +Na Но алюминий в электрохимическом ряду напряжений металлов: K Ca Na Mg Al Zn Fe Pb H2 Cu Ag Hg Pt находится правее натрия, а значит его восстановительные свойства меньше, чем у натрия. Следовательно, алюминий не может вытеснить натрий из его солей.
Cлайд 34
 Алюминий может покраснеть …!!! 2Аl + 3СиSO4 = Al2(SO4 )3 + 3 Cu Al – является восстановителем Алюминий покрылся медным налетом в растворе медного купороса
Алюминий может покраснеть …!!! 2Аl + 3СиSO4 = Al2(SO4 )3 + 3 Cu Al – является восстановителем Алюминий покрылся медным налетом в растворе медного купороса
Cлайд 35
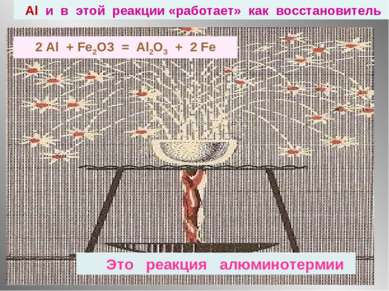 Это реакция алюминотермии Аl и в этой реакции «работает» как восстановитель 2 Al + Fe2O3 = Al2O3 + 2 Fe
Это реакция алюминотермии Аl и в этой реакции «работает» как восстановитель 2 Al + Fe2O3 = Al2O3 + 2 Fe
Cлайд 40
 Алюминий – «крылатый металл» Входит в состав известных сплавов – дюралюминий, магналий, силумин, используемых в самолетостроении Используемые свойства: легкость, прочность, коррозионная стойкость (устойчивость к воздуху и воде )
Алюминий – «крылатый металл» Входит в состав известных сплавов – дюралюминий, магналий, силумин, используемых в самолетостроении Используемые свойства: легкость, прочность, коррозионная стойкость (устойчивость к воздуху и воде )
Cлайд 47
 Алюминий в электротехнике Используемые свойства Высокая электропроводность Легкость При одинаковом электросопротивлении алюминиевый провод весит вдвое меньше медного
Алюминий в электротехнике Используемые свойства Высокая электропроводность Легкость При одинаковом электросопротивлении алюминиевый провод весит вдвое меньше медного
Cлайд 50
 Алюминий в быту Используемые свойства: легкость,прочность,коррозионная прочность, нетоксичность
Алюминий в быту Используемые свойства: легкость,прочность,коррозионная прочность, нетоксичность
Cлайд 51
 Термит – смесь Fe3O4 с порошком Al. При поджигании смеси происходит энергичная реакция с выделением большого количества теплоты, которой достаточно для полного расплавления получаемого железа. 8Al + 3Fe3O4 4Al2O3 + 9Fe Этот процесс используют для сварки стальных рельс.
Термит – смесь Fe3O4 с порошком Al. При поджигании смеси происходит энергичная реакция с выделением большого количества теплоты, которой достаточно для полного расплавления получаемого железа. 8Al + 3Fe3O4 4Al2O3 + 9Fe Этот процесс используют для сварки стальных рельс.
Cлайд 52
 * Металл будущего Вывод: Обладая такими свойствами как лёгкость, прочность, коррозионноустойчивость, устойчивость к действию сильных химических реагентов - алюминий нашёл большое значение в авиационном и космическом транспорте применение во многих отраслях народного хозяйства. Особое место алюминий и его сплавы занимают в электротехнике, а за ними будущее нашей науки и техники.
* Металл будущего Вывод: Обладая такими свойствами как лёгкость, прочность, коррозионноустойчивость, устойчивость к действию сильных химических реагентов - алюминий нашёл большое значение в авиационном и космическом транспорте применение во многих отраслях народного хозяйства. Особое место алюминий и его сплавы занимают в электротехнике, а за ними будущее нашей науки и техники.
Cлайд 53
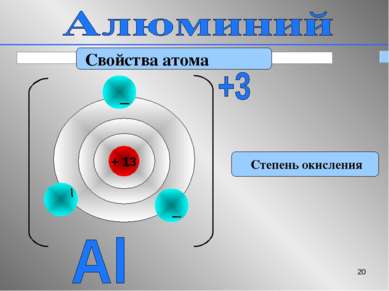
 * Вставьте пропущенные слова Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом. Оксид и гидроксид алюминия имеют амфотерный характер.
* Вставьте пропущенные слова Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом. Оксид и гидроксид алюминия имеют амфотерный характер.