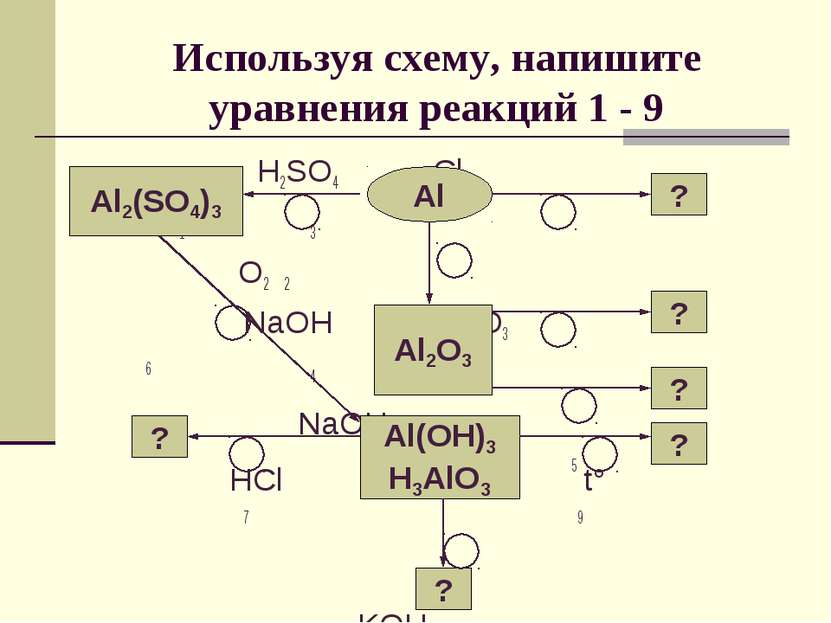
X
Код презентации скопируйте его
Алюминий и его соединения
Скачать эту презентациюПрезентация на тему Алюминий и его соединения
Скачать эту презентациюCлайд 1
 Презентация Поспеловой С.В. учителя химии ГОУ школа №122 Центрального р-на Санкт-Петербурга Алюминий и его соединения
Презентация Поспеловой С.В. учителя химии ГОУ школа №122 Центрального р-на Санкт-Петербурга Алюминий и его соединения
Cлайд 2
 Положение в Периодической системе Алюминий располагается в 3 периоде, в главной подгруппе 3 группы. Порядковый номер элемента – 13 Относительная атомная масса – 27 Алюминий – металл, соединения которого обладают амфотерными свойствами.
Положение в Периодической системе Алюминий располагается в 3 периоде, в главной подгруппе 3 группы. Порядковый номер элемента – 13 Относительная атомная масса – 27 Алюминий – металл, соединения которого обладают амфотерными свойствами.
Cлайд 3
 Строение атома алюминия Заряд ядра атома алюминия +13 В атоме 3 энергетических уровня Электронная оболочка атома алюминия содержит s- и p-электроны На внешнем электронном уровне 3 электрона (2 – спаренных s-электрона и 1 – неспаренный p-электрон)
Строение атома алюминия Заряд ядра атома алюминия +13 В атоме 3 энергетических уровня Электронная оболочка атома алюминия содержит s- и p-электроны На внешнем электронном уровне 3 электрона (2 – спаренных s-электрона и 1 – неспаренный p-электрон)
Cлайд 4
 Нахождение в природе По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов. Встречается только в составе соединений.
Нахождение в природе По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов. Встречается только в составе соединений.
Cлайд 5
 Получение алюминия Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути. Название элемента образовано от лат. aluminis — квасцы. AlCl3 + 3K = 3KCl + Al В настоящее время алюминий получают электролизом оксида: эл.ток 2Al2O3 = 4Al + 3O2 – 3352 кДж
Получение алюминия Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути. Название элемента образовано от лат. aluminis — квасцы. AlCl3 + 3K = 3KCl + Al В настоящее время алюминий получают электролизом оксида: эл.ток 2Al2O3 = 4Al + 3O2 – 3352 кДж
Cлайд 6
 Физические свойства плотность (при 20°С) 2698,9 кг/м3; tпл 660,24°С; tкип около 2500°С; Алюминий сочетает весьма ценный комплекс свойств: малую плотность, высокие теплопровод-ность и электрическую проводимость, высокую пластичность и хорошую коррозионную стойкость, обладает высокой отражательной способностью, близкой к серебру (он отражает до 90% падающей световой энергии). На воздухе алюминий покрывается тонкой, но очень прочной пленкой оксида Al2О3, защищающей металл от дальнейшего окисления и обусловливающей его высокие антикоррозионные свойства.
Физические свойства плотность (при 20°С) 2698,9 кг/м3; tпл 660,24°С; tкип около 2500°С; Алюминий сочетает весьма ценный комплекс свойств: малую плотность, высокие теплопровод-ность и электрическую проводимость, высокую пластичность и хорошую коррозионную стойкость, обладает высокой отражательной способностью, близкой к серебру (он отражает до 90% падающей световой энергии). На воздухе алюминий покрывается тонкой, но очень прочной пленкой оксида Al2О3, защищающей металл от дальнейшего окисления и обусловливающей его высокие антикоррозионные свойства.
Cлайд 7
 Химические свойства Окисляется на воздухе: 4Al + 3O2 = 2Al2O3 4 Al0 - 3ē → Al+3 окисление, восстановитель 3 O20 + 4ē → 2O-2 восстановление, окислитель Вытесняет водород из воды 2Al + 6H2O = 2Al(OH)3 + 3H2↑ 4 Al0 - 3ē → Al+3 окисление, восстановитель 3 2H+1 + 2ē → H20 восстановление, окислитель
Химические свойства Окисляется на воздухе: 4Al + 3O2 = 2Al2O3 4 Al0 - 3ē → Al+3 окисление, восстановитель 3 O20 + 4ē → 2O-2 восстановление, окислитель Вытесняет водород из воды 2Al + 6H2O = 2Al(OH)3 + 3H2↑ 4 Al0 - 3ē → Al+3 окисление, восстановитель 3 2H+1 + 2ē → H20 восстановление, окислитель
Cлайд 8
 Химические свойства Взаимодействует с кислотами: 2Al + 6HCl = 2AlCl3 + 3H2↑ 2Al + 6H+ + 6Cl- = 2Al3+ + 6Cl-+ 3H2↑ 2Al + 6H+ = 2Al3+ + 3H2↑ Взаимодействует со щелочами: 2Al + 2H2O + 2NaOH = 2NaAlO2 + 3H2↑ 2Al + 2H2O + 2Na+ + 2OH- = 2Na+ + 2AlO2- + 3H2↑ 2Al + 2H2O + 2OH- = 2AlO2- + 3H2↑
Химические свойства Взаимодействует с кислотами: 2Al + 6HCl = 2AlCl3 + 3H2↑ 2Al + 6H+ + 6Cl- = 2Al3+ + 6Cl-+ 3H2↑ 2Al + 6H+ = 2Al3+ + 3H2↑ Взаимодействует со щелочами: 2Al + 2H2O + 2NaOH = 2NaAlO2 + 3H2↑ 2Al + 2H2O + 2Na+ + 2OH- = 2Na+ + 2AlO2- + 3H2↑ 2Al + 2H2O + 2OH- = 2AlO2- + 3H2↑
Cлайд 9
 Химические свойства Вытесняет металлы из их оксидов (алюминотермия): 8Al + 3Fe3O4 = 9Fe + 4Al2O3 8 Al0 - 3ē → Al+3 – окисление, восстановитель 3 24 Fe+2 + 2ē → Fe0 – восстановление, ок-ль 3 2Fe+3 + 6ē → 2Fe0 – восстановление, ок-ль
Химические свойства Вытесняет металлы из их оксидов (алюминотермия): 8Al + 3Fe3O4 = 9Fe + 4Al2O3 8 Al0 - 3ē → Al+3 – окисление, восстановитель 3 24 Fe+2 + 2ē → Fe0 – восстановление, ок-ль 3 2Fe+3 + 6ē → 2Fe0 – восстановление, ок-ль
Cлайд 10
 Соединения алюминия. Оксид Очень твердый порошок белого цвета. Образуется: а) при окислении или горении алюминия: 4Al + 3O2 = 2Al2O3 б) в реакции алюминотермии: 2Al + Fe2O3 = 2Fe + Al2O3 в) при термическом разложении гидроксида: 2Al(OH)3 = Al2O3 + H2O
Соединения алюминия. Оксид Очень твердый порошок белого цвета. Образуется: а) при окислении или горении алюминия: 4Al + 3O2 = 2Al2O3 б) в реакции алюминотермии: 2Al + Fe2O3 = 2Fe + Al2O3 в) при термическом разложении гидроксида: 2Al(OH)3 = Al2O3 + H2O
Cлайд 11
 Химические свойства оксида алюминия Al2O3 по характеру амфотерный оксид. Взаимодействует: а) с кислотами: Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O Al2O3 + 6H+ + 3SO42- = 2Al3+ + 3SO42- + 3H2O Al2O3 + 6H+ = 2Al3+ + 3H2O б) со щелочами: Al2O3 + 6NaOH = 2Na3AlO3 + 3H2O Al2O3 + 6Na+ + 6OH- = 6Na+ + 2AlO33- + 3H2O Al2O3 + 6OH- = 2AlO33- + 3H2O
Химические свойства оксида алюминия Al2O3 по характеру амфотерный оксид. Взаимодействует: а) с кислотами: Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O Al2O3 + 6H+ + 3SO42- = 2Al3+ + 3SO42- + 3H2O Al2O3 + 6H+ = 2Al3+ + 3H2O б) со щелочами: Al2O3 + 6NaOH = 2Na3AlO3 + 3H2O Al2O3 + 6Na+ + 6OH- = 6Na+ + 2AlO33- + 3H2O Al2O3 + 6OH- = 2AlO33- + 3H2O
Cлайд 12
 Гидроксид алюминия Белый нерастворимый в воде порошок Проявляет амфотерные свойства. Взаимодействует: а) с кислотами: Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O Al(OH)3 + 3H+ + 3NO3- = Al3+ + 3NO3- + 3H2O Al(OH)3 + 3H+ = Al3+ + 3H2O б) со щелочами: Al(OH)3 + 3KOH = K3AlO3 + 3H2O Al(OH)3 + 3K+ + 3OH- = 3K+ + AlO33- + 3H2O Al(OH)3 + 3OH- = AlO33- + 3H2O
Гидроксид алюминия Белый нерастворимый в воде порошок Проявляет амфотерные свойства. Взаимодействует: а) с кислотами: Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O Al(OH)3 + 3H+ + 3NO3- = Al3+ + 3NO3- + 3H2O Al(OH)3 + 3H+ = Al3+ + 3H2O б) со щелочами: Al(OH)3 + 3KOH = K3AlO3 + 3H2O Al(OH)3 + 3K+ + 3OH- = 3K+ + AlO33- + 3H2O Al(OH)3 + 3OH- = AlO33- + 3H2O