X
Код презентации скопируйте его
Алюминий – крылатый металл. Этому металлу принадлежит будущее
Скачать эту презентациюПрезентация на тему Алюминий – крылатый металл. Этому металлу принадлежит будущее
Скачать эту презентациюCлайд 2
 «Открытие алюминия» В 1825 г. датский физик Ханс Кристиан Эрстед был первым, кому удалось, подобно неизвестному мастеру Древнего Рима, получить относительно чистый алюминий; поскольку сообщение об этом было опубликовано в малоизвестном датском журнале и не сразу стало известно химикам, иногда первооткрывателем алюминия называют Ф. Вёлера.
«Открытие алюминия» В 1825 г. датский физик Ханс Кристиан Эрстед был первым, кому удалось, подобно неизвестному мастеру Древнего Рима, получить относительно чистый алюминий; поскольку сообщение об этом было опубликовано в малоизвестном датском журнале и не сразу стало известно химикам, иногда первооткрывателем алюминия называют Ф. Вёлера.
Cлайд 3
 «Серебро из глины» Немецкий учёный Ф. Велер (1827 г.) получил алюминий при нагревании хлорида алюминия со щелочными металлами: калием и натрием. А.Сент-Клер Девиль. Впервые получил алюминий промышленным способом (1855г.).
«Серебро из глины» Немецкий учёный Ф. Велер (1827 г.) получил алюминий при нагревании хлорида алюминия со щелочными металлами: калием и натрием. А.Сент-Клер Девиль. Впервые получил алюминий промышленным способом (1855г.).
Cлайд 4
 «Электролитический способ» В 1886 году Поль Эру французский инженер-химик запатентовал открытие способа получения алюминия Чарльз Мартин Холл американский ученый
«Электролитический способ» В 1886 году Поль Эру французский инженер-химик запатентовал открытие способа получения алюминия Чарльз Мартин Холл американский ученый
Cлайд 5
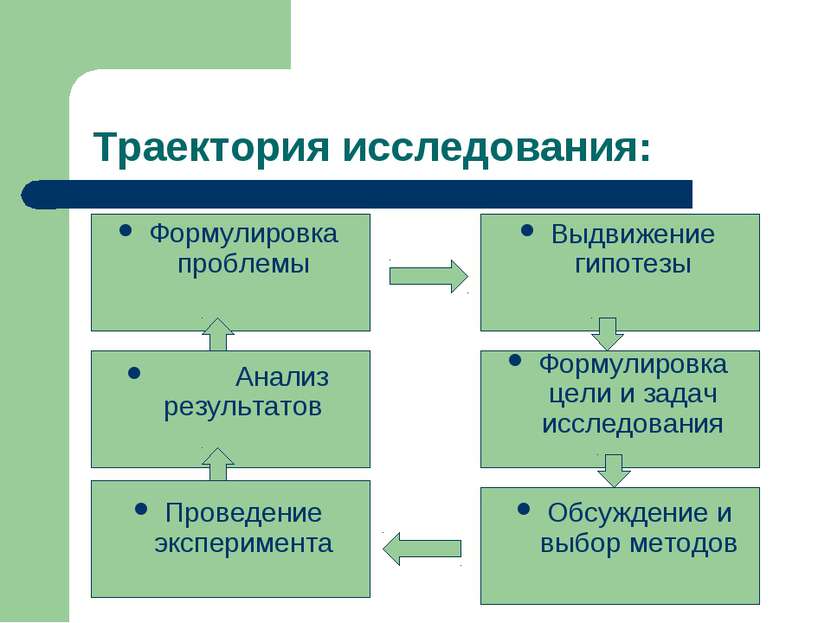
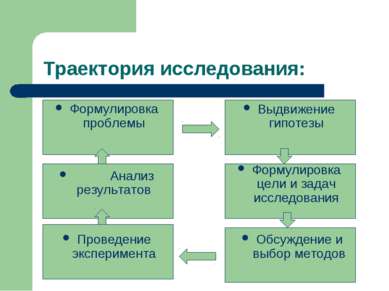 Траектория исследования: Формулировка проблемы Выдвижение гипотезы Формулировка цели и задач исследования Проведение эксперимента Обсуждение и выбор методов Анализ результатов
Траектория исследования: Формулировка проблемы Выдвижение гипотезы Формулировка цели и задач исследования Проведение эксперимента Обсуждение и выбор методов Анализ результатов
Cлайд 8
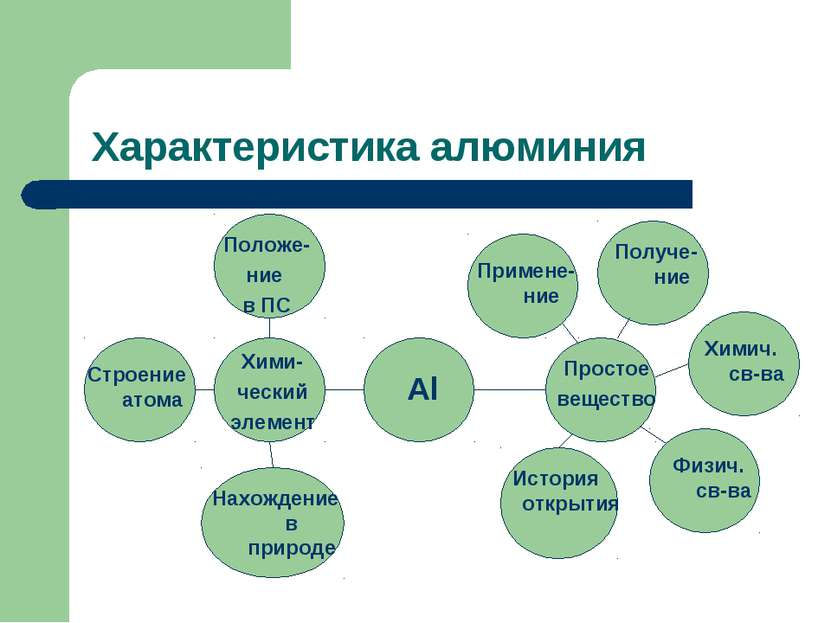
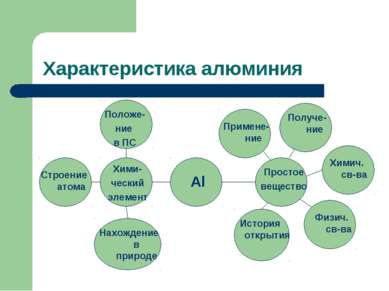 Характеристика алюминия Положе- ние в ПС Строение атома Примене- ние Al Хими- ческий элемент Нахождение в природе Простое вещество Физич. св-ва Химич. св-ва Получе-ние История открытия
Характеристика алюминия Положе- ние в ПС Строение атома Примене- ние Al Хими- ческий элемент Нахождение в природе Простое вещество Физич. св-ва Химич. св-ва Получе-ние История открытия
Cлайд 9
 Цель и задачи исследования: Ответить на вопрос: « Почему алюминий называют металлом будущего?» Дать характеристику элемента по его положению в периодической системе химических элементов. На основе строения атома рассмотреть его физические и химические свойства, указать области применения алюминия.
Цель и задачи исследования: Ответить на вопрос: « Почему алюминий называют металлом будущего?» Дать характеристику элемента по его положению в периодической системе химических элементов. На основе строения атома рассмотреть его физические и химические свойства, указать области применения алюминия.
Cлайд 10
 Положение алюминия в ПСХЭ Д.И.Менделеева. Строение атома. Порядковый номер 13 . Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом.
Положение алюминия в ПСХЭ Д.И.Менделеева. Строение атома. Порядковый номер 13 . Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом.
Cлайд 11
 Положение алюминия в ПСХЭ Д.И.Менделеева. Строение атома. Порядковый номер 13 . Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом.
Положение алюминия в ПСХЭ Д.И.Менделеева. Строение атома. Порядковый номер 13 . Алюминий - элемент III группы, главной подгруппы. Заряд ядра атома алюминия равен +13. В ядре атома алюминия 13 протонов. В ядре атома алюминия 14 нейтронов. В атоме алюминия 13 электронов. Атом алюминия имеет 3 энергетических уровня. Электронная оболочка имеет строение 2е, 8е, 3е. На внешнем уровне в атоме 3 электронов. Степень окисления атома в соединениях равна +3 . Простое вещество алюминий является металлом.
Cлайд 13
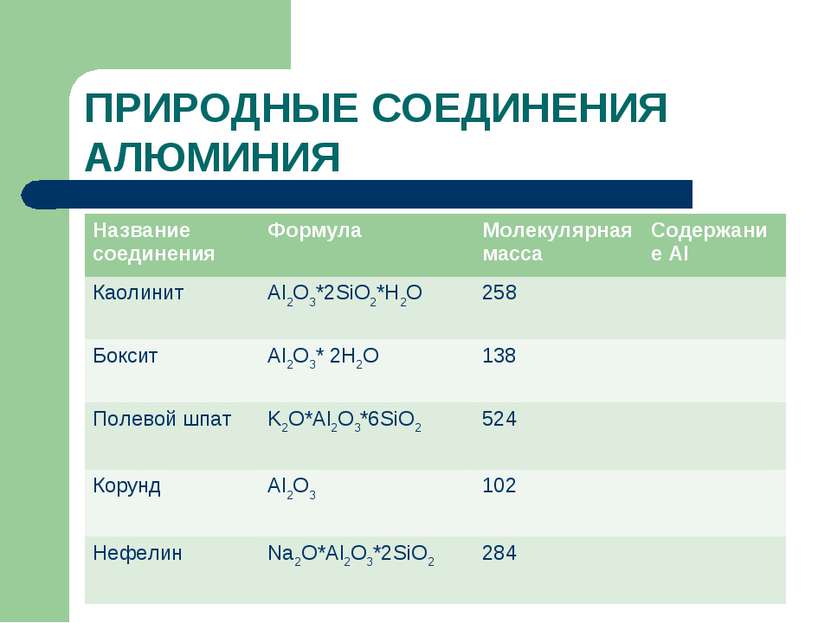
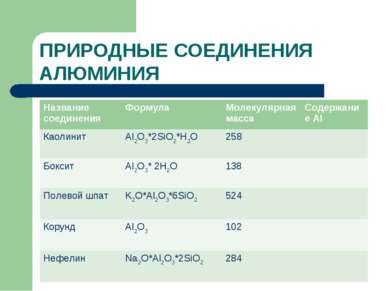 ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 Боксит Al2O3* 2H2O 138 Полевой шпат K2O*Al2O3*6SiO2 524 Корунд Al2O3 102 Нефелин Na2O*Al2O3*2SiO2 284
ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 Боксит Al2O3* 2H2O 138 Полевой шпат K2O*Al2O3*6SiO2 524 Корунд Al2O3 102 Нефелин Na2O*Al2O3*2SiO2 284
Cлайд 14
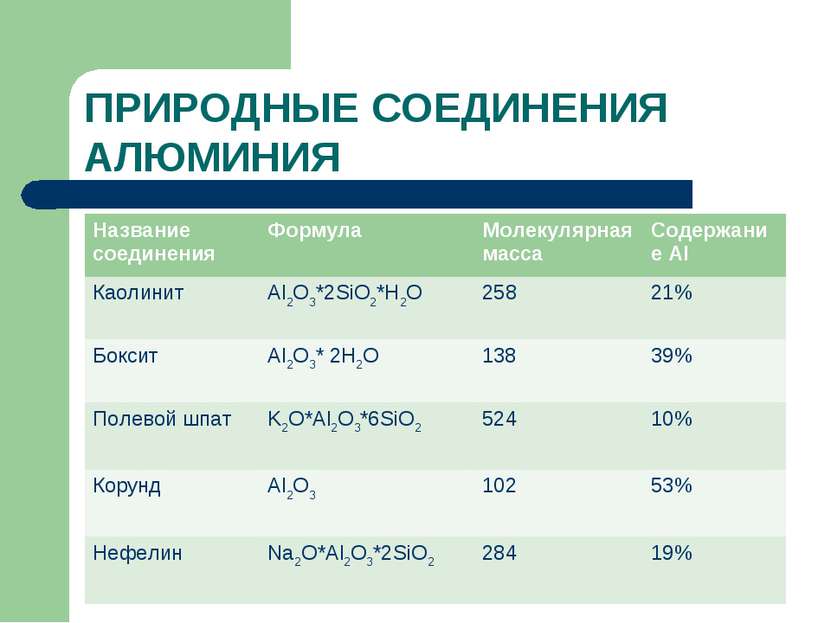
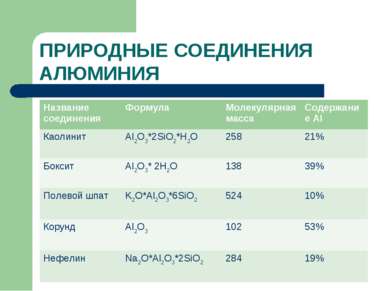 ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 21% Боксит Al2O3* 2H2O 100 39% Полевой шпат K2O*Al2O3*6SiO2 524 10% Корунд Al2O3 102 53% Нефелин Na2O*Al2O3*2SiO2 284 19% Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 21% Боксит Al2O3* 2H2O 138 39% Полевой шпат K2O*Al2O3*6SiO2 524 10% Корунд Al2O3 102 53% Нефелин Na2O*Al2O3*2SiO2 284 19%
ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 21% Боксит Al2O3* 2H2O 100 39% Полевой шпат K2O*Al2O3*6SiO2 524 10% Корунд Al2O3 102 53% Нефелин Na2O*Al2O3*2SiO2 284 19% Название соединения Формула Молекулярная масса Содержание Al Каолинит Al2O3*2SiO2*H2O 258 21% Боксит Al2O3* 2H2O 138 39% Полевой шпат K2O*Al2O3*6SiO2 524 10% Корунд Al2O3 102 53% Нефелин Na2O*Al2O3*2SiO2 284 19%
Cлайд 16
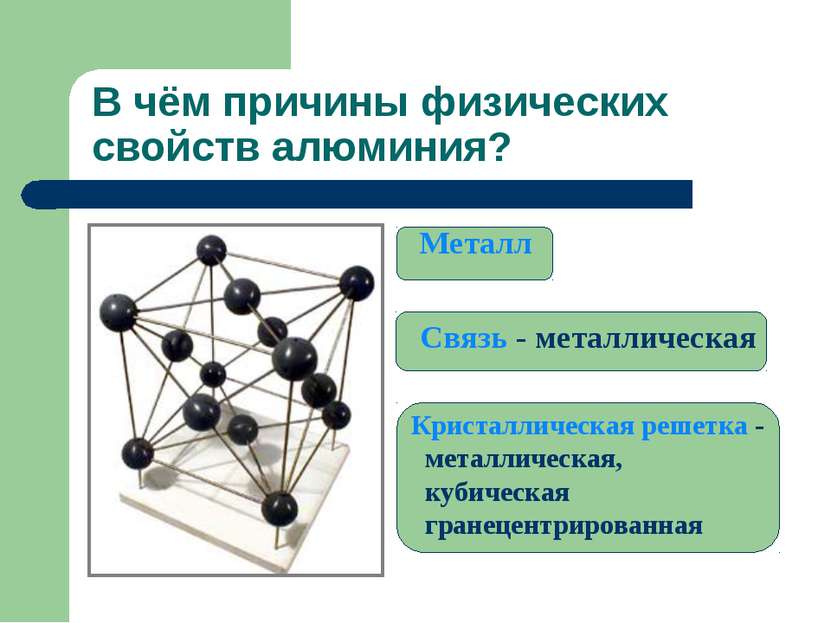
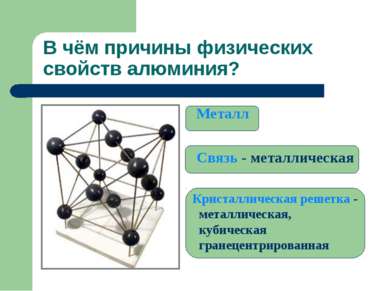 В чём причины физических свойств алюминия? Металл Связь - металлическая Кристаллическая решетка - металлическая, кубическая гранецентрированная
В чём причины физических свойств алюминия? Металл Связь - металлическая Кристаллическая решетка - металлическая, кубическая гранецентрированная
Cлайд 17
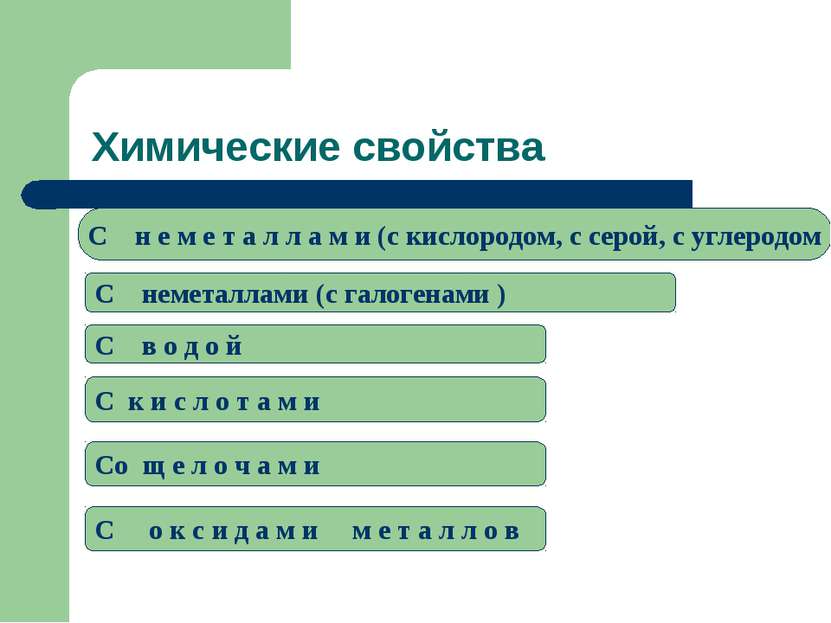
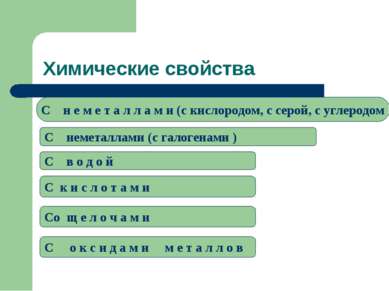 Химические свойства C н е м е т а л л а м и (c кислородом, с серой, с углеродом C неметаллами (c галогенами ) C в о д о й C к и с л о т а м и Cо щ е л о ч а м и C о к с и д а м и м е т а л л о в
Химические свойства C н е м е т а л л а м и (c кислородом, с серой, с углеродом C неметаллами (c галогенами ) C в о д о й C к и с л о т а м и Cо щ е л о ч а м и C о к с и д а м и м е т а л л о в
Cлайд 19
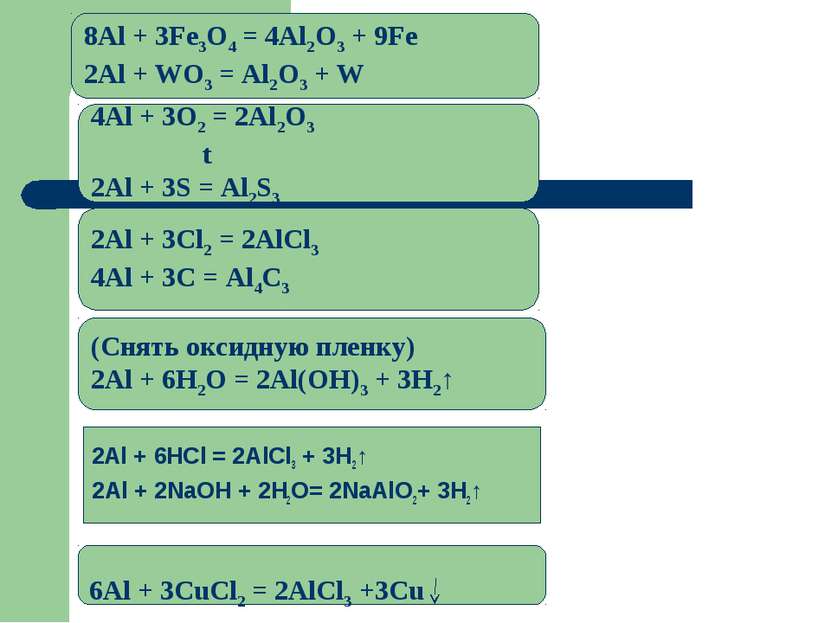
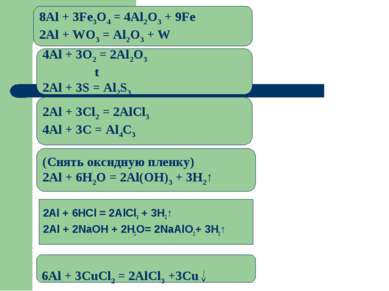 2Al + 6HCl = 2AlCl3 + 3H2↑ 2Al + 2NaOH + 2H2O= 2NaAlO2+ 3H2↑ (Снять оксидную пленку) 2Al + 6H2O = 2Al(OH)3 + 3H2↑ 2Аl + 3Cl2 = 2AlCl3 4Al + 3C = Al4C3 4Аl + 3O2 = 2Al2O3 t 2Al + 3S = Al2S3 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + WO3 = Al2O3 + W 6Al + 3CuCl2 = 2AlCl3 +3Cu
2Al + 6HCl = 2AlCl3 + 3H2↑ 2Al + 2NaOH + 2H2O= 2NaAlO2+ 3H2↑ (Снять оксидную пленку) 2Al + 6H2O = 2Al(OH)3 + 3H2↑ 2Аl + 3Cl2 = 2AlCl3 4Al + 3C = Al4C3 4Аl + 3O2 = 2Al2O3 t 2Al + 3S = Al2S3 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + WO3 = Al2O3 + W 6Al + 3CuCl2 = 2AlCl3 +3Cu
Cлайд 20
 Химические свойства Алюминий - очень активный металл. В реакциях он проявляет восстановительные свойства. Реагирует с простыми веществами – неметаллами. Восстанавливает металлы, стоящие в электрохимическом ряду напряжения справа от него. « Пассивность» алюминия связана с наличием оксидной пленки.
Химические свойства Алюминий - очень активный металл. В реакциях он проявляет восстановительные свойства. Реагирует с простыми веществами – неметаллами. Восстанавливает металлы, стоящие в электрохимическом ряду напряжения справа от него. « Пассивность» алюминия связана с наличием оксидной пленки.