X
Код презентации скопируйте его
«Азот»( урок-сказка)
Скачать эту презентациюПрезентация на тему «Азот»( урок-сказка)
Скачать эту презентациюCлайд 1
 Обобщение по теме: «Азот»( урок-сказка) Тайны царства Азота Новикова Ирина Валерьевна учитель химии МОУ Лицей № 57 Г. Тольятти
Обобщение по теме: «Азот»( урок-сказка) Тайны царства Азота Новикова Ирина Валерьевна учитель химии МОУ Лицей № 57 Г. Тольятти
Cлайд 2
 При помощи периодической системы Д.И. Менделеева дайте характеристику строению атома азота. Объясните многообразие кислородных соединений азота.
При помощи периодической системы Д.И. Менделеева дайте характеристику строению атома азота. Объясните многообразие кислородных соединений азота.
Cлайд 3
 Получение азота 1. Промышленный способ. Перегонка жидкого воздуха. 2. Лабораторный способ. Разложение нитрита аммония: NH4NO2 –t° N2 + 2H2O
Получение азота 1. Промышленный способ. Перегонка жидкого воздуха. 2. Лабораторный способ. Разложение нитрита аммония: NH4NO2 –t° N2 + 2H2O
Cлайд 4
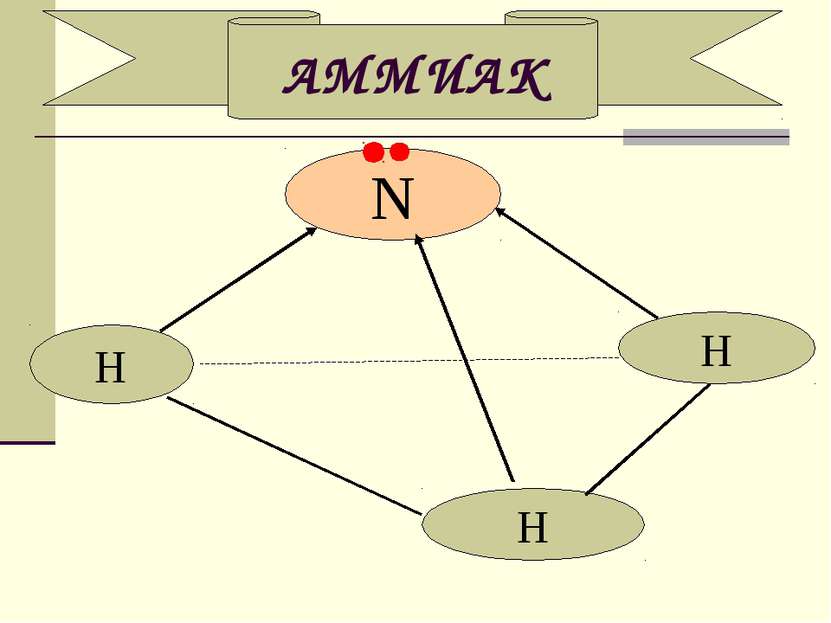
 Свойства азота Молекула азота (:NºN:) Очень устойчива (три ковалентные связи), поэтому обладает низкой реакционной способностью. Восстановитель N20 2N+2 Высокая температура (электрическая дуга, 3000°С) N20 + O20 2N+2O (в природе - во время грозы) Окислитель N20 2N-3 1. c водородом (500°С, kat, p) N20 + 3H20 2N-3HЗ 2. с активными металлами (с щелочными и щел.зем. металлами) 6Li + N20 2LiЗN-3 3Mg + N20 –t° MgЗ N2-3
Свойства азота Молекула азота (:NºN:) Очень устойчива (три ковалентные связи), поэтому обладает низкой реакционной способностью. Восстановитель N20 2N+2 Высокая температура (электрическая дуга, 3000°С) N20 + O20 2N+2O (в природе - во время грозы) Окислитель N20 2N-3 1. c водородом (500°С, kat, p) N20 + 3H20 2N-3HЗ 2. с активными металлами (с щелочными и щел.зем. металлами) 6Li + N20 2LiЗN-3 3Mg + N20 –t° MgЗ N2-3
Cлайд 6
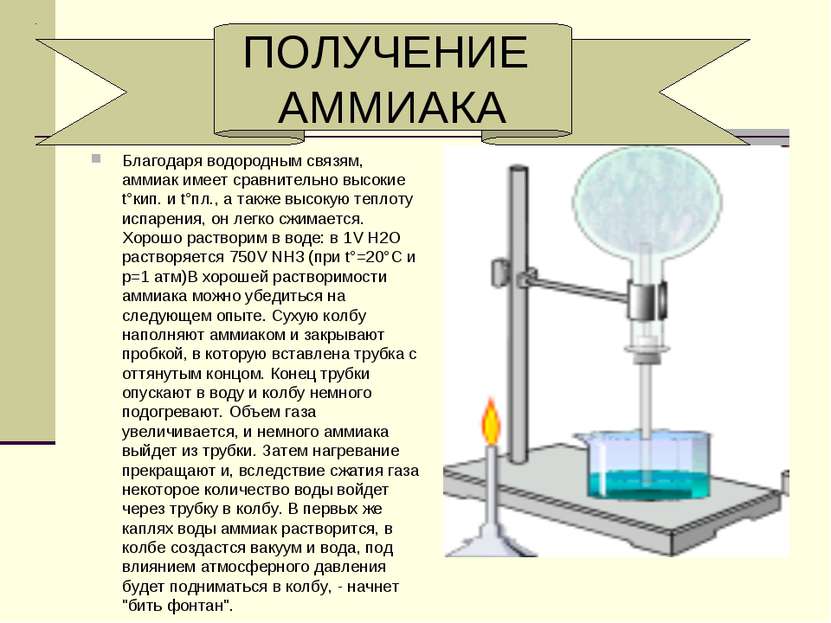
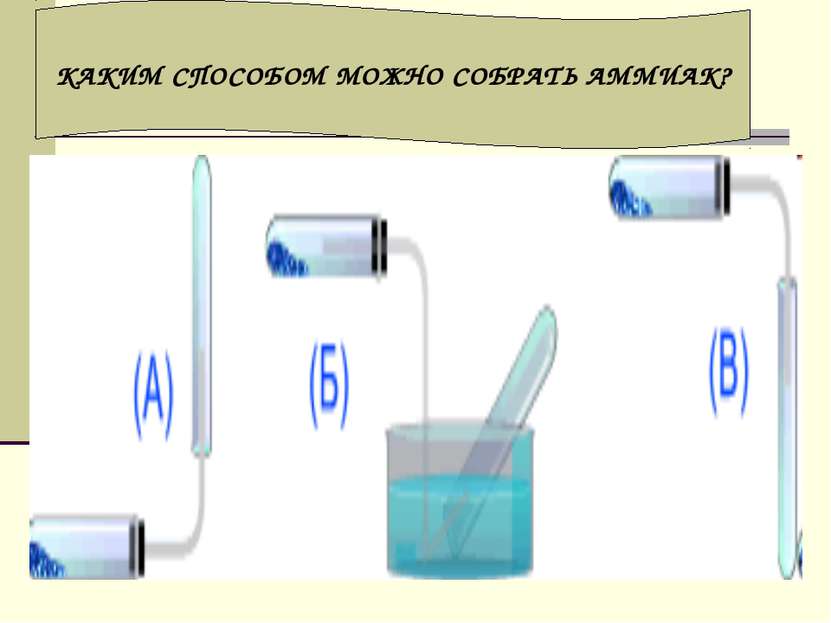
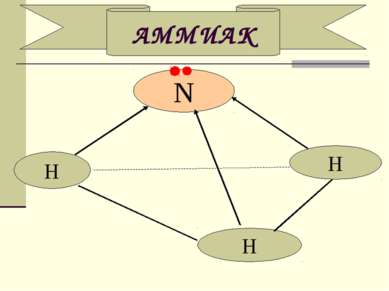
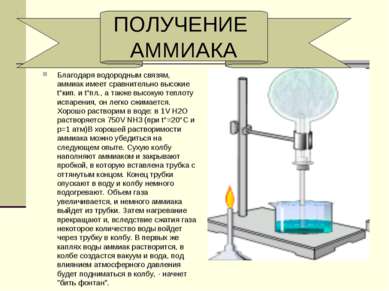 Благодаря водородным связям, аммиак имеет сравнительно высокие t°кип. и t°пл., а также высокую теплоту испарения, он легко сжимается. Хорошо растворим в воде: в 1V Н2O растворяется 750V NH3 (при t°=20°C и p=1 атм)В хорошей растворимости аммиака можно убедиться на следующем опыте. Сухую колбу наполняют аммиаком и закрывают пробкой, в которую вставлена трубка с оттянутым концом. Конец трубки опускают в воду и колбу немного подогревают. Объем газа увеличивается, и немного аммиака выйдет из трубки. Затем нагревание прекращают и, вследствие сжатия газа некоторое количество воды войдет через трубку в колбу. В первых же каплях воды аммиак растворится, в колбе создастся вакуум и вода, под влиянием атмосферного давления будет подниматься в колбу, - начнет "бить фонтан". ПОЛУЧЕНИЕ АММИАКА
Благодаря водородным связям, аммиак имеет сравнительно высокие t°кип. и t°пл., а также высокую теплоту испарения, он легко сжимается. Хорошо растворим в воде: в 1V Н2O растворяется 750V NH3 (при t°=20°C и p=1 атм)В хорошей растворимости аммиака можно убедиться на следующем опыте. Сухую колбу наполняют аммиаком и закрывают пробкой, в которую вставлена трубка с оттянутым концом. Конец трубки опускают в воду и колбу немного подогревают. Объем газа увеличивается, и немного аммиака выйдет из трубки. Затем нагревание прекращают и, вследствие сжатия газа некоторое количество воды войдет через трубку в колбу. В первых же каплях воды аммиак растворится, в колбе создастся вакуум и вода, под влиянием атмосферного давления будет подниматься в колбу, - начнет "бить фонтан". ПОЛУЧЕНИЕ АММИАКА
Cлайд 9
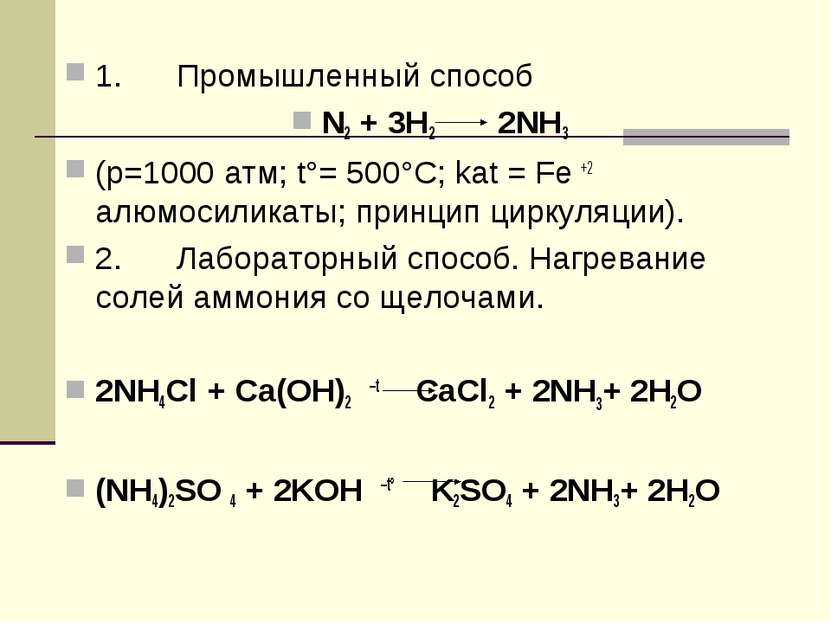
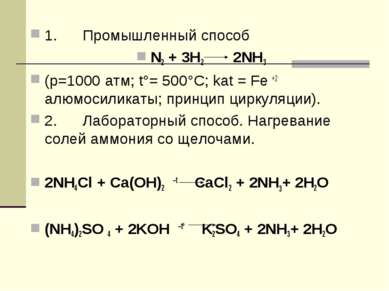 1. Промышленный способ N2 + 3H2 2NH3 (p=1000 атм; t°= 500°C; kat = Fe +2 алюмосиликаты; принцип циркуляции). 2. Лабораторный способ. Нагревание солей аммония со щелочами. 2NH4Cl + Ca(OH)2 –t CaCl2 + 2NH3+ 2Н2O (NH4)2SO 4 + 2KOH –t° K2SO4 + 2NH3+ 2Н2O
1. Промышленный способ N2 + 3H2 2NH3 (p=1000 атм; t°= 500°C; kat = Fe +2 алюмосиликаты; принцип циркуляции). 2. Лабораторный способ. Нагревание солей аммония со щелочами. 2NH4Cl + Ca(OH)2 –t CaCl2 + 2NH3+ 2Н2O (NH4)2SO 4 + 2KOH –t° K2SO4 + 2NH3+ 2Н2O
Cлайд 11
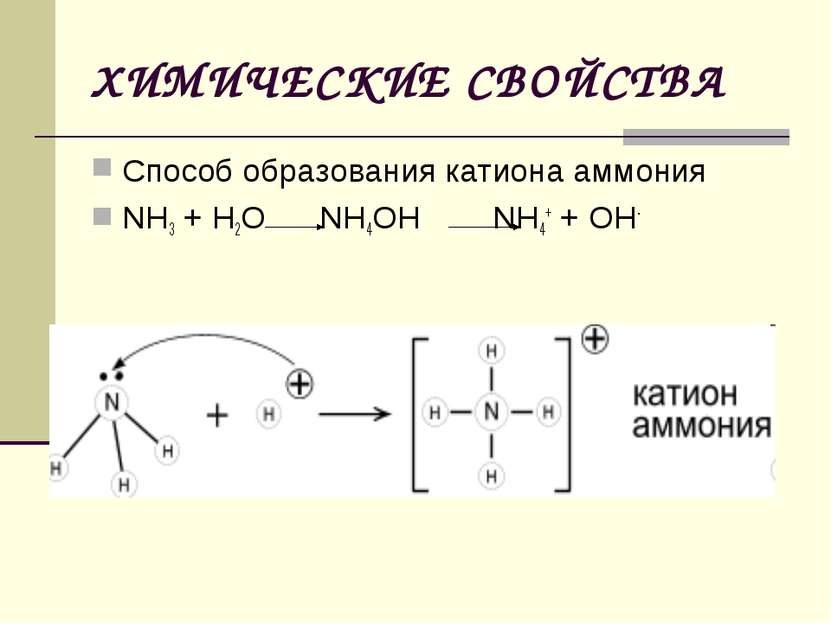
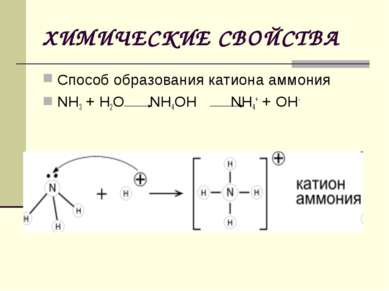
 1. Разложение при нагревании 2N-3H3 t° N20 + 3H2 2. Горение в кислороде a) без катализатора 4N-3H3 + 3O2 2N20 + 6Н2O b) каталитическое окисление ( kat = Pt ) 4N-3H3 + 5O2 4N+2O + 6Н2O 3. Восстановление оксидов некоторых металлов 3Cu+2O + 2N-3H3 3Cu + N2 + 3Н2O Аммиак - восстановитель (окисляется до N2+1O или N+2O)
1. Разложение при нагревании 2N-3H3 t° N20 + 3H2 2. Горение в кислороде a) без катализатора 4N-3H3 + 3O2 2N20 + 6Н2O b) каталитическое окисление ( kat = Pt ) 4N-3H3 + 5O2 4N+2O + 6Н2O 3. Восстановление оксидов некоторых металлов 3Cu+2O + 2N-3H3 3Cu + N2 + 3Н2O Аммиак - восстановитель (окисляется до N2+1O или N+2O)
Cлайд 12
 Кислородсодержащие соединения азота N2O ОКСИД АЗОТА (I) ЗАКИСЬ АЗОТА, "ВЕСЕЛЯЩИЙ ГАЗ» NO ОКСИД АЗОТА (II) ОКИСЬ АЗОТА N2O3 ОКСИД АЗОТА (III) АЗОТИСТЫЙ АНГИДРИД NO2 ОКСИД АЗОТА (IV) ДВУОКИСЬ АЗОТА, ДИОКСИД АЗОТА N2O5 ОКСИД АЗОТА (V) АЗОТНЫЙ АНГИДРИД Определите степень окисления атома азота в оксидах
Кислородсодержащие соединения азота N2O ОКСИД АЗОТА (I) ЗАКИСЬ АЗОТА, "ВЕСЕЛЯЩИЙ ГАЗ» NO ОКСИД АЗОТА (II) ОКИСЬ АЗОТА N2O3 ОКСИД АЗОТА (III) АЗОТИСТЫЙ АНГИДРИД NO2 ОКСИД АЗОТА (IV) ДВУОКИСЬ АЗОТА, ДИОКСИД АЗОТА N2O5 ОКСИД АЗОТА (V) АЗОТНЫЙ АНГИДРИД Определите степень окисления атома азота в оксидах
Cлайд 13
 Какой оксид при комнатной температуре легко окисляется? Напишите уравнение реакции Какой оксид при взаимодействии с водой одновременно образует две кислоты? Напишите уравнение реакции
Какой оксид при комнатной температуре легко окисляется? Напишите уравнение реакции Какой оксид при взаимодействии с водой одновременно образует две кислоты? Напишите уравнение реакции
Cлайд 14
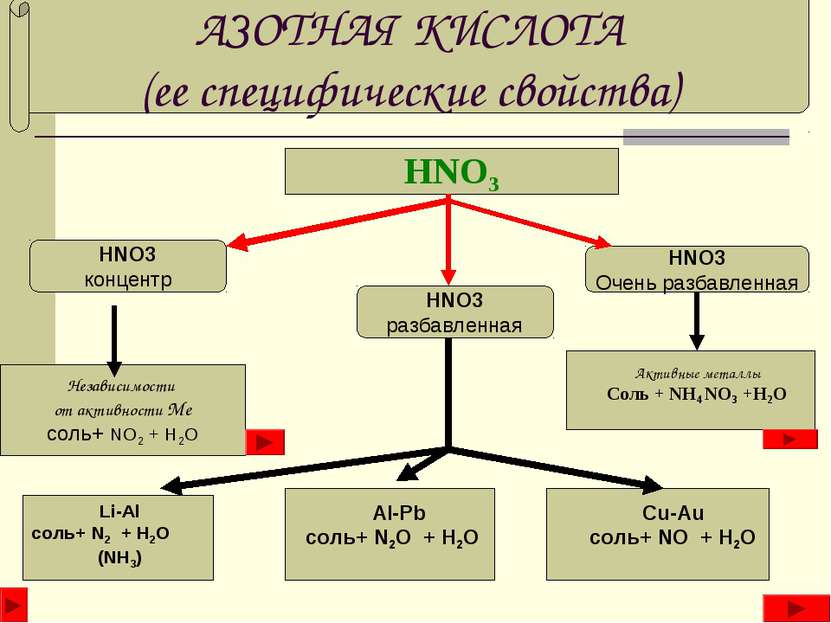
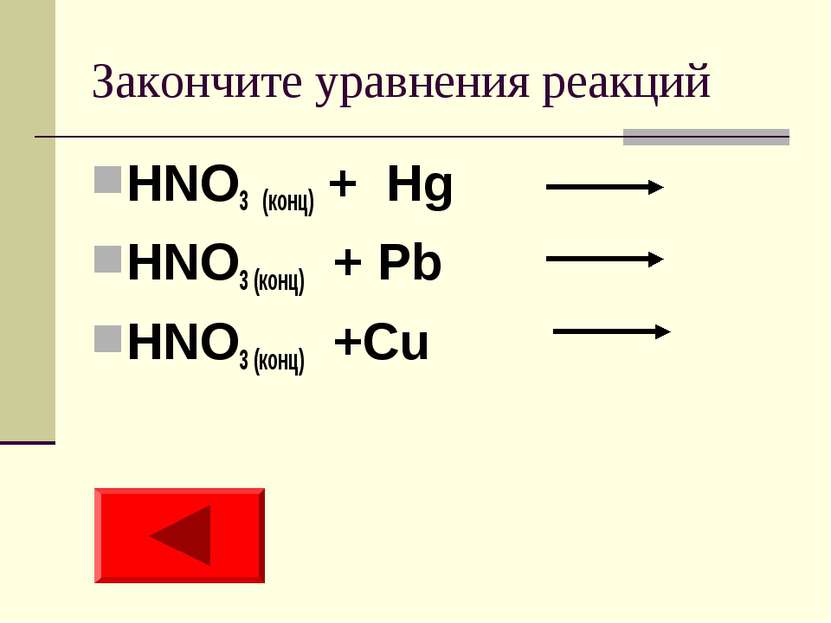
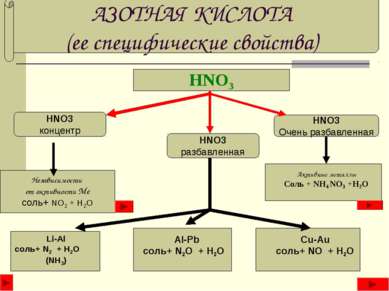 АЗОТНАЯ КИСЛОТА (ее специфические свойства) HNO3 HNO3 концентр HNO3 разбавленная HNO3 Очень разбавленная Независимости от активности Ме соль+ NO2 + H2O Li-Al соль+ N2 + H2O (NH3) Al-Pb соль+ N2O + H2O Cu-Au соль+ NO + H2O Активные металлы Соль + NH4 NO3 +H2O
АЗОТНАЯ КИСЛОТА (ее специфические свойства) HNO3 HNO3 концентр HNO3 разбавленная HNO3 Очень разбавленная Независимости от активности Ме соль+ NO2 + H2O Li-Al соль+ N2 + H2O (NH3) Al-Pb соль+ N2O + H2O Cu-Au соль+ NO + H2O Активные металлы Соль + NH4 NO3 +H2O
Cлайд 17
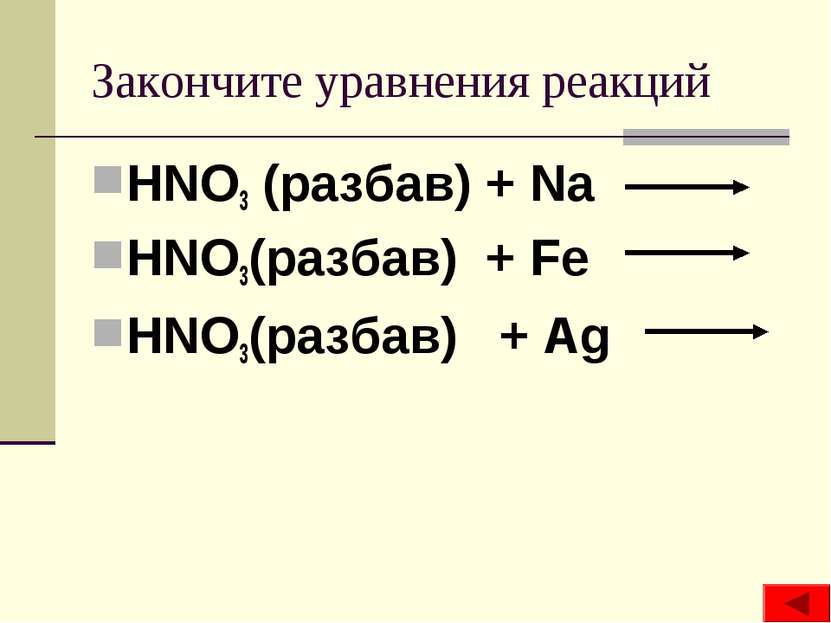
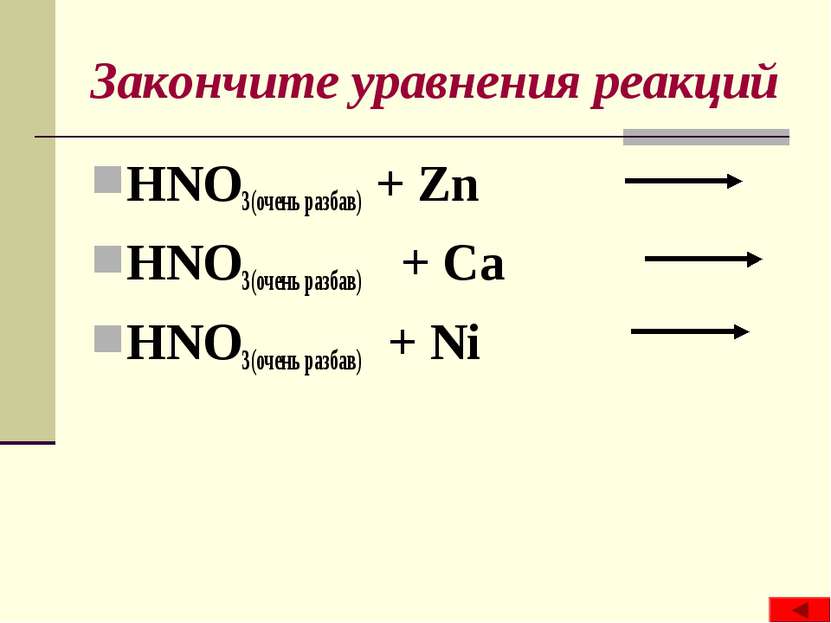
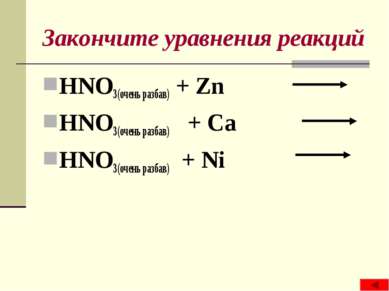 Закончите уравнения реакций HNO3(очень разбав) + Zn HNO3(очень разбав) + Ca HNO3(очень разбав) + Ni
Закончите уравнения реакций HNO3(очень разбав) + Zn HNO3(очень разбав) + Ca HNO3(очень разбав) + Ni
Cлайд 18
 1.Какие металлы не взаимодействуют с холодной концентрированной азотной кислотой? 2. Закончите уравнения реакции Au + HNO3 + HCl
1.Какие металлы не взаимодействуют с холодной концентрированной азотной кислотой? 2. Закончите уравнения реакции Au + HNO3 + HCl
Cлайд 19
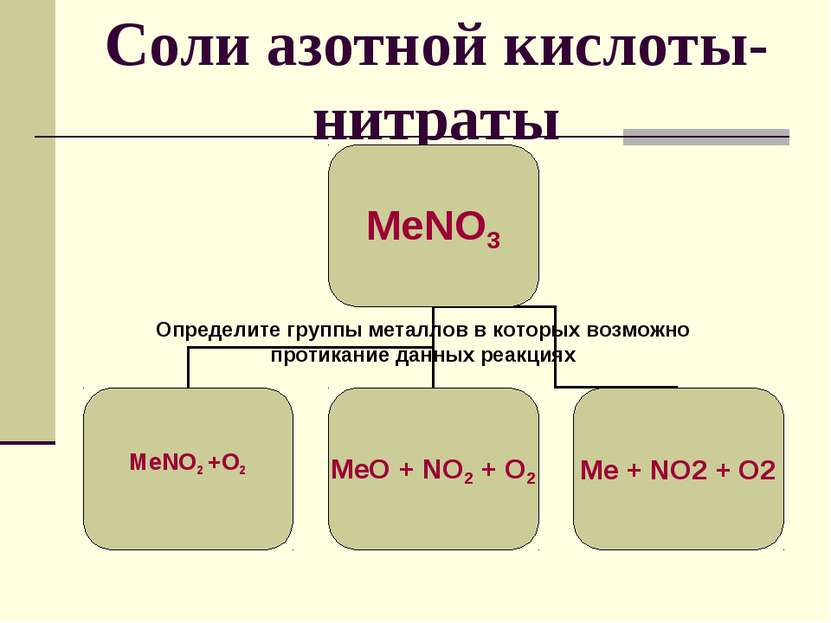
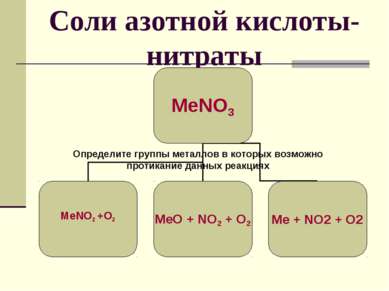 Соли азотной кислоты- нитраты Определите группы металлов в которых возможно протикание данных реакциях МеNO2 +O2
Соли азотной кислоты- нитраты Определите группы металлов в которых возможно протикание данных реакциях МеNO2 +O2