X
Код презентации скопируйте его
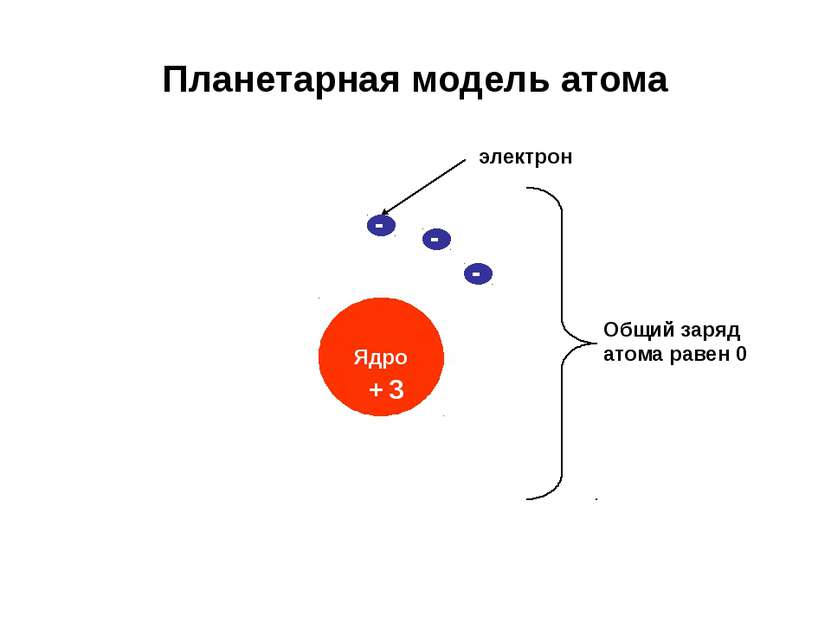
Строение атома
Скачать эту презентациюПрезентация на тему Строение атома
Скачать эту презентациюCлайд 1
 Строение атома Автор презентации: учитель МОУ СОШ пгт. Новокручининский Забайкальского края Журова О. В.
Строение атома Автор презентации: учитель МОУ СОШ пгт. Новокручининский Забайкальского края Журова О. В.
Cлайд 4
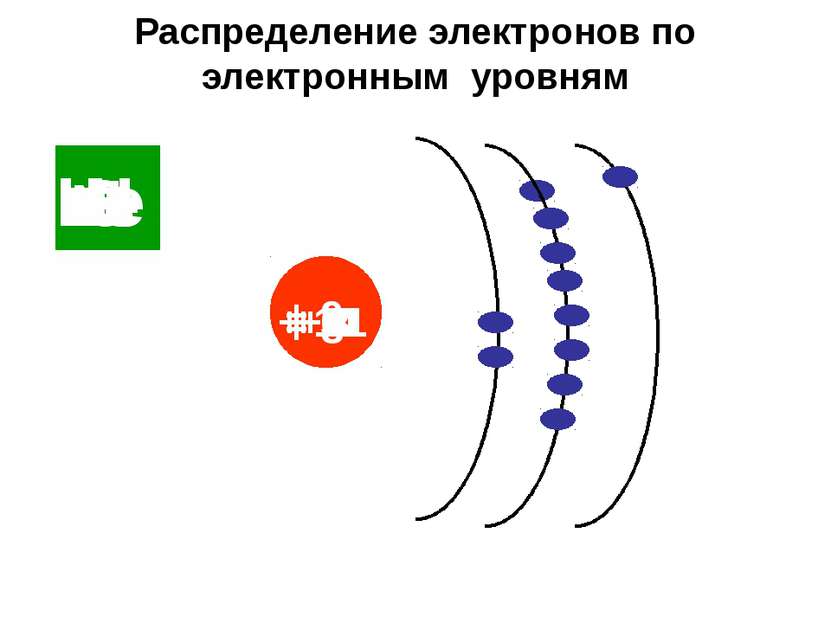
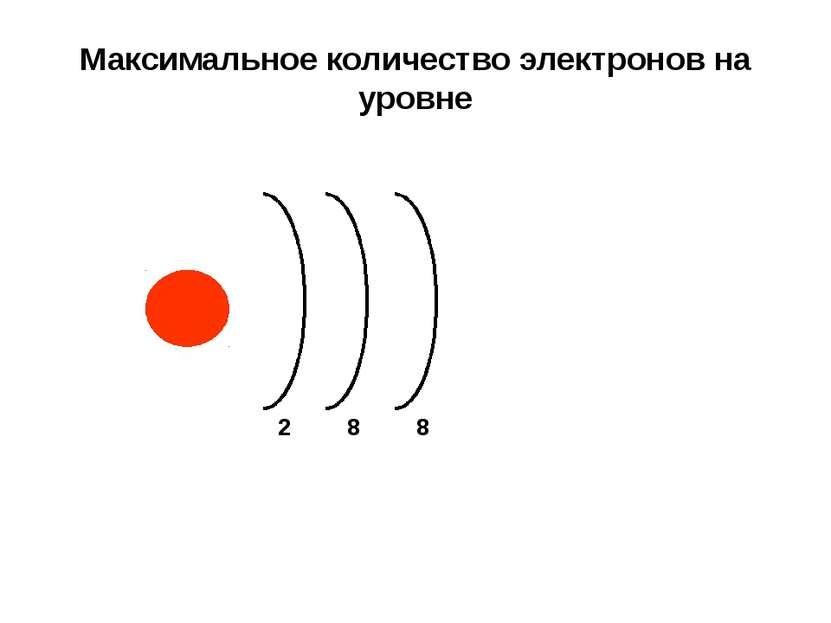
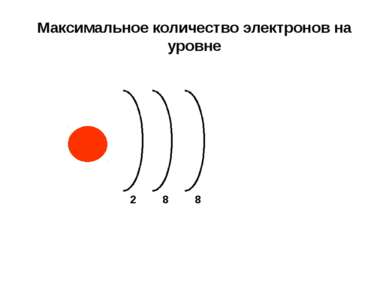
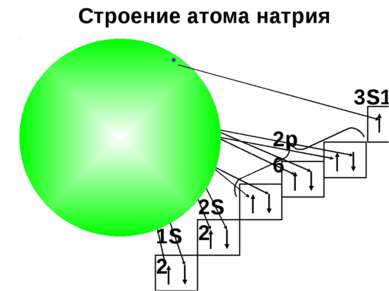
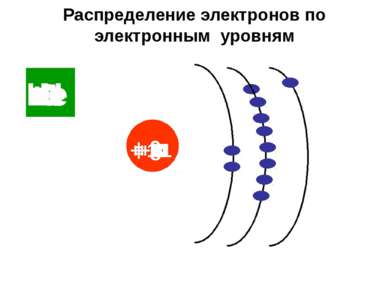 Распределение электронов по электронным уровням Н + 1 Не + 2 Li + 3 + 4 Be B + 5 C + 6 N + 7 O + 8 F + 9 Ne + 10 Na + 11
Распределение электронов по электронным уровням Н + 1 Не + 2 Li + 3 + 4 Be B + 5 C + 6 N + 7 O + 8 F + 9 Ne + 10 Na + 11
Cлайд 6
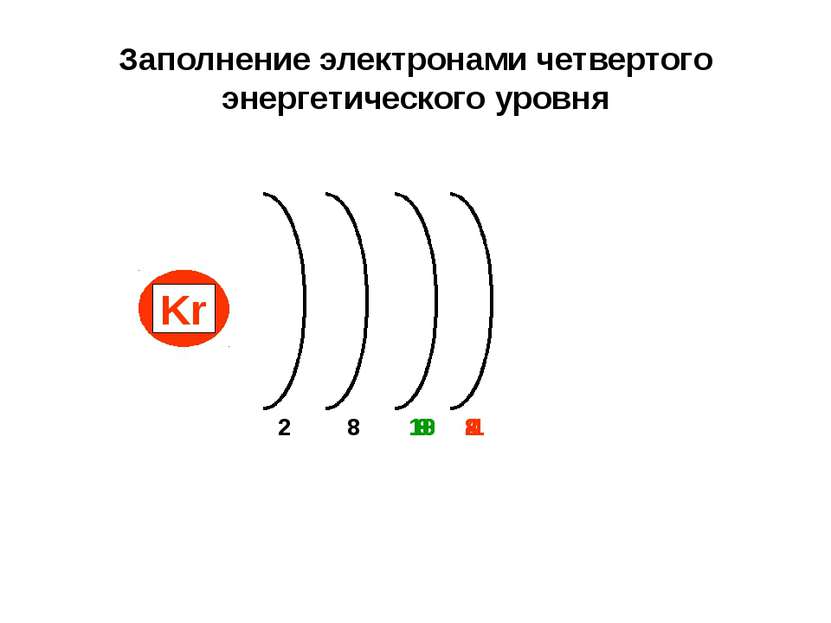
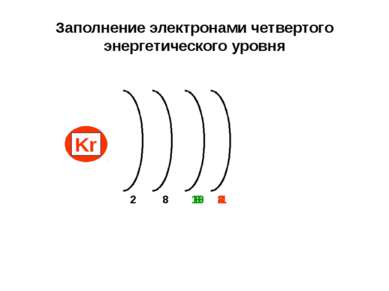 Заполнение электронами четвертого энергетического уровня 8 1 K Ca Sc Ti 2 9 10 Zn 18 Ga 3 Ge 4 Kr 8 2 8
Заполнение электронами четвертого энергетического уровня 8 1 K Ca Sc Ti 2 9 10 Zn 18 Ga 3 Ge 4 Kr 8 2 8
Cлайд 7
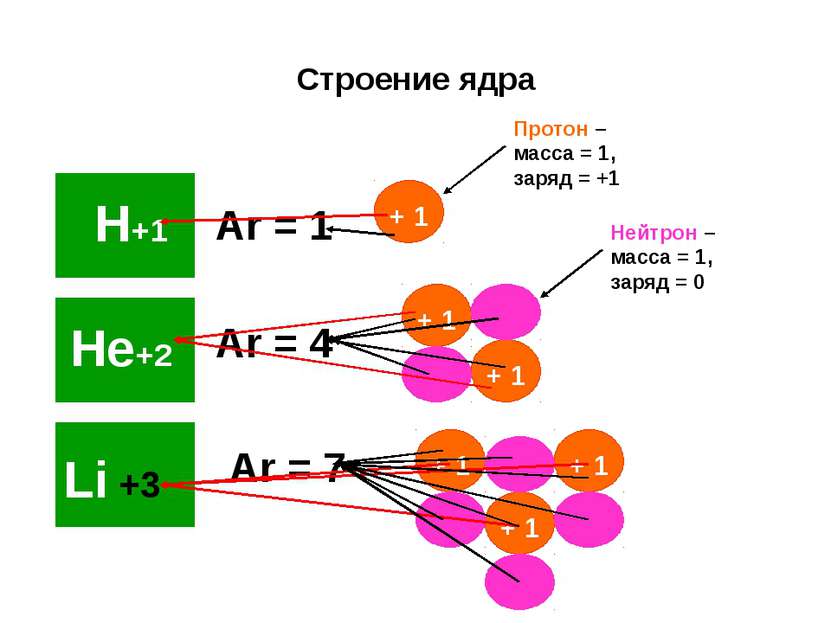
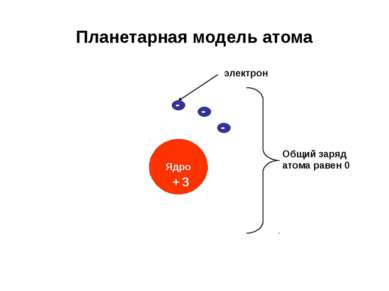
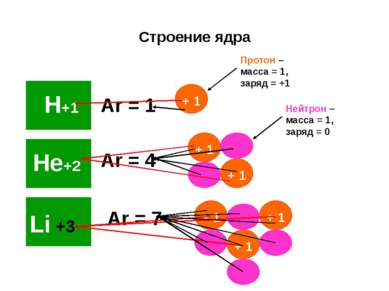 Строение ядра Аr = 1 Аr = 4 Аr = 7 Протон – масса = 1, заряд = +1 Нейтрон – масса = 1, заряд = 0 +3 Н+1 + 1 Не+2 Li
Строение ядра Аr = 1 Аr = 4 Аr = 7 Протон – масса = 1, заряд = +1 Нейтрон – масса = 1, заряд = 0 +3 Н+1 + 1 Не+2 Li
Cлайд 8
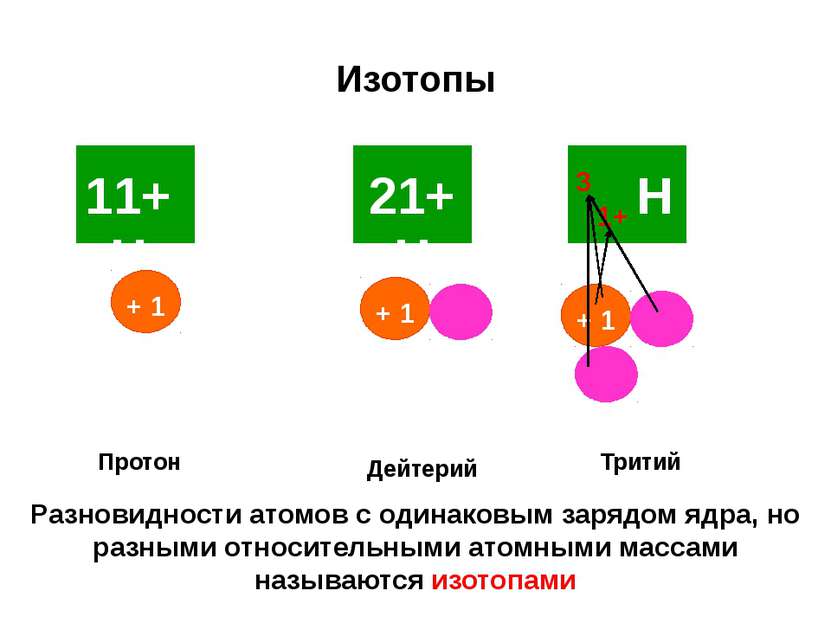
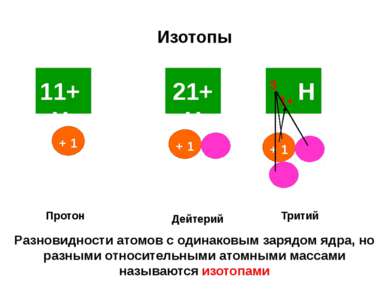 Изотопы Протон Дейтерий Тритий 1+ 3 Разновидности атомов с одинаковым зарядом ядра, но разными относительными атомными массами называются изотопами 11+ Н + 1 21+ Н Н
Изотопы Протон Дейтерий Тритий 1+ 3 Разновидности атомов с одинаковым зарядом ядра, но разными относительными атомными массами называются изотопами 11+ Н + 1 21+ Н Н
Cлайд 10
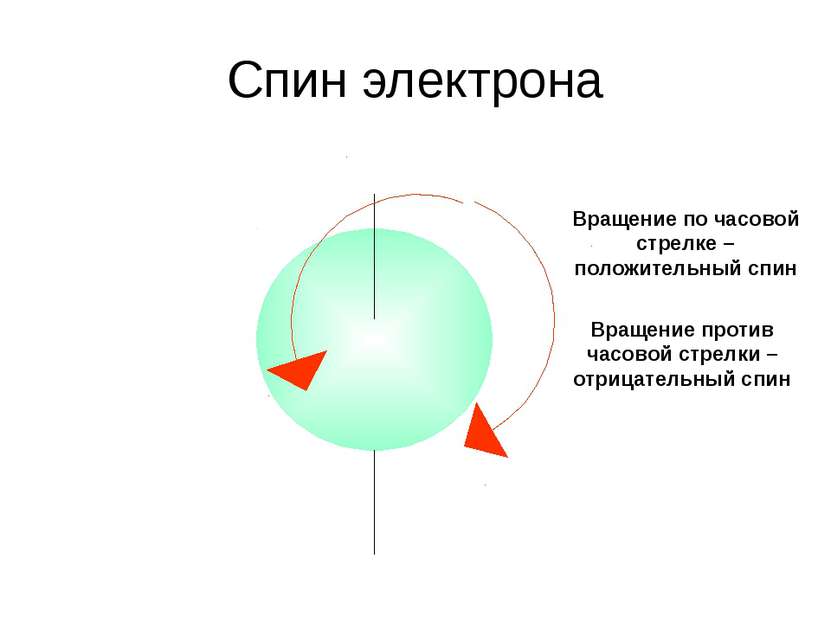
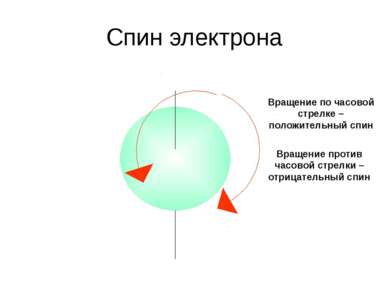 Спин электрона Вращение по часовой стрелке – положительный спин Вращение против часовой стрелки – отрицательный спин
Спин электрона Вращение по часовой стрелке – положительный спин Вращение против часовой стрелки – отрицательный спин
Cлайд 11
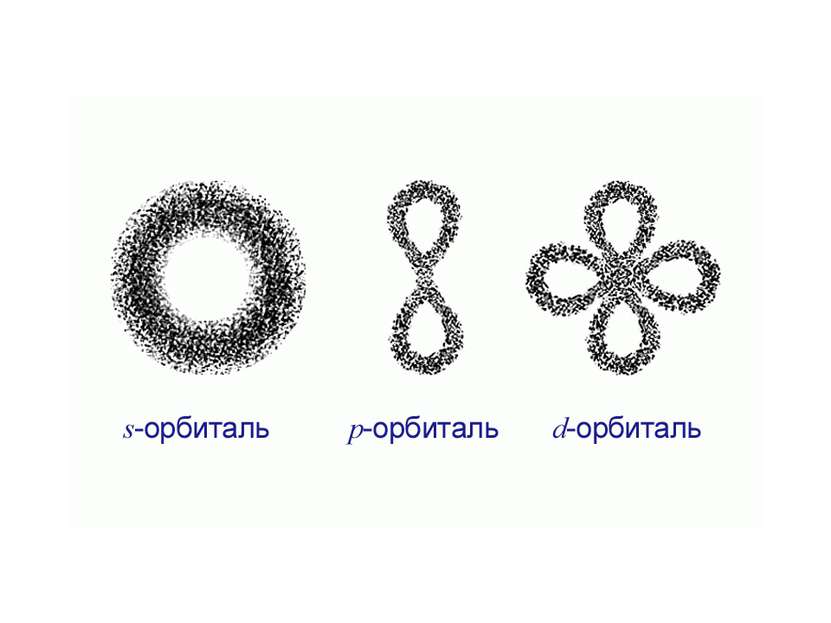
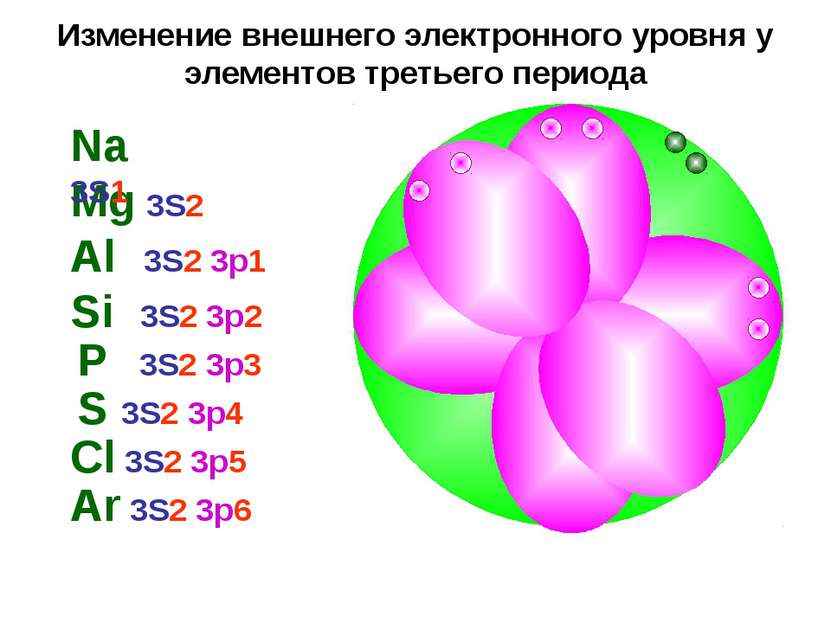
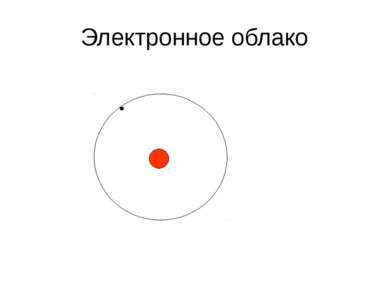
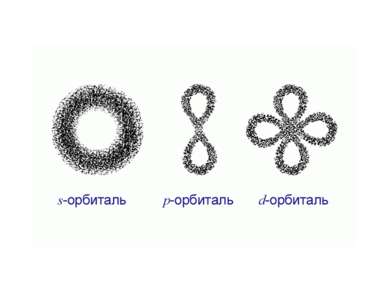
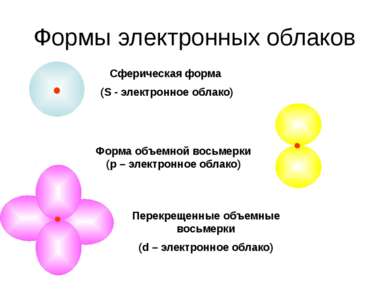 Формы электронных облаков Сферическая форма (S - электронное облако) Форма объемной восьмерки (p – электронное облако) Перекрещенные объемные восьмерки (d – электронное облако)
Формы электронных облаков Сферическая форма (S - электронное облако) Форма объемной восьмерки (p – электронное облако) Перекрещенные объемные восьмерки (d – электронное облако)
Cлайд 13
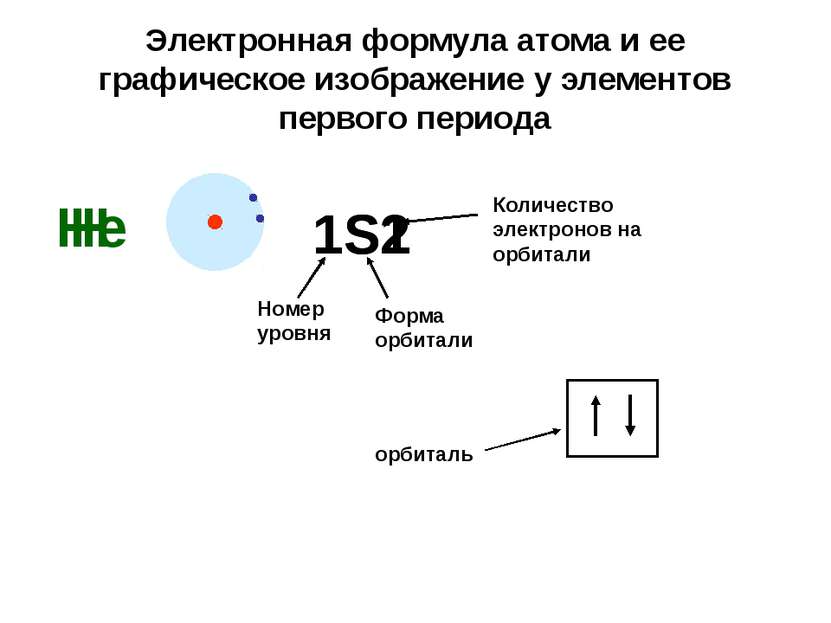
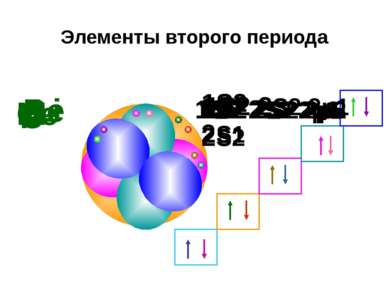
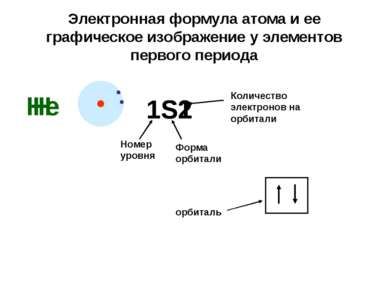 Электронная формула атома и ее графическое изображение у элементов первого периода Н 1S1 Номер уровня Форма орбитали Количество электронов на орбитали Не 1S2 орбиталь
Электронная формула атома и ее графическое изображение у элементов первого периода Н 1S1 Номер уровня Форма орбитали Количество электронов на орбитали Не 1S2 орбиталь