X
Код презентации скопируйте его
Фосфор как элемент и вещество
Скачать эту презентациюПрезентация на тему Фосфор как элемент и вещество
Скачать эту презентациюCлайд 1
 Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородская область «Фосфор как элемент и вещество» урок химии 9 класс
Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородская область «Фосфор как элемент и вещество» урок химии 9 класс
Cлайд 2
 Цели урока: организовать деятельность учащихся по изучению особенностей строения атома фосфора на основании его положения в ПСХЭ Д.Менделеева выяснить аллотропные возможности фосфора изучить химические свойства фосфора как простого вещества на основе его строения развивать познавательную самостоятельность учащихся при работе с учебником, дополнительной литературой, сайтами Интернета формировать умения составления химических уравнений на основе химического эксперимента, навыки решения расчетных задач воспитывать ответственность за конечный результат работы.
Цели урока: организовать деятельность учащихся по изучению особенностей строения атома фосфора на основании его положения в ПСХЭ Д.Менделеева выяснить аллотропные возможности фосфора изучить химические свойства фосфора как простого вещества на основе его строения развивать познавательную самостоятельность учащихся при работе с учебником, дополнительной литературой, сайтами Интернета формировать умения составления химических уравнений на основе химического эксперимента, навыки решения расчетных задач воспитывать ответственность за конечный результат работы.
Cлайд 3
 Мотивационно-ориентационный этап. Академик А.Е.Ферсман назвал этот элемент « элементом мысли и жизни», без него невозможно существование на Земле живого, в теле человека его примерно 0,8 кг. Он - основа нервных, мышечных, мозговых и костных тканей. Является жителем V-A подгруппы периодической системы химических элементов Д.И.Менделеева. О каком элементе идет речь?
Мотивационно-ориентационный этап. Академик А.Е.Ферсман назвал этот элемент « элементом мысли и жизни», без него невозможно существование на Земле живого, в теле человека его примерно 0,8 кг. Он - основа нервных, мышечных, мозговых и костных тканей. Является жителем V-A подгруппы периодической системы химических элементов Д.И.Менделеева. О каком элементе идет речь?
Cлайд 5
 История открытия фосфора 1669 г- Х.Бранд-первооткрыватель фосфора 1682г- Р.Бойль в химической лаборатории при работе с фосфором.
История открытия фосфора 1669 г- Х.Бранд-первооткрыватель фосфора 1682г- Р.Бойль в химической лаборатории при работе с фосфором.
Cлайд 8
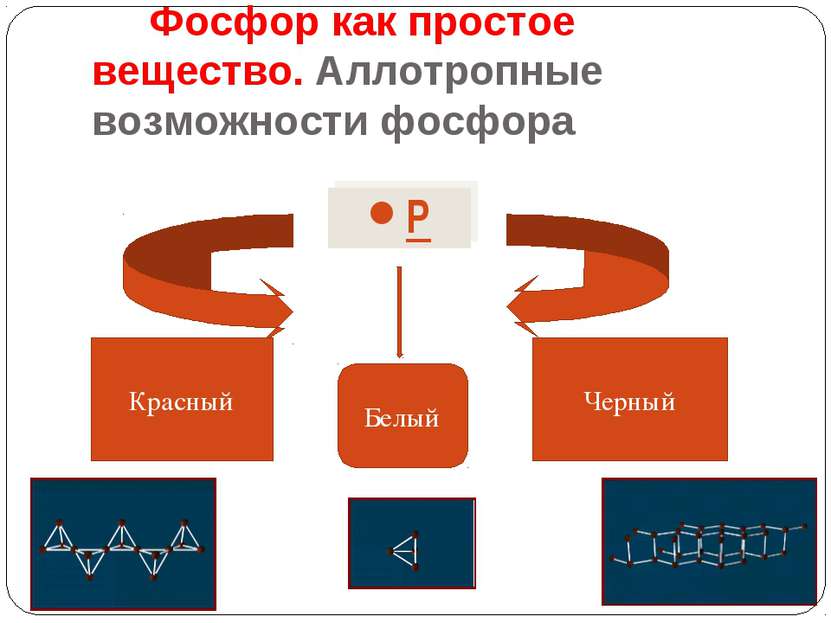
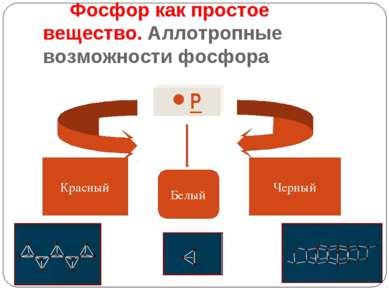
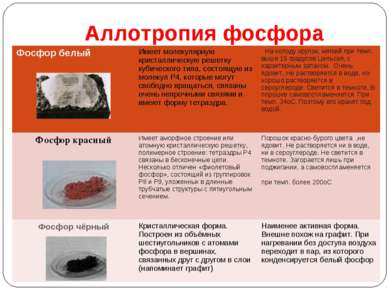 Аллотропия фосфора Фосфор белый Имеет молекулярную кристаллическую решетку кубического типа, состоящую из молекул Р4, которые могут свободно вращаться, связаны очень непрочными связями и имеют форму тетраэдра. На холоду хрупок, мягкий при темп. выше 15 градусов Цельсия, с характерным запахом. Очень ядовит. Не растворяется в воде, но хорошо растворяется в сероуглероде. Светится в темноте. В порошке самовоспламеняется. При темп. 34оС. Поэтому его хранят под водой. Фосфор красный Имеет аморфное строение или атомную кристаллическую решетку, полимерное строение: тетраэдры Р4 связаны в бесконечные цепи. Несколько отличен «фиолетовый фосфор», состоящий из группировок Р8 и Р9, уложенных в длинные трубчатые структуры с пятиугольным сечением. Порошок красно-бурого цвета ,не ядовит. Не растворяется ни в воде, ни в сероуглероде. Не светится в темноте. Загорается лишь при поджигании, а самовоспламеняется при темп. более 200оС Фосфор чёрный Кристаллическая форма. Построен из объёмных шестиугольников с атомами фосфора в вершинах, связанных друг с другом в слои (напоминает графит) Наименее активная форма. Внешне похож на графит. При нагревании без доступа воздуха переходит в пар, из которого конденсируется белый фосфор
Аллотропия фосфора Фосфор белый Имеет молекулярную кристаллическую решетку кубического типа, состоящую из молекул Р4, которые могут свободно вращаться, связаны очень непрочными связями и имеют форму тетраэдра. На холоду хрупок, мягкий при темп. выше 15 градусов Цельсия, с характерным запахом. Очень ядовит. Не растворяется в воде, но хорошо растворяется в сероуглероде. Светится в темноте. В порошке самовоспламеняется. При темп. 34оС. Поэтому его хранят под водой. Фосфор красный Имеет аморфное строение или атомную кристаллическую решетку, полимерное строение: тетраэдры Р4 связаны в бесконечные цепи. Несколько отличен «фиолетовый фосфор», состоящий из группировок Р8 и Р9, уложенных в длинные трубчатые структуры с пятиугольным сечением. Порошок красно-бурого цвета ,не ядовит. Не растворяется ни в воде, ни в сероуглероде. Не светится в темноте. Загорается лишь при поджигании, а самовоспламеняется при темп. более 200оС Фосфор чёрный Кристаллическая форма. Построен из объёмных шестиугольников с атомами фосфора в вершинах, связанных друг с другом в слои (напоминает графит) Наименее активная форма. Внешне похож на графит. При нагревании без доступа воздуха переходит в пар, из которого конденсируется белый фосфор
Cлайд 9
 Прокомментируйте отрывок из романа А.Конан-Дойля « Собака Баскервилей». Попытайте определить, где правда, а где вымысел автора? «...Да! Это была собака, огромная, черная, как смоль. Но такой собаки еще никто из нас, смертных, не видывал. Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь .Ее огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте. - Фосфор, – сказал я».
Прокомментируйте отрывок из романа А.Конан-Дойля « Собака Баскервилей». Попытайте определить, где правда, а где вымысел автора? «...Да! Это была собака, огромная, черная, как смоль. Но такой собаки еще никто из нас, смертных, не видывал. Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь .Ее огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте. - Фосфор, – сказал я».
Cлайд 10
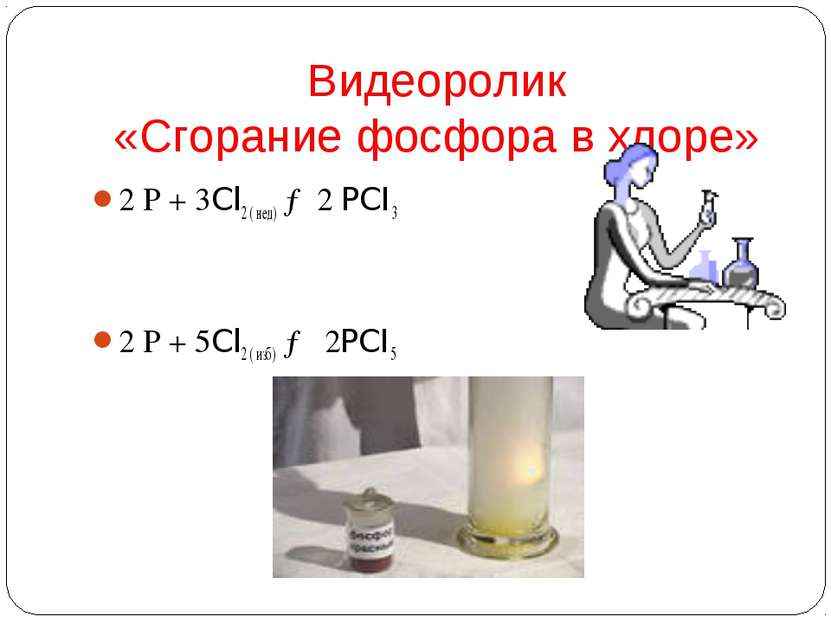
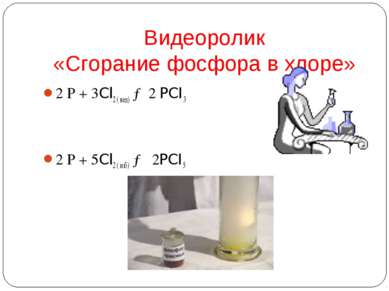
 Химические свойства фосфора. ( Работа с учебником стр.160 и дополнительной литературой) Фосфор как окислитель Фосфор как восстановитель 2P0 + 3Mg Mg3P2-3 3Li + P Li3P-3 4P + 3NaOH + 3H2O PH3 + 3NaH2PO2 4P0 + 5O2 –t 2P2+5O5 2P + 3Cl2 2PCl3 2P + 5Cl2 2PCl5 2P + 5S –t P2S5 3P0 + 5HN+5O3 + 2H2O 3H3P+5O4 + 5N+2O
Химические свойства фосфора. ( Работа с учебником стр.160 и дополнительной литературой) Фосфор как окислитель Фосфор как восстановитель 2P0 + 3Mg Mg3P2-3 3Li + P Li3P-3 4P + 3NaOH + 3H2O PH3 + 3NaH2PO2 4P0 + 5O2 –t 2P2+5O5 2P + 3Cl2 2PCl3 2P + 5Cl2 2PCl5 2P + 5S –t P2S5 3P0 + 5HN+5O3 + 2H2O 3H3P+5O4 + 5N+2O
Cлайд 14
 Первичное закрепление полученных знаний. Учащиеся выбирают для закрепления материала задания разных уровней сложности: 1 уровень: упр. №1 стр. 163 учебника ( О.С.Габриелян, «Химия-9») 2 уровень:упр.№2 стр. 163 учебника 3 уровень: решение расчетной задачи №5 стр.163 учебника.
Первичное закрепление полученных знаний. Учащиеся выбирают для закрепления материала задания разных уровней сложности: 1 уровень: упр. №1 стр. 163 учебника ( О.С.Габриелян, «Химия-9») 2 уровень:упр.№2 стр. 163 учебника 3 уровень: решение расчетной задачи №5 стр.163 учебника.
Cлайд 15
 Домашнее задание: п.28 ( до стр.160- соединения фосфора), упр.№3,6 ( по выбору учащихся); творческое задание: презентация темы « Биологическое значение фосфора».
Домашнее задание: п.28 ( до стр.160- соединения фосфора), упр.№3,6 ( по выбору учащихся); творческое задание: презентация темы « Биологическое значение фосфора».
Cлайд 16
 Итоги урока. Рефлексивно- оценочный этап. Рефлексия « Телеграмма» ученика учителю о впечатлениях об уроке.
Итоги урока. Рефлексивно- оценочный этап. Рефлексия « Телеграмма» ученика учителю о впечатлениях об уроке.
Cлайд 18
 СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ Учебник О.С.Габриеляна « Химия- 9», изд.» Дрофа», 2007 год. Виртуальная лаборатория. Открытая химия. 8-11 класс. [Электронный носитель]. – М.: Габриелян О.С. Настольная книга учителя. Химия. 9 класс. – М.: Дрофа, 2002. Уроки химии Кирилла и Мефодия. 8-9 класс. [Электронный носитель]. – М.: «Кирилл и Мефодий», 2002. http://www.alhimik.ru http://him.1september.ru.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ Учебник О.С.Габриеляна « Химия- 9», изд.» Дрофа», 2007 год. Виртуальная лаборатория. Открытая химия. 8-11 класс. [Электронный носитель]. – М.: Габриелян О.С. Настольная книга учителя. Химия. 9 класс. – М.: Дрофа, 2002. Уроки химии Кирилла и Мефодия. 8-9 класс. [Электронный носитель]. – М.: «Кирилл и Мефодий», 2002. http://www.alhimik.ru http://him.1september.ru.