X
Код презентации скопируйте его
Свойства воды
Скачать эту презентациюПрезентация на тему Свойства воды
Скачать эту презентациюCлайд 2
 2. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ: ЖИДКОСТЬ - БЕЗ ЦВЕТА, ВКУСА И ЗАПАХА СУЩЕСТВУЕТ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ КИПИТ ПРИ 100°С ЗАМЕРЗАЕТ (ПЛАВИТСЯ) ПРИ 0°С ПЛОТНОСТЬ 1 Г/МЛ ОБЛАДАЕТ САМОЙ БОЛЬШОЙ ТЕПЛОЁМКОСТЬЮ НЕ ПРОВОДИТ ЭЛЕКТРИЧЕСКИЙ ТОК ПЛОТНОСТЬ ЛЬДА МЕНЬШЕ ПЛОТНОСТИ ВОДЫ УНИВЕРСАЛЬНЫЙ РАСТВОРИТЕЛЬ
2. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ: ЖИДКОСТЬ - БЕЗ ЦВЕТА, ВКУСА И ЗАПАХА СУЩЕСТВУЕТ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ КИПИТ ПРИ 100°С ЗАМЕРЗАЕТ (ПЛАВИТСЯ) ПРИ 0°С ПЛОТНОСТЬ 1 Г/МЛ ОБЛАДАЕТ САМОЙ БОЛЬШОЙ ТЕПЛОЁМКОСТЬЮ НЕ ПРОВОДИТ ЭЛЕКТРИЧЕСКИЙ ТОК ПЛОТНОСТЬ ЛЬДА МЕНЬШЕ ПЛОТНОСТИ ВОДЫ УНИВЕРСАЛЬНЫЙ РАСТВОРИТЕЛЬ
Cлайд 4
 3. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ 1. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ: а) очень активные металлы при взаимодействии с водой образуют гидроксид металла и водород: 2Na + 2H2O = 2NaOH + H2 гидроксид натрия 2K + 2H2O = 2KOH + H2 гидроксид калия Ca + 2H2O = Ca(OH)2 + H2 гидроксид кальция
3. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ 1. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ: а) очень активные металлы при взаимодействии с водой образуют гидроксид металла и водород: 2Na + 2H2O = 2NaOH + H2 гидроксид натрия 2K + 2H2O = 2KOH + H2 гидроксид калия Ca + 2H2O = Ca(OH)2 + H2 гидроксид кальция
Cлайд 5
 б) металлы средней активности взаимодействуют с водой при нагревании, образуя оксид металла и водород: Zn + H2O = ZnO + H2 оксид цинка 3Fe + 4H2O = Fe3O4 + 4H2 железная окалина в) малоактивные металлы с водой не реагируют: Cu + H2O =
б) металлы средней активности взаимодействуют с водой при нагревании, образуя оксид металла и водород: Zn + H2O = ZnO + H2 оксид цинка 3Fe + 4H2O = Fe3O4 + 4H2 железная окалина в) малоактивные металлы с водой не реагируют: Cu + H2O =
Cлайд 6
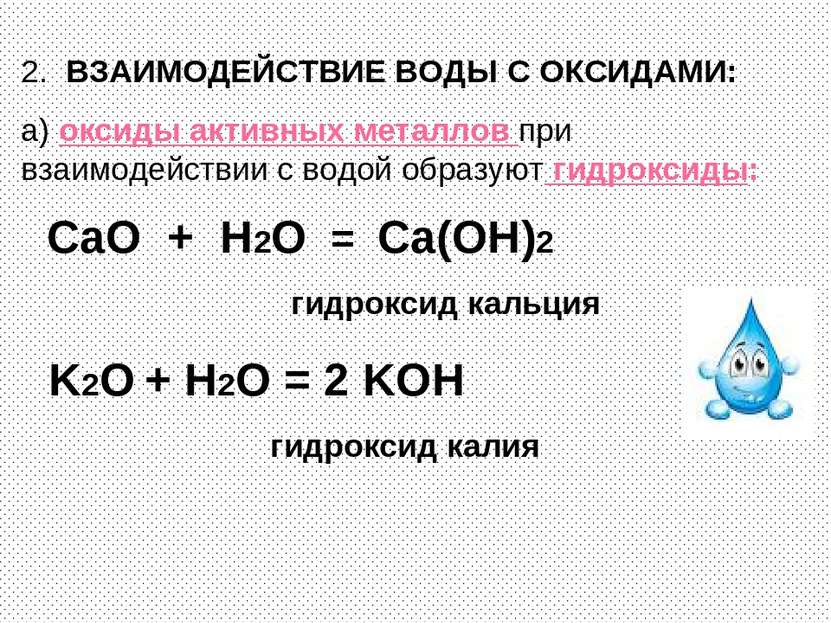
 2. ВЗАИМОДЕЙСТВИЕ ВОДЫ С ОКСИДАМИ: а) оксиды активных металлов при взаимодействии с водой образуют гидроксиды: CaO + H2O = Ca(OH)2 гидроксид кальция K2O + H2O = 2 KOH гидроксид калия
2. ВЗАИМОДЕЙСТВИЕ ВОДЫ С ОКСИДАМИ: а) оксиды активных металлов при взаимодействии с водой образуют гидроксиды: CaO + H2O = Ca(OH)2 гидроксид кальция K2O + H2O = 2 KOH гидроксид калия
Cлайд 8
 б) оксиды неметаллов при взаимодействии с водой образуют кислоты: SO2 + H2O = H2SO3 cернистая кислота SO3 + H2O = H2SO4 серная кислота
б) оксиды неметаллов при взаимодействии с водой образуют кислоты: SO2 + H2O = H2SO3 cернистая кислота SO3 + H2O = H2SO4 серная кислота
Cлайд 10
 Определите ряд веществ, которые взаимодействуют с водой. Составьте уравнения реакций 1.А) Na2O Ca CO2 Б) SO3 Al2O3 Cu В) Au CaO K A) SO2 CuO Cu Б) Fe3O4 Ag Na2O В) SO3 CaO K
Определите ряд веществ, которые взаимодействуют с водой. Составьте уравнения реакций 1.А) Na2O Ca CO2 Б) SO3 Al2O3 Cu В) Au CaO K A) SO2 CuO Cu Б) Fe3O4 Ag Na2O В) SO3 CaO K