X
Код презентации скопируйте его
Общая характеристика оксидов
Скачать эту презентациюПрезентация на тему Общая характеристика оксидов
Скачать эту презентациюCлайд 2
 Оксиды - это сложные вещества, состоящие из двух элементов, один из которых кислород. Например: CaO, SO2, Al2O3, CO.
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых кислород. Например: CaO, SO2, Al2O3, CO.
Cлайд 3
 Оксиды Оксиды – соединения элементов с кислородом (кроме соединений фтора). Степень окисления кислорода в оксидах равна – II. Один из способов получения оксидов – реакция окисления (в частности, горения) Действие углекислотного огнетушителя
Оксиды Оксиды – соединения элементов с кислородом (кроме соединений фтора). Степень окисления кислорода в оксидах равна – II. Один из способов получения оксидов – реакция окисления (в частности, горения) Действие углекислотного огнетушителя
Cлайд 4
 Способы получения оксидов. Взаимодействие простых веществ с кислородом: 2Mg + O2 = 2Mg O 2. Горение на воздухе сложных веществ: CH4 + 2O2 = CO2 + 2H2O 3. Разложение нерастворимых оснований: Mg(OH)2 = MgO + H2O 4. Разложение некоторых кислот: H2SiO3 = SiO2 + H2O 5. Разложение некоторых солей: CaCO3 = CaO + CO2
Способы получения оксидов. Взаимодействие простых веществ с кислородом: 2Mg + O2 = 2Mg O 2. Горение на воздухе сложных веществ: CH4 + 2O2 = CO2 + 2H2O 3. Разложение нерастворимых оснований: Mg(OH)2 = MgO + H2O 4. Разложение некоторых кислот: H2SiO3 = SiO2 + H2O 5. Разложение некоторых солей: CaCO3 = CaO + CO2
Cлайд 6
 Несолеобразующие оксиды Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями и не образуют солей. Оксиды образованы атомами неметаллов: CO, NO, N2O, SiO. Солеобразующие оксиды Это оксиды, которые взаимодействуют с кислотами или со щелочами с образованием солей и воды: N2O5, CO2, CaO, Na2O.
Несолеобразующие оксиды Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями и не образуют солей. Оксиды образованы атомами неметаллов: CO, NO, N2O, SiO. Солеобразующие оксиды Это оксиды, которые взаимодействуют с кислотами или со щелочами с образованием солей и воды: N2O5, CO2, CaO, Na2O.
Cлайд 7
 Основные оксиды Это оксиды, которым в качестве гидроксидов соответствуют основания. Например: CuO → Cu(OH)2 Основные оксиды образуют только металлы со степенью окисления +1, +2. Например: Na2O, K2O, CaO, MgO, CuO, CrO. Исключение BeO, ZnO, SnO, PbO.
Основные оксиды Это оксиды, которым в качестве гидроксидов соответствуют основания. Например: CuO → Cu(OH)2 Основные оксиды образуют только металлы со степенью окисления +1, +2. Например: Na2O, K2O, CaO, MgO, CuO, CrO. Исключение BeO, ZnO, SnO, PbO.
Cлайд 8
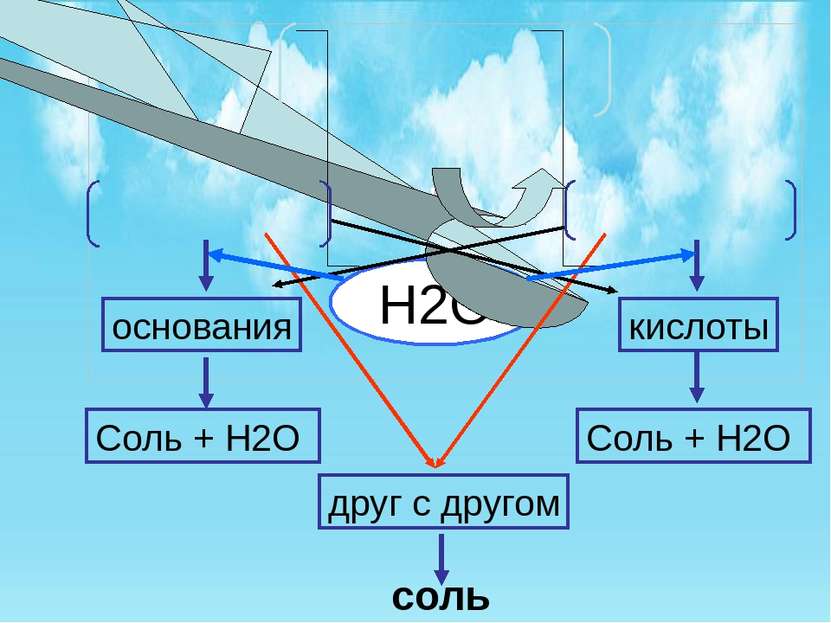
 Химические свойства основных оксидов. Взаимодействие с кислотами, с образованием соли и воды: MgO + HCl = MgCl2 + H2O 2. С кислотными оксидами, образуя соли: CaO + N2O5 = Ca(NO3)2 3. С водой (реагируют только оксиды щелочных и щелочно-земельных металлов): Na2O + H2O = 2NaOH
Химические свойства основных оксидов. Взаимодействие с кислотами, с образованием соли и воды: MgO + HCl = MgCl2 + H2O 2. С кислотными оксидами, образуя соли: CaO + N2O5 = Ca(NO3)2 3. С водой (реагируют только оксиды щелочных и щелочно-земельных металлов): Na2O + H2O = 2NaOH
Cлайд 9
 Кислотные оксиды Это оксиды, которым в качестве гидроксидов соответствуют кислоты. Например: SO3 → H2SO4 Кислотные оксиды образуют все неметаллы в любой степени окисления, исключая несолеобразующие оксиды, и металлы со степенью окисления +5 и выше. Например: CO2, N2O5, SiO2, Mn2O7, CrO3.
Кислотные оксиды Это оксиды, которым в качестве гидроксидов соответствуют кислоты. Например: SO3 → H2SO4 Кислотные оксиды образуют все неметаллы в любой степени окисления, исключая несолеобразующие оксиды, и металлы со степенью окисления +5 и выше. Например: CO2, N2O5, SiO2, Mn2O7, CrO3.
Cлайд 10
 Химические свойства кислотных оксидов. С основаниями, образуя соль и воду: CO2 + 2KOH = K2CO3 + H2O 2. С основными оксидами, образуя соли: CO2 + MgO = MgCO3 3. С водой (большинство оксидов), образуя кислоты: SO3 + H2O = H2SO4 CrO3 + H2O = H2CrO4
Химические свойства кислотных оксидов. С основаниями, образуя соль и воду: CO2 + 2KOH = K2CO3 + H2O 2. С основными оксидами, образуя соли: CO2 + MgO = MgCO3 3. С водой (большинство оксидов), образуя кислоты: SO3 + H2O = H2SO4 CrO3 + H2O = H2CrO4
Cлайд 12
 Амфотерные Оксиды. Это оксиды, которым соответствуют гидроксиды, проявляющие свойства как оснований, так и кислот. Например: BeO → Be(OH)2 → H2BeO2 ZnO → Zn(OH)2 → H2ZnO2 Амфотерные оксиды образуют только металлы со степенью окисления +3, +4. Например: Cr2O3, Fe2O3, Al2O3. Оксиды BeO, ZnO , SnO, PbO также являются амфотерными.
Амфотерные Оксиды. Это оксиды, которым соответствуют гидроксиды, проявляющие свойства как оснований, так и кислот. Например: BeO → Be(OH)2 → H2BeO2 ZnO → Zn(OH)2 → H2ZnO2 Амфотерные оксиды образуют только металлы со степенью окисления +3, +4. Например: Cr2O3, Fe2O3, Al2O3. Оксиды BeO, ZnO , SnO, PbO также являются амфотерными.
Cлайд 13
 Химические свойства амфотерных оксидов. В качестве основных оксидов. С кислотами, образуя соль и воду: ZnO + 2HCl = ZnCl2 + H2O 2. С кислотными оксидами, образуя соли: ZnO + SiO2 = ZnSiO3 В качестве кислотных оксидов. Со щелочами, образуя соль и воду: ZnO + 2KOH = K2ZnO2 + H2O 2. С основными оксидами, образуя соли: ZnO + CaO = CaZnO2 С водой амфотерные оксиды не взаимодействуют.
Химические свойства амфотерных оксидов. В качестве основных оксидов. С кислотами, образуя соль и воду: ZnO + 2HCl = ZnCl2 + H2O 2. С кислотными оксидами, образуя соли: ZnO + SiO2 = ZnSiO3 В качестве кислотных оксидов. Со щелочами, образуя соль и воду: ZnO + 2KOH = K2ZnO2 + H2O 2. С основными оксидами, образуя соли: ZnO + CaO = CaZnO2 С водой амфотерные оксиды не взаимодействуют.
Cлайд 14
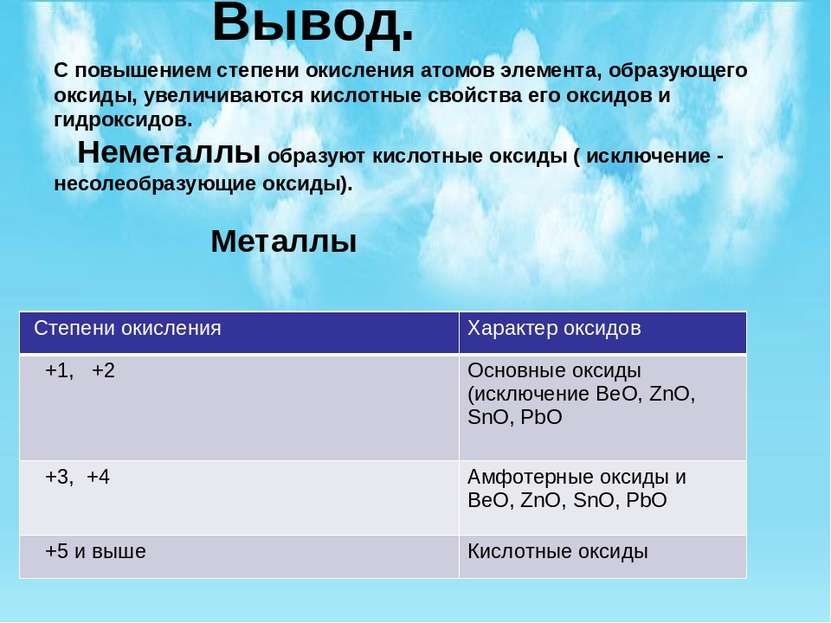
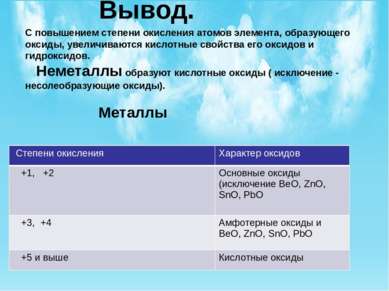 Вывод. С повышением степени окисления атомов элемента, образующего оксиды, увеличиваются кислотные свойства его оксидов и гидроксидов. Неметаллы образуют кислотные оксиды ( исключение - несолеобразующие оксиды). Металлы Степени окисления Характер оксидов +1, +2 Основные оксиды (исключениеBeO,ZnO,SnO,PbO +3,+4 Амфотерныеоксиды иBeO,ZnO,SnO,PbO +5 и выше Кислотные оксиды
Вывод. С повышением степени окисления атомов элемента, образующего оксиды, увеличиваются кислотные свойства его оксидов и гидроксидов. Неметаллы образуют кислотные оксиды ( исключение - несолеобразующие оксиды). Металлы Степени окисления Характер оксидов +1, +2 Основные оксиды (исключениеBeO,ZnO,SnO,PbO +3,+4 Амфотерныеоксиды иBeO,ZnO,SnO,PbO +5 и выше Кислотные оксиды
Cлайд 15
 Газ, необходимый растениям для фотосинтеза Содержание углекислого газа в атмосфере относительно невелико, всего 0,04—0,03%. В воздухе, выдыхаемом человеком, углекислого газа 4%. Растения благодаря фотосинтезу усваивают углекислый газ из атмосферы, превращая минеральные вещества в органические — глюкозу, крахмал.
Газ, необходимый растениям для фотосинтеза Содержание углекислого газа в атмосфере относительно невелико, всего 0,04—0,03%. В воздухе, выдыхаемом человеком, углекислого газа 4%. Растения благодаря фотосинтезу усваивают углекислый газ из атмосферы, превращая минеральные вещества в органические — глюкозу, крахмал.
Cлайд 16
 Один из распространенных оксидов – диоксид углерода CO2 – содержится в составе вулканических газов. В природе
Один из распространенных оксидов – диоксид углерода CO2 – содержится в составе вулканических газов. В природе
Cлайд 17
 Cухой лед – тоже CO2 Сухой лед в отличие от водяного льда плотный. Он тонет в воде, резко охлаждая ее. Горящий бензин можно быстро потушить, бросив в пламя несколько кусочков сухого льда. Главное применение сухого льда — хранение и перевозка продуктов: рыбы, мяса, мороженого. Ценность сухого льда заключается не только в его охлаждающем действии но и в том, что продукты в углекислом газе не плесневеют, не гниют.
Cухой лед – тоже CO2 Сухой лед в отличие от водяного льда плотный. Он тонет в воде, резко охлаждая ее. Горящий бензин можно быстро потушить, бросив в пламя несколько кусочков сухого льда. Главное применение сухого льда — хранение и перевозка продуктов: рыбы, мяса, мороженого. Ценность сухого льда заключается не только в его охлаждающем действии но и в том, что продукты в углекислом газе не плесневеют, не гниют.
Cлайд 18
 Оксид хрома(III) – Cr2O3 –кристаллы зеленого цвета, нерастворимые в воде. Cr2O3 используют как пигмент при изготовлении декоративного зеленого стекла и керамики. Паста ГОИ (“Государственный оптический институт”) на основе Cr2O3 применяется для шлифовки и полировки оптических изделий, в ювелирном деле. ОКСИД ХРОМА Cr2O3
Оксид хрома(III) – Cr2O3 –кристаллы зеленого цвета, нерастворимые в воде. Cr2O3 используют как пигмент при изготовлении декоративного зеленого стекла и керамики. Паста ГОИ (“Государственный оптический институт”) на основе Cr2O3 применяется для шлифовки и полировки оптических изделий, в ювелирном деле. ОКСИД ХРОМА Cr2O3
Cлайд 19
 Оксид магния MgO Оксид магния – основный оксид. Магниевая лента, вступив в реакцию с кислородом воздуха, горит ярким белым пламенем.
Оксид магния MgO Оксид магния – основный оксид. Магниевая лента, вступив в реакцию с кислородом воздуха, горит ярким белым пламенем.
Cлайд 20
 Оксид кремния (IV) SiO2 Плиний считал, что горный хрусталь «рождается из небесной влаги и чистейшего снега». Однако состав его иной: оксид кремния (IV) SiO2. Кварц, кремень, горный хрусталь, аметист, яшма, опал — все это оксид кремния (IV).
Оксид кремния (IV) SiO2 Плиний считал, что горный хрусталь «рождается из небесной влаги и чистейшего снега». Однако состав его иной: оксид кремния (IV) SiO2. Кварц, кремень, горный хрусталь, аметист, яшма, опал — все это оксид кремния (IV).
Cлайд 21
 Оксид цинка ZnO – вещество белого цвета, используется для приготовления белой масляной краски (цинковые белила). Цинковыми белилами можно красить любые поверхности, в том числе и те, которые подвергаются воздействию атмосферных осадков. Фармацевты делают из оксида цинка вяжущий и подсушивающий порошок для наружного применения. Такими же ценными свойствами обладает оксид титана (IV) – TiO2. Он тоже имеет красивый белый цвет и применяется для изготовления титановых белил. .… БЕЛИЛА
Оксид цинка ZnO – вещество белого цвета, используется для приготовления белой масляной краски (цинковые белила). Цинковыми белилами можно красить любые поверхности, в том числе и те, которые подвергаются воздействию атмосферных осадков. Фармацевты делают из оксида цинка вяжущий и подсушивающий порошок для наружного применения. Такими же ценными свойствами обладает оксид титана (IV) – TiO2. Он тоже имеет красивый белый цвет и применяется для изготовления титановых белил. .… БЕЛИЛА
Cлайд 22
 Задания. Определите характер данных оксидов CO2, ZnO, Na2O, SO2, CaO, NO и напишите соответствующие им гидроксиды. 2. Из предложенного ряда K2O, SO3, NaOH, HCl, ZnO, CaSO4, H2O выпишите вещества, реагирующие с оксидом кальция. Напишите уравнения соответствующих реакций в молекулярном и ионно-молекулярном виде. 3. Найдите массу оксида магния, образовавшегося при горении 0,3 моль магния.
Задания. Определите характер данных оксидов CO2, ZnO, Na2O, SO2, CaO, NO и напишите соответствующие им гидроксиды. 2. Из предложенного ряда K2O, SO3, NaOH, HCl, ZnO, CaSO4, H2O выпишите вещества, реагирующие с оксидом кальция. Напишите уравнения соответствующих реакций в молекулярном и ионно-молекулярном виде. 3. Найдите массу оксида магния, образовавшегося при горении 0,3 моль магния.