X
Код презентации скопируйте его
Алкены. Этилен (непредельные углеводороды)
Скачать эту презентациюПрезентация на тему Алкены. Этилен (непредельные углеводороды)
Скачать эту презентациюCлайд 2
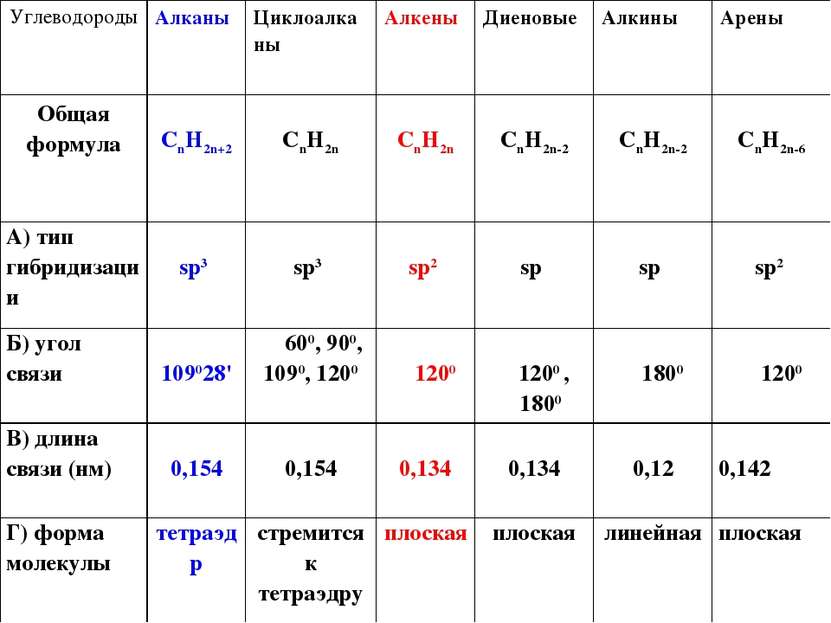
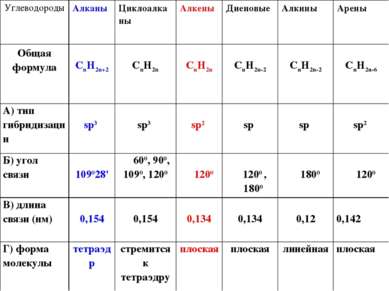 Углеводороды Алканы Циклоалканы Алкены Диеновые Алкины Арены Общая формула CnH2n+2 CnH2n CnH2n CnH2n-2 CnH2n-2 CnH2n-6 А) тип гибридизации sp3 sp3 sp2 sp sp sp2 Б) угол связи ∟ 109028' ∟ 600, 900, 1090, 1200 ∟1200 ∟1200 , ∟1800 ∟1800 ∟1200 В) длина связи (нм) 0,154 0,154 0,134 0,134 0,12 0,142 Г) форма молекулы тетраэдр стремится к тетраэдру плоская плоская линейная плоская
Углеводороды Алканы Циклоалканы Алкены Диеновые Алкины Арены Общая формула CnH2n+2 CnH2n CnH2n CnH2n-2 CnH2n-2 CnH2n-6 А) тип гибридизации sp3 sp3 sp2 sp sp sp2 Б) угол связи ∟ 109028' ∟ 600, 900, 1090, 1200 ∟1200 ∟1200 , ∟1800 ∟1800 ∟1200 В) длина связи (нм) 0,154 0,154 0,134 0,134 0,12 0,142 Г) форма молекулы тетраэдр стремится к тетраэдру плоская плоская линейная плоская
Cлайд 3
 Алкены (Олефины) Алкены — это непредельные углеводороды, содержащие в молекуле, кроме одинарных связей, одну двойную С=С связь. Алкены соответствуют общей формуле СnН2n.
Алкены (Олефины) Алкены — это непредельные углеводороды, содержащие в молекуле, кроме одинарных связей, одну двойную С=С связь. Алкены соответствуют общей формуле СnН2n.
Cлайд 4
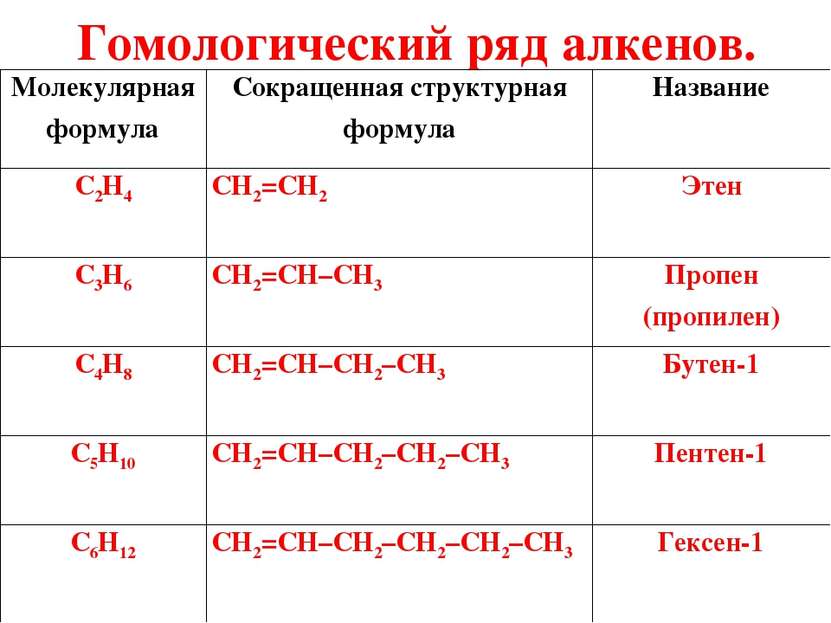
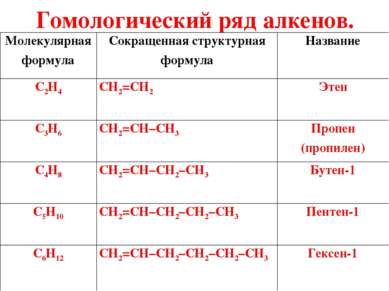 Гомологический ряд алкенов. Молекулярная формула Сокращенная структурная формула Название C2H4 CH2=CH2 Этен C3H6 CH2=CH–CH3 Пропен (пропилен) C4H8 CH2=CH–CH2–CH3 Бутен-1 C5H10 CH2=CH–CH2–CH2–CH3 Пентен-1 C6H12 CH2=CH–CH2–CH2–CH2–CH3 Гексен-1
Гомологический ряд алкенов. Молекулярная формула Сокращенная структурная формула Название C2H4 CH2=CH2 Этен C3H6 CH2=CH–CH3 Пропен (пропилен) C4H8 CH2=CH–CH2–CH3 Бутен-1 C5H10 CH2=CH–CH2–CH2–CH3 Пентен-1 C6H12 CH2=CH–CH2–CH2–CH2–CH3 Гексен-1
Cлайд 5
 Номенклатура ИЮПАК Правила при составлении названий алкенов: 1) Выбор главной цепи. В случае алкенов главная цепь должна содержать одну двойную связь (С=С) 2) Нумерация главной цепи. Нумерация атомов углерода главной цепи начинается с того конца, к которому ближе находится двойная связь. 3) Формирование названия. С учетом всех заместителей.
Номенклатура ИЮПАК Правила при составлении названий алкенов: 1) Выбор главной цепи. В случае алкенов главная цепь должна содержать одну двойную связь (С=С) 2) Нумерация главной цепи. Нумерация атомов углерода главной цепи начинается с того конца, к которому ближе находится двойная связь. 3) Формирование названия. С учетом всех заместителей.
Cлайд 6
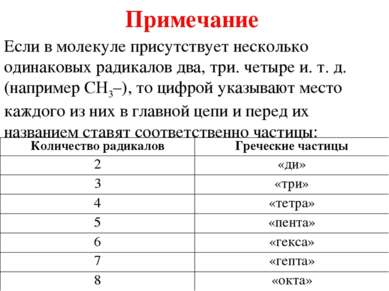 Примечание Если в молекуле присутствует несколько одинаковых радикалов два, три. четыре и. т. д. (например CH3–), то цифрой указывают место каждого из них в главной цепи и перед их названием ставят соответственно частицы: Количество радикалов Греческие частицы 2 «ди» 3 «три» 4 «тетра» 5 «пента» 6 «гекса» 7 «гепта» 8 «окта»
Примечание Если в молекуле присутствует несколько одинаковых радикалов два, три. четыре и. т. д. (например CH3–), то цифрой указывают место каждого из них в главной цепи и перед их названием ставят соответственно частицы: Количество радикалов Греческие частицы 2 «ди» 3 «три» 4 «тетра» 5 «пента» 6 «гекса» 7 «гепта» 8 «окта»
Cлайд 7
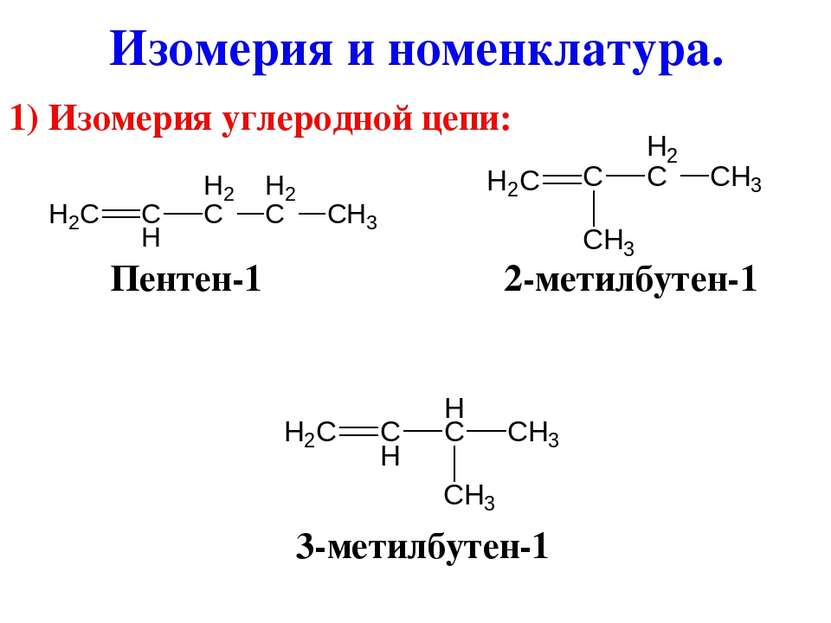
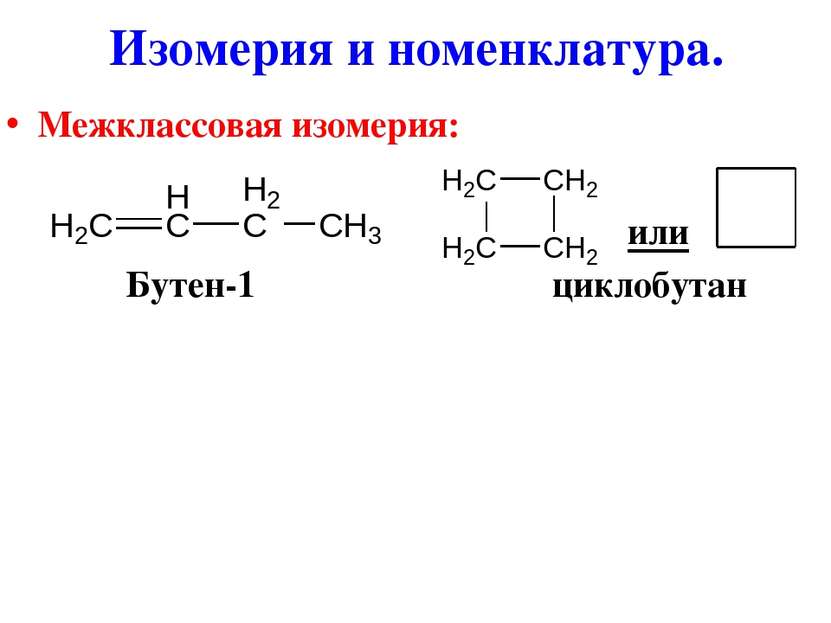
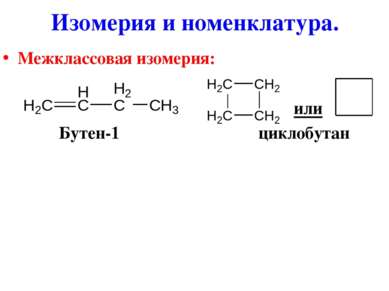
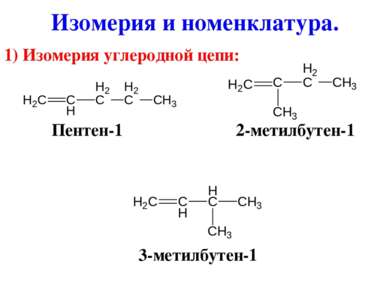 Изомерия и номенклатура. 1) Изомерия углеродной цепи: Пентен-1 2-метилбутен-1 3-метилбутен-1
Изомерия и номенклатура. 1) Изомерия углеродной цепи: Пентен-1 2-метилбутен-1 3-метилбутен-1
Cлайд 8
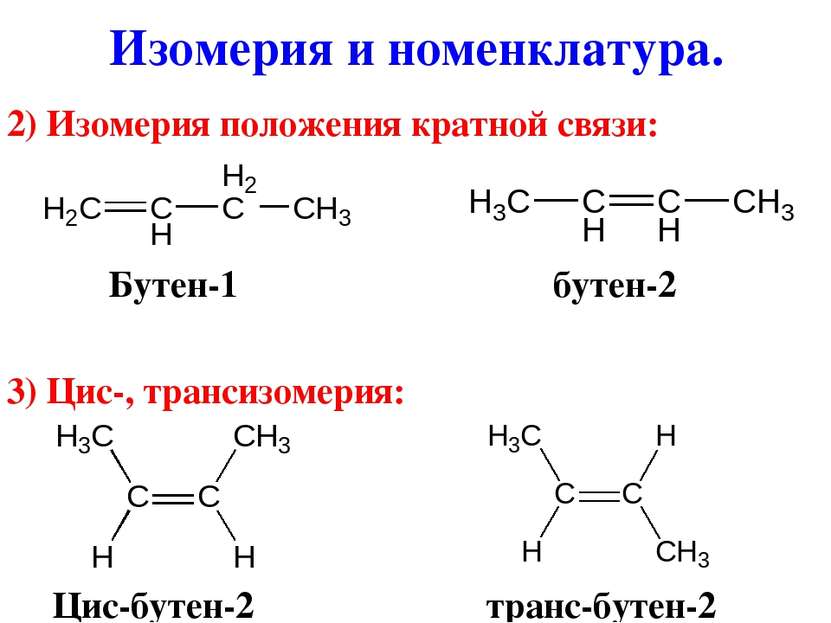
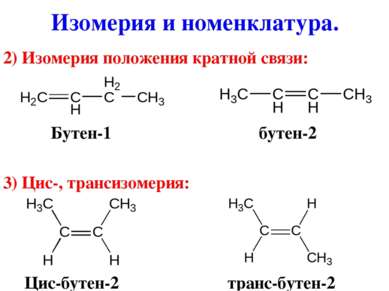 2) Изомерия положения кратной связи: Бутен-1 бутен-2 3) Цис-, трансизомерия: Цис-бутен-2 транс-бутен-2 Изомерия и номенклатура.
2) Изомерия положения кратной связи: Бутен-1 бутен-2 3) Цис-, трансизомерия: Цис-бутен-2 транс-бутен-2 Изомерия и номенклатура.
Cлайд 10
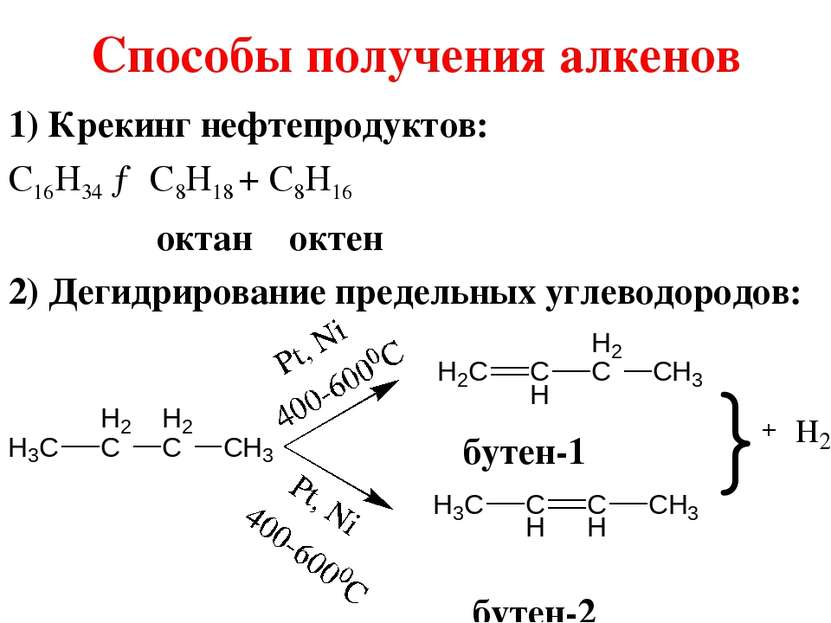
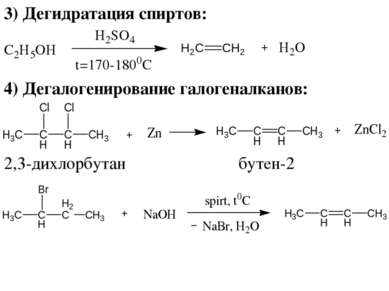
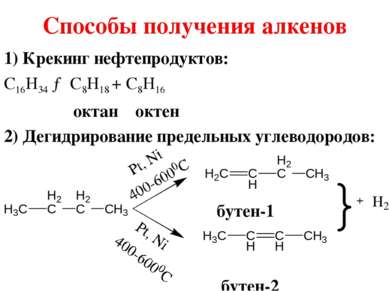 Способы получения алкенов 1) Крекинг нефтепродуктов: C16H34 → C8H18 + C8H16 октан октен 2) Дегидрирование предельных углеводородов: бутен-1 бутен-2
Способы получения алкенов 1) Крекинг нефтепродуктов: C16H34 → C8H18 + C8H16 октан октен 2) Дегидрирование предельных углеводородов: бутен-1 бутен-2
Cлайд 12
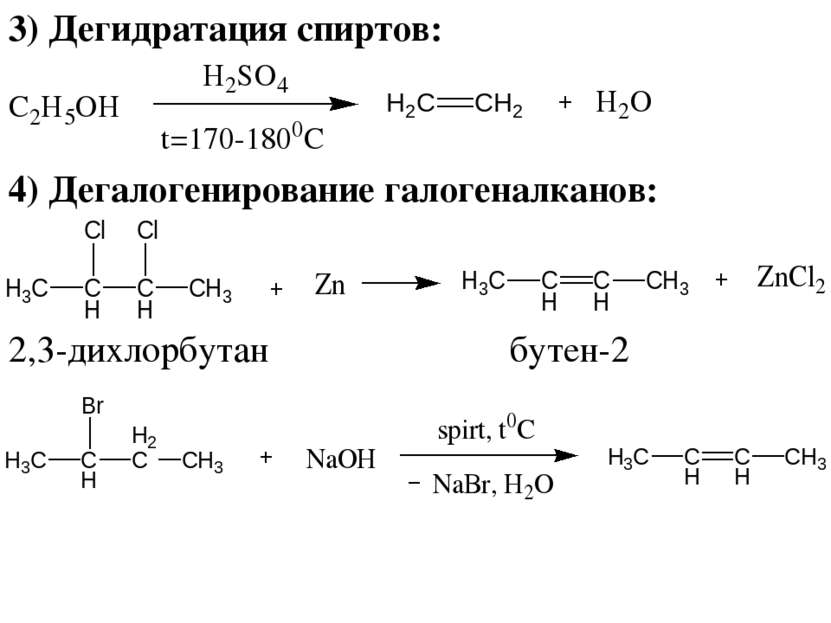
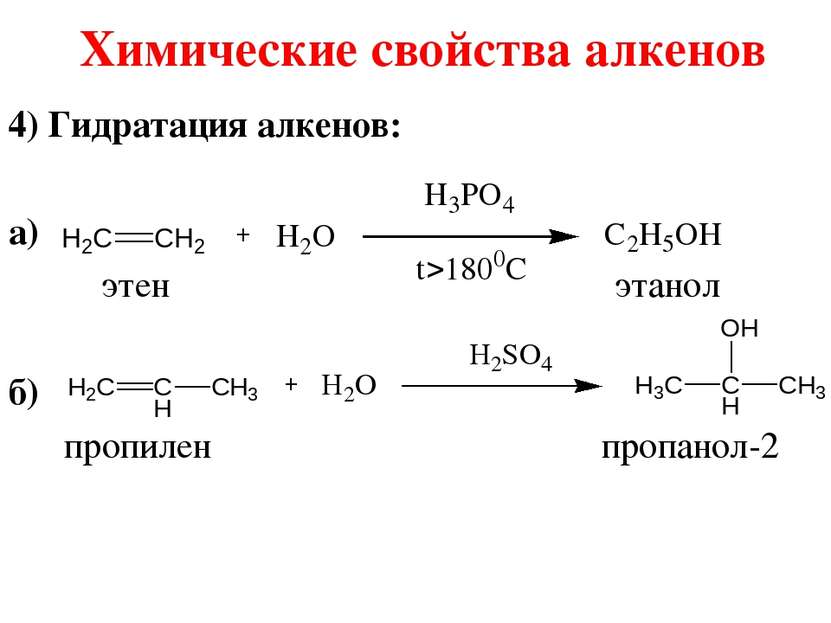
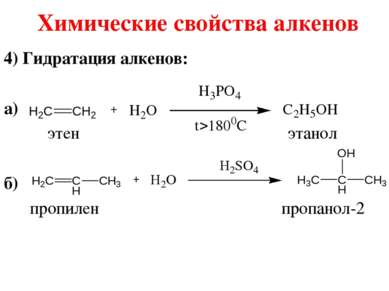
 Химические свойства алкенов 1) Гидрирования алкенов (kat – Pt, Pd, Ni): CH3–CH=CH2 + H2 → CH3–CH2–CH3 2) Галогенирование алкенов: CH2=CH2 +Br2 → CH2Br–CH2Br 3) Гидрогалогенирование алкенов (правило Марковникова): CH3–CH=CH2 + HBr → CH3–CHBr–CH3 При присоединении галогеноводорода к алкену, водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген к менее гидрированному.
Химические свойства алкенов 1) Гидрирования алкенов (kat – Pt, Pd, Ni): CH3–CH=CH2 + H2 → CH3–CH2–CH3 2) Галогенирование алкенов: CH2=CH2 +Br2 → CH2Br–CH2Br 3) Гидрогалогенирование алкенов (правило Марковникова): CH3–CH=CH2 + HBr → CH3–CHBr–CH3 При присоединении галогеноводорода к алкену, водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген к менее гидрированному.