X
Код презентации скопируйте его
Серная кислота, свойства серной кислоты
Скачать эту презентациюПрезентация на тему Серная кислота, свойства серной кислоты
Скачать эту презентациюCлайд 2
 Состав Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток H-R, где R-кислотный остаток При электролитической диссоциации кислот в водном растворе образуются катионы водорода и анион кислотного остатка
Состав Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток H-R, где R-кислотный остаток При электролитической диссоциации кислот в водном растворе образуются катионы водорода и анион кислотного остатка
Cлайд 3
 Классификация кислот Одноосновные кислоты, например, HCl, HNO3 (отщепляют при диссоциации один атом водорода) Многоосновные кислоты, например, H2SO4, H3PO4 (отщепляют при диссоциации несколько атомов водорода) Кислородные кислоты, например, H2CO3, H3PO4 (отвечают кислотным оксидам и являются фактически кислотными гидроксидами) Бескислородные кислоты, например, HBr, H2S (относятся к числу бинарных соединений)
Классификация кислот Одноосновные кислоты, например, HCl, HNO3 (отщепляют при диссоциации один атом водорода) Многоосновные кислоты, например, H2SO4, H3PO4 (отщепляют при диссоциации несколько атомов водорода) Кислородные кислоты, например, H2CO3, H3PO4 (отвечают кислотным оксидам и являются фактически кислотными гидроксидами) Бескислородные кислоты, например, HBr, H2S (относятся к числу бинарных соединений)
Cлайд 4
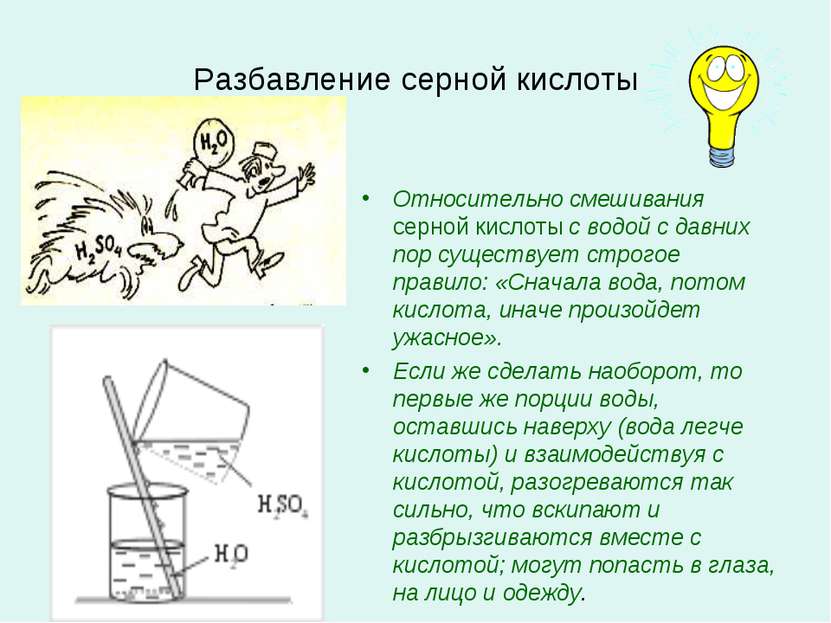
 Разбавление серной кислоты Относительно смешивания серной кислоты с водой с давних пор существует строгое правило: «Сначала вода, потом кислота, иначе произойдет ужасное». Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
Разбавление серной кислоты Относительно смешивания серной кислоты с водой с давних пор существует строгое правило: «Сначала вода, потом кислота, иначе произойдет ужасное». Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
Cлайд 5
 S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы) S+6O3- бесцветная жидкость Получение серной кислоты: S+6O3 + Н2О =Н2 S+6O4 серная кислота
S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы) S+6O3- бесцветная жидкость Получение серной кислоты: S+6O3 + Н2О =Н2 S+6O4 серная кислота
Cлайд 6
 Химические свойства серной кислоты разбавленная серная кислота проявляет все характерные свойства кислот: С оксидами металлов.(реакция обмена) Н2SO4+MeO→MeSO4+H2O 2. С основаниями.(реакция обмена, реакция нейтрализации) Н2SO4+Me(OН)n→MeSO4+H2O 3. С металлами. Н2SO4+Me(до Н)→MeSO4(р)+H2↑(реакция замещения) 4.С солями( реакция обмена) Н2SO4+MeR(Р)→MeSO4 (Р)+HR (протекает в том случае, если образуется осадок или газ)
Химические свойства серной кислоты разбавленная серная кислота проявляет все характерные свойства кислот: С оксидами металлов.(реакция обмена) Н2SO4+MeO→MeSO4+H2O 2. С основаниями.(реакция обмена, реакция нейтрализации) Н2SO4+Me(OН)n→MeSO4+H2O 3. С металлами. Н2SO4+Me(до Н)→MeSO4(р)+H2↑(реакция замещения) 4.С солями( реакция обмена) Н2SO4+MeR(Р)→MeSO4 (Р)+HR (протекает в том случае, если образуется осадок или газ)
Cлайд 7
 Качественная реакция на ион –SO42- Реактивом на серную кислоту и ее соли является катион бария , т.к. с ионами бария сульфат ион образует белый нерастворимый сульфат бария, выпадающий в осадок. Ва2++SO42- = BaSO4↓
Качественная реакция на ион –SO42- Реактивом на серную кислоту и ее соли является катион бария , т.к. с ионами бария сульфат ион образует белый нерастворимый сульфат бария, выпадающий в осадок. Ва2++SO42- = BaSO4↓
Cлайд 8
 Концентрированная серная кислота Ме+Н2SO4(кoнц)→МеSO4+H2O+(Н2S,S,SO2) Серная кислота(конц) восстанавливается до (Н2S,S,SO2) в зависимости от активности металла и условий протекания реакции. Железо и алюминий пассивируются кислотой, т.е покрываются защитной пленкой, поэтому кислоту(конц) можно перевозить в стальных и алюминиевых цистернах. Сu+2H2SO4(конц)→CuSO4+2H2O+SO2 4Zn+5H2SO4(конц)→4ZnSO4+4H2O+H2S Концентрированная серная кислота способна отнимать воду из молекул органических веществ, обугливая их. Взаимодействие кислоты с сахарозой(C12H22O11) C12H22O11 + 2H2SO4(конц) = 11C + 13H2O↑ +2SO2↑ +CO2↑
Концентрированная серная кислота Ме+Н2SO4(кoнц)→МеSO4+H2O+(Н2S,S,SO2) Серная кислота(конц) восстанавливается до (Н2S,S,SO2) в зависимости от активности металла и условий протекания реакции. Железо и алюминий пассивируются кислотой, т.е покрываются защитной пленкой, поэтому кислоту(конц) можно перевозить в стальных и алюминиевых цистернах. Сu+2H2SO4(конц)→CuSO4+2H2O+SO2 4Zn+5H2SO4(конц)→4ZnSO4+4H2O+H2S Концентрированная серная кислота способна отнимать воду из молекул органических веществ, обугливая их. Взаимодействие кислоты с сахарозой(C12H22O11) C12H22O11 + 2H2SO4(конц) = 11C + 13H2O↑ +2SO2↑ +CO2↑