X
Код презентации скопируйте его
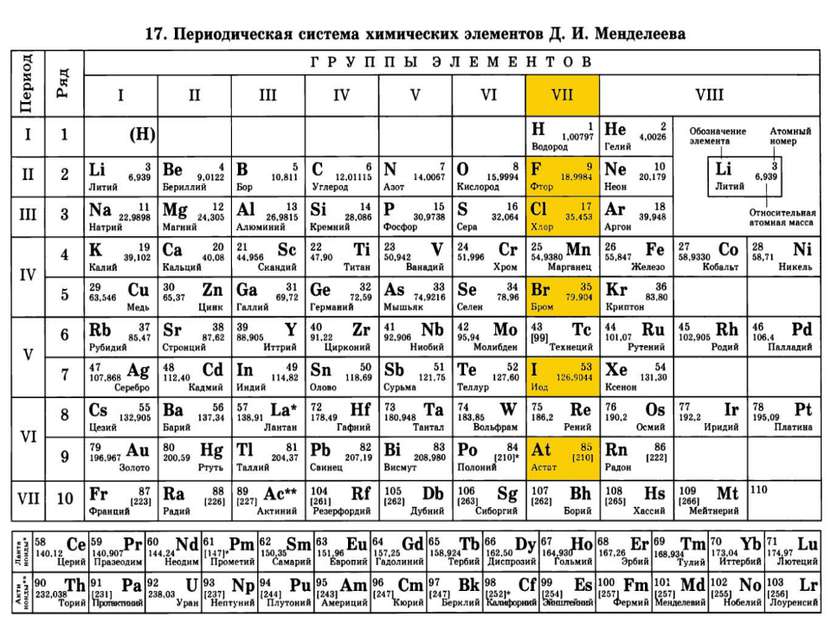
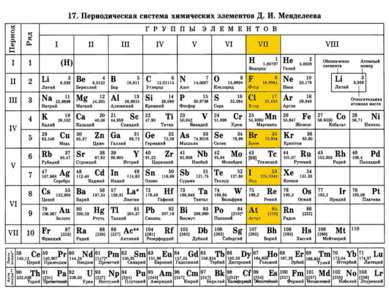
Характеристика элементов VII группы главной подгруппы. Хлор
Скачать эту презентациюПрезентация на тему Характеристика элементов VII группы главной подгруппы. Хлор
Скачать эту презентациюCлайд 6
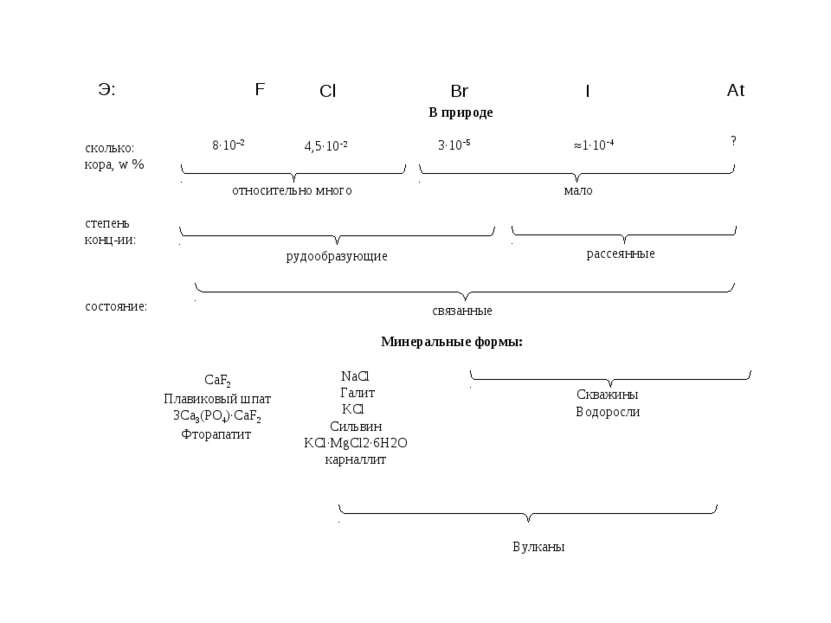
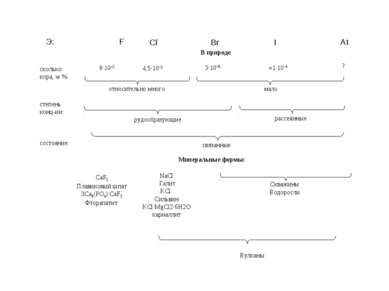
 Нахождение в природе В земной коре хлор - самый распространённый галоген. Поскольку хлор очень активен, в природе он встречается только в виде соединений в составе минералов: Галит NaCl Галит синий. Нью-Мексико, США Галит (фиолетовый). Саксония-Анхальт, Германия.
Нахождение в природе В земной коре хлор - самый распространённый галоген. Поскольку хлор очень активен, в природе он встречается только в виде соединений в составе минералов: Галит NaCl Галит синий. Нью-Мексико, США Галит (фиолетовый). Саксония-Анхальт, Германия.
Cлайд 7
 Сильвин KCl Сильвин, Германия. Музей им. А.Е.Ферсмана Сильвин и галит, Соликамск. Музей им. А.Е.Ферсмана Сильвинит KCl · NaCl Сильвинит. Верхнекамское месторождение (Пермский край) Сильвинит или калийная соль. Добыча
Сильвин KCl Сильвин, Германия. Музей им. А.Е.Ферсмана Сильвин и галит, Соликамск. Музей им. А.Е.Ферсмана Сильвинит KCl · NaCl Сильвинит. Верхнекамское месторождение (Пермский край) Сильвинит или калийная соль. Добыча
Cлайд 11
 Характеристика химического элемента Хлор – элемент VII А группы. Порядковый номер 17 Относительная атомная масса: 35,4527 а. е. м. (г/моль) Количество протонов, нейтронов, электронов: 17,18,17 Строение атома:
Характеристика химического элемента Хлор – элемент VII А группы. Порядковый номер 17 Относительная атомная масса: 35,4527 а. е. м. (г/моль) Количество протонов, нейтронов, электронов: 17,18,17 Строение атома:
Cлайд 12
 Электронная формула: Типичные степени окисления: -1, 0, +1, +3, +4, +5, +7 Энергия ионизации: 1254,9(13,01) кДж/моль (эВ) Сродство к электрону: 349 (кДж/моль) Электроотрицательность по Полингу: 3,20
Электронная формула: Типичные степени окисления: -1, 0, +1, +3, +4, +5, +7 Энергия ионизации: 1254,9(13,01) кДж/моль (эВ) Сродство к электрону: 349 (кДж/моль) Электроотрицательность по Полингу: 3,20
Cлайд 13
 Характеристика простого вещества Тип связи: ковалентная неполярная Молекула двухатомная Изотопы: 35Cl (75,78 %) и 37Cl(24,22 %) Тип кристаллической решетки: молекулярная Молекулярная кристаллическая решётка
Характеристика простого вещества Тип связи: ковалентная неполярная Молекула двухатомная Изотопы: 35Cl (75,78 %) и 37Cl(24,22 %) Тип кристаллической решетки: молекулярная Молекулярная кристаллическая решётка
Cлайд 14
 Термодинамические параметры Параметр Значение ΔH°обр. (298 К, газ) 0 (кДж/моль) S°обр (298 К, газ) 222,9 (Дж/моль·K) ΔHплавления 6,406 (кДж/моль) ΔHкипения 20,41 (кДж/моль) Энергия гомолитического разрыва связи Х-Х 243 (кДж/моль) Энергия гетеролитического разрыва связи Х-Х 1150 (кДж/моль)
Термодинамические параметры Параметр Значение ΔH°обр. (298 К, газ) 0 (кДж/моль) S°обр (298 К, газ) 222,9 (Дж/моль·K) ΔHплавления 6,406 (кДж/моль) ΔHкипения 20,41 (кДж/моль) Энергия гомолитического разрыва связи Х-Х 243 (кДж/моль) Энергия гетеролитического разрыва связи Х-Х 1150 (кДж/моль)
Cлайд 15
 Физические свойства Свойство Значение Цвет (газ) Жёлто-зелёный Температура кипения −34 °C Температура плавления −100 °C Температура разложения (диссоциации на атомы) ~1400 °C Плотность (газ, н.у.) 3,214 г/л Теплоемкость (298 К, газ) 34,94 (Дж/моль·K) Критическая температура 144 °C Критическое давление 76 атм Запах Резкий, удушающий
Физические свойства Свойство Значение Цвет (газ) Жёлто-зелёный Температура кипения −34 °C Температура плавления −100 °C Температура разложения (диссоциации на атомы) ~1400 °C Плотность (газ, н.у.) 3,214 г/л Теплоемкость (298 К, газ) 34,94 (Дж/моль·K) Критическая температура 144 °C Критическое давление 76 атм Запах Резкий, удушающий
Cлайд 16
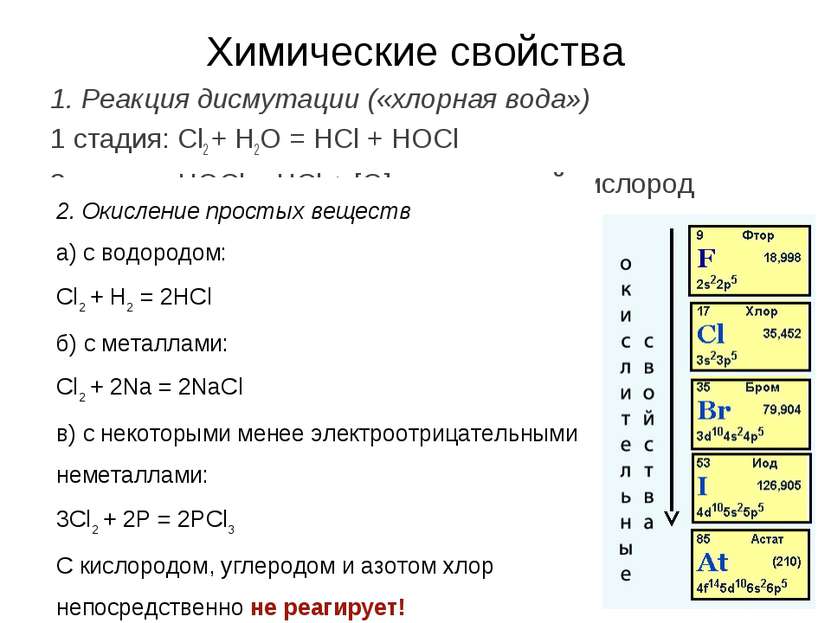
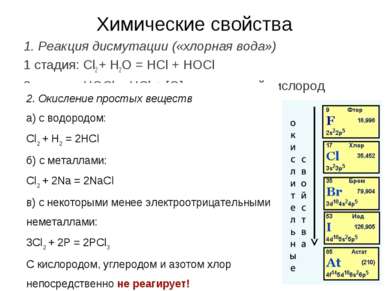 Химические свойства 1. Реакция дисмутации («хлорная вода») 1 стадия: Cl2 + H2O = HCl + HOCl 2 стадия: HOCl = HCl + [О] – атомарный кислород 2. Окисление простых веществ a) с водородом: Cl2 + H2 = 2HCl б) с металлами: Cl2 + 2Na = 2NaCl в) с некоторыми менее электроотрицательными неметаллами: 3Cl2 + 2P = 2PCl3 С кислородом, углеродом и азотом хлор непосредственно не реагирует!
Химические свойства 1. Реакция дисмутации («хлорная вода») 1 стадия: Cl2 + H2O = HCl + HOCl 2 стадия: HOCl = HCl + [О] – атомарный кислород 2. Окисление простых веществ a) с водородом: Cl2 + H2 = 2HCl б) с металлами: Cl2 + 2Na = 2NaCl в) с некоторыми менее электроотрицательными неметаллами: 3Cl2 + 2P = 2PCl3 С кислородом, углеродом и азотом хлор непосредственно не реагирует!
Cлайд 17
 3. Взаимодействие со сложными веществами а) с водой: см. выше реакция дисмутации б) с кислородсодержащими кислотами: не реагирует! в) с растворами щелочей: на холоду: Cl2 + 2NaOH = NaCl + NaClO + H2O при нагревании: 3Cl2+ 6 KOH = 5KCl + KClO3 + 3H2O д) со многими органическими веществами: Cl2 + CH4 = CH3Cl + HCl C6H6 + Cl2 = C6H5Cl + HCl
3. Взаимодействие со сложными веществами а) с водой: см. выше реакция дисмутации б) с кислородсодержащими кислотами: не реагирует! в) с растворами щелочей: на холоду: Cl2 + 2NaOH = NaCl + NaClO + H2O при нагревании: 3Cl2+ 6 KOH = 5KCl + KClO3 + 3H2O д) со многими органическими веществами: Cl2 + CH4 = CH3Cl + HCl C6H6 + Cl2 = C6H5Cl + HCl
Cлайд 18
 Важнейшие соединения хлора Хло роводоро д, хло ристый водоро д (HCl) Бесцветный, термически устойчивый газ (при н.у.) с резким запахом, дымящий во влажном воздухе, легко растворяется в воде с образованием хлороводородной (соляной) кислоты. При растворении в воде протекают следующие процессы: HClг + H2Oж = H3O+ж + Cl−ж Процесс растворения сильно экзотермичен. Соляная кислота образует соли — хлориды
Важнейшие соединения хлора Хло роводоро д, хло ристый водоро д (HCl) Бесцветный, термически устойчивый газ (при н.у.) с резким запахом, дымящий во влажном воздухе, легко растворяется в воде с образованием хлороводородной (соляной) кислоты. При растворении в воде протекают следующие процессы: HClг + H2Oж = H3O+ж + Cl−ж Процесс растворения сильно экзотермичен. Соляная кислота образует соли — хлориды
Cлайд 19
 Свойства соляной кислоты: Очень устойчива к нагреванию В воде кислота Слабый окислитель по протону Под действием сильных окислителей анион окисляется HCl → t°
Свойства соляной кислоты: Очень устойчива к нагреванию В воде кислота Слабый окислитель по протону Под действием сильных окислителей анион окисляется HCl → t°
Cлайд 20
 Как окислитель реагирует: Mg + 2 HCl → MgCl2 + H2↑ Конц. соляная кислота реагирует с медью: 2 Cu + 4 HCl → 2 H[CuCl2] + H2↑ FeO + 2 HCl → FeCl2 + H2O При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства: MnO2 + 4 HCl → MnCl2 + Cl2↑ + 2 H2O При нагревании окисляется кислородом (катализатор — хлорид меди(II) CuCl2): 4 HCl + O2 → 2 H2O +2 Cl2↑
Как окислитель реагирует: Mg + 2 HCl → MgCl2 + H2↑ Конц. соляная кислота реагирует с медью: 2 Cu + 4 HCl → 2 H[CuCl2] + H2↑ FeO + 2 HCl → FeCl2 + H2O При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства: MnO2 + 4 HCl → MnCl2 + Cl2↑ + 2 H2O При нагревании окисляется кислородом (катализатор — хлорид меди(II) CuCl2): 4 HCl + O2 → 2 H2O +2 Cl2↑
Cлайд 21
 Смесь 3v HCl : 1v HNO3 называется «царской водкой». Она способна растворять даже золото и платину. 4 H3O+ + 3 Cl− + NO3− = NOCl + Cl2 + 6 H2O Расстворение идет благодаря высокой концентрации хлорид-ионов : 3 Pt + 4 HNO3 + 18 HCl → 3 H2[PtCl6] + 4 NO↑ + 8 H2O Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение): R-CH=CH2 + HCl → R-CHCl-CH3 R-C≡CH + 2 HCl → R-CCl2-CH3
Смесь 3v HCl : 1v HNO3 называется «царской водкой». Она способна растворять даже золото и платину. 4 H3O+ + 3 Cl− + NO3− = NOCl + Cl2 + 6 H2O Расстворение идет благодаря высокой концентрации хлорид-ионов : 3 Pt + 4 HNO3 + 18 HCl → 3 H2[PtCl6] + 4 NO↑ + 8 H2O Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение): R-CH=CH2 + HCl → R-CHCl-CH3 R-C≡CH + 2 HCl → R-CCl2-CH3
Cлайд 22
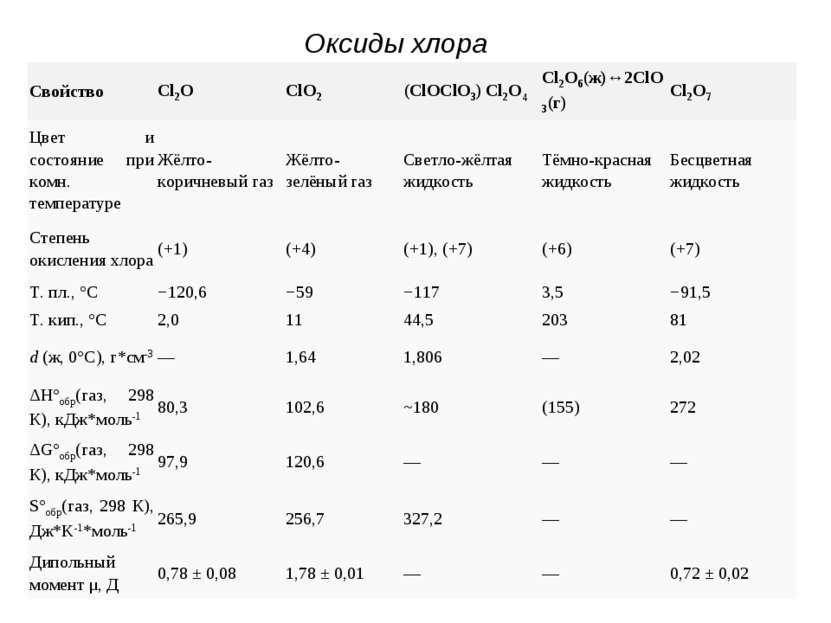
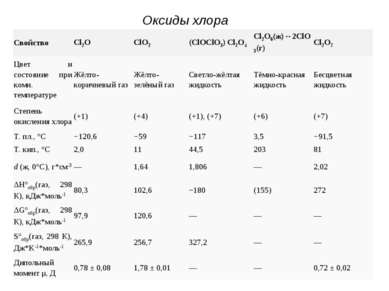 Оксиды хлора Свойство Cl2O ClO2 (ClOClO3) Cl2O4 Cl2O6(ж)↔2ClO3(г) Cl2O7 Цвет и состояние при комн. температуре Жёлто-коричневый газ Жёлто-зелёный газ Светло-жёлтая жидкость Тёмно-красная жидкость Бесцветная жидкость Степень окисления хлора (+1) (+4) (+1), (+7) (+6) (+7) Т. пл., °C −120,6 −59 −117 3,5 −91,5 Т. кип., °C 2,0 11 44,5 203 81 d (ж, 0°C), г*см-3 — 1,64 1,806 — 2,02 ΔH°обр(газ, 298 К), кДж*моль-1 80,3 102,6 ~180 (155) 272 ΔG°обр(газ, 298 К), кДж*моль-1 97,9 120,6 — — — S°обр(газ, 298 К), Дж*K-1*моль-1 265,9 256,7 327,2 — — Дипольный момент μ, Д 0,78 ± 0,08 1,78 ± 0,01 — — 0,72 ± 0,02
Оксиды хлора Свойство Cl2O ClO2 (ClOClO3) Cl2O4 Cl2O6(ж)↔2ClO3(г) Cl2O7 Цвет и состояние при комн. температуре Жёлто-коричневый газ Жёлто-зелёный газ Светло-жёлтая жидкость Тёмно-красная жидкость Бесцветная жидкость Степень окисления хлора (+1) (+4) (+1), (+7) (+6) (+7) Т. пл., °C −120,6 −59 −117 3,5 −91,5 Т. кип., °C 2,0 11 44,5 203 81 d (ж, 0°C), г*см-3 — 1,64 1,806 — 2,02 ΔH°обр(газ, 298 К), кДж*моль-1 80,3 102,6 ~180 (155) 272 ΔG°обр(газ, 298 К), кДж*моль-1 97,9 120,6 — — — S°обр(газ, 298 К), Дж*K-1*моль-1 265,9 256,7 327,2 — — Дипольный момент μ, Д 0,78 ± 0,08 1,78 ± 0,01 — — 0,72 ± 0,02
Cлайд 23
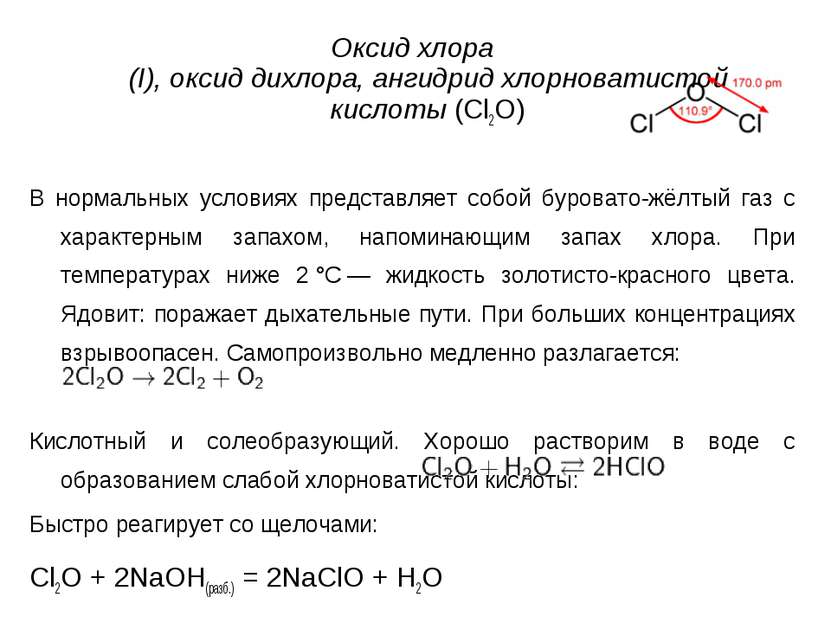
 Оксид хлора (I), оксид дихлора, ангидрид хлорноватистой кислоты (Cl2O) В нормальных условиях представляет собой буровато-жёлтый газ с характерным запахом, напоминающим запах хлора. При температурах ниже 2 °C — жидкость золотисто-красного цвета. Ядовит: поражает дыхательные пути. При больших концентрациях взрывоопасен. Самопроизвольно медленно разлагается: Кислотный и солеобразующий. Хорошо растворим в воде с образованием слабой хлорноватистой кислоты: Быстро реагирует со щелочами: Cl2O + 2NaOH(разб.) = 2NaClO + H2O
Оксид хлора (I), оксид дихлора, ангидрид хлорноватистой кислоты (Cl2O) В нормальных условиях представляет собой буровато-жёлтый газ с характерным запахом, напоминающим запах хлора. При температурах ниже 2 °C — жидкость золотисто-красного цвета. Ядовит: поражает дыхательные пути. При больших концентрациях взрывоопасен. Самопроизвольно медленно разлагается: Кислотный и солеобразующий. Хорошо растворим в воде с образованием слабой хлорноватистой кислоты: Быстро реагирует со щелочами: Cl2O + 2NaOH(разб.) = 2NaClO + H2O
Cлайд 24
 Диоксид хлора, оксид хлора (IV), (ClO2) В нормальных условиях газ красновато-жёлтого цвета, с характерным запахом. При температурах ниже 10 °C ClO2 представляет собой жидкость красно-коричневого цвета. Малоустойчив, взрывается на свету. Кислотный оксид. При растворении в воде образуются хлористая и хлорноватая кислоты (реакция диспропорционирования). Разбавленные растворы на свету медленно разлагаются:
Диоксид хлора, оксид хлора (IV), (ClO2) В нормальных условиях газ красновато-жёлтого цвета, с характерным запахом. При температурах ниже 10 °C ClO2 представляет собой жидкость красно-коричневого цвета. Малоустойчив, взрывается на свету. Кислотный оксид. При растворении в воде образуются хлористая и хлорноватая кислоты (реакция диспропорционирования). Разбавленные растворы на свету медленно разлагаются:
Cлайд 25
 Проявляет окислительно-восстановительные свойства. 2ClO2 + 5H2SO4 (разб.) + 10FeSO4 = 5Fe2(SO4)3 + 2HCl + 4H2O ClO2 + O3 = ClO3 + O2 ClO2 + 2NaOHхол. = NaClO2 + NaClO3 + H2O ClO2 реагирует со многими с органическими соединениями и выступает окислителем средней силы. Выгодным считается обеззараживание воды при помощи диоксида хлора. Но в наши дни этот метод практически не применяется.
Проявляет окислительно-восстановительные свойства. 2ClO2 + 5H2SO4 (разб.) + 10FeSO4 = 5Fe2(SO4)3 + 2HCl + 4H2O ClO2 + O3 = ClO3 + O2 ClO2 + 2NaOHхол. = NaClO2 + NaClO3 + H2O ClO2 реагирует со многими с органическими соединениями и выступает окислителем средней силы. Выгодным считается обеззараживание воды при помощи диоксида хлора. Но в наши дни этот метод практически не применяется.
Cлайд 26
 Хлорноватистая кислота (HClO) Очень слабая одноосновная кислота, в которой хлор имеет степень окисления +1. Существует лишь в растворах. В водных растворах хлорноватистая кислота частично распадается на протон и гипохлорит-анион ClO−: Неустойчива. Хлорноватистая кислота и её соли — гипохлориты — сильные окислители. Реагирует с соляной кислотой HCl, образуя молекулярный хлор: HClO + NaOH (разб.) = NaClO + H2O
Хлорноватистая кислота (HClO) Очень слабая одноосновная кислота, в которой хлор имеет степень окисления +1. Существует лишь в растворах. В водных растворах хлорноватистая кислота частично распадается на протон и гипохлорит-анион ClO−: Неустойчива. Хлорноватистая кислота и её соли — гипохлориты — сильные окислители. Реагирует с соляной кислотой HCl, образуя молекулярный хлор: HClO + NaOH (разб.) = NaClO + H2O
Cлайд 27
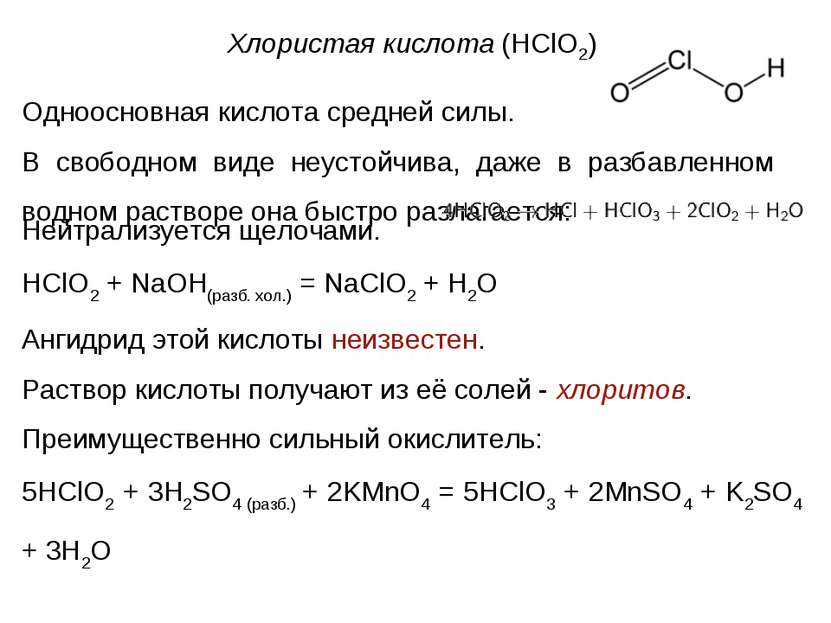
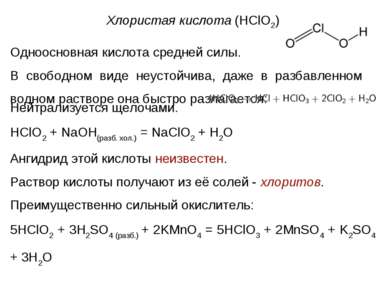 Хлористая кислота (HClO2) Одноосновная кислота средней силы. В свободном виде неустойчива, даже в разбавленном водном растворе она быстро разлагается: Нейтрализуется щелочами. HClO2 + NaOH(разб. хол.) = NaClO2 + H2O Ангидрид этой кислоты неизвестен. Раствор кислоты получают из её солей - хлоритов. Преимущественно сильный окислитель: 5HClO2 + 3H2SO4 (разб.) + 2KMnO4 = 5HClO3 + 2MnSO4 + K2SO4 + 3H2O
Хлористая кислота (HClO2) Одноосновная кислота средней силы. В свободном виде неустойчива, даже в разбавленном водном растворе она быстро разлагается: Нейтрализуется щелочами. HClO2 + NaOH(разб. хол.) = NaClO2 + H2O Ангидрид этой кислоты неизвестен. Раствор кислоты получают из её солей - хлоритов. Преимущественно сильный окислитель: 5HClO2 + 3H2SO4 (разб.) + 2KMnO4 = 5HClO3 + 2MnSO4 + K2SO4 + 3H2O
Cлайд 28
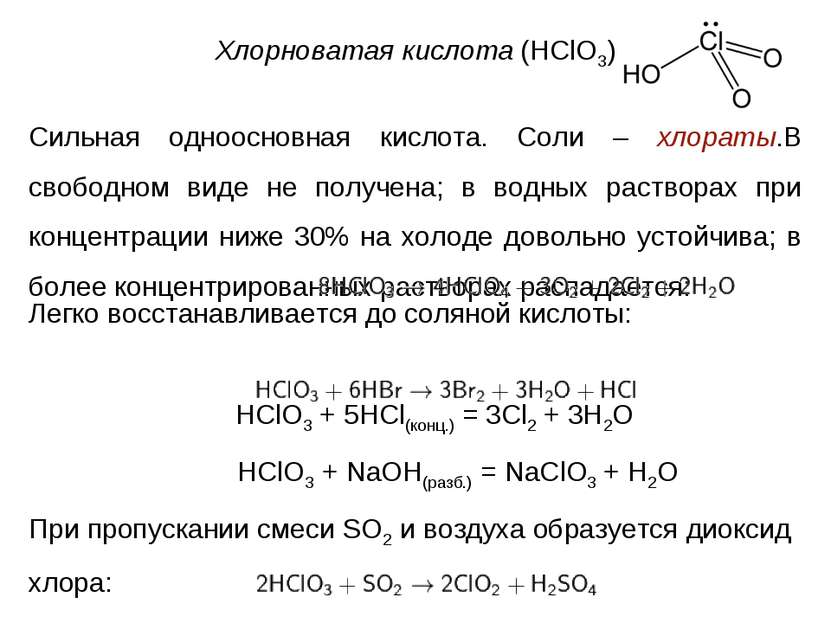
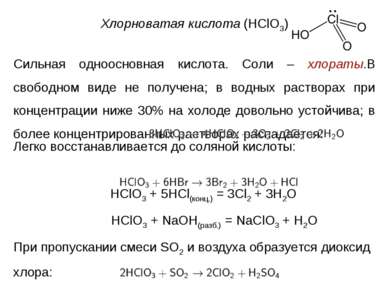 Хлорноватая кислота (HClO3) Сильная одноосновная кислота. Соли – хлораты.В свободном виде не получена; в водных растворах при концентрации ниже 30% на холоде довольно устойчива; в более концентрированных растворах распадается: Легко восстанавливается до соляной кислоты: HClO3 + 5HCl(конц.) = 3Cl2 + 3H2O HClO3 + NaOH(разб.) = NaClO3 + H2O При пропускании смеси SO2 и воздуха образуется диоксид хлора:
Хлорноватая кислота (HClO3) Сильная одноосновная кислота. Соли – хлораты.В свободном виде не получена; в водных растворах при концентрации ниже 30% на холоде довольно устойчива; в более концентрированных растворах распадается: Легко восстанавливается до соляной кислоты: HClO3 + 5HCl(конц.) = 3Cl2 + 3H2O HClO3 + NaOH(разб.) = NaClO3 + H2O При пропускании смеси SO2 и воздуха образуется диоксид хлора:
Cлайд 29
 Получение Химические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение: Метод Шееле Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой:
Получение Химические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение: Метод Шееле Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой:
Cлайд 30
 Получение Метод Дикона Метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Электрохимические методы Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли, основные процессы которого можно представить суммарной формулой:
Получение Метод Дикона Метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Электрохимические методы Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли, основные процессы которого можно представить суммарной формулой:
Cлайд 33
 Физиологическое действие Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л (т.е. в два раза выше порога восприятия запаха хлора). ПДК хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
Физиологическое действие Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л (т.е. в два раза выше порога восприятия запаха хлора). ПДК хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
Cлайд 34
 Бром и его пары сильно токсичны. Уже при содержании брома в воздухе в концентрации около 0,001 % (по объёму) наблюдается раздражение слизистых оболочек, головокружение, носовые кровотечения, а при более высоких концентрациях — спазмы дыхательных путей, удушье. ПДК паров брома 0,5 мг/м³. Летальня доза для человека перорально составляет 14 мг/кг. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух. Для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Рекомендуется обильное питьё теплого молока с минеральной водой или содой, кофе. Жидкий бром при попадании на кожу вызывает болезненные и долго не заживающие ожоги.
Бром и его пары сильно токсичны. Уже при содержании брома в воздухе в концентрации около 0,001 % (по объёму) наблюдается раздражение слизистых оболочек, головокружение, носовые кровотечения, а при более высоких концентрациях — спазмы дыхательных путей, удушье. ПДК паров брома 0,5 мг/м³. Летальня доза для человека перорально составляет 14 мг/кг. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух. Для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Рекомендуется обильное питьё теплого молока с минеральной водой или содой, кофе. Жидкий бром при попадании на кожу вызывает болезненные и долго не заживающие ожоги.
Cлайд 35
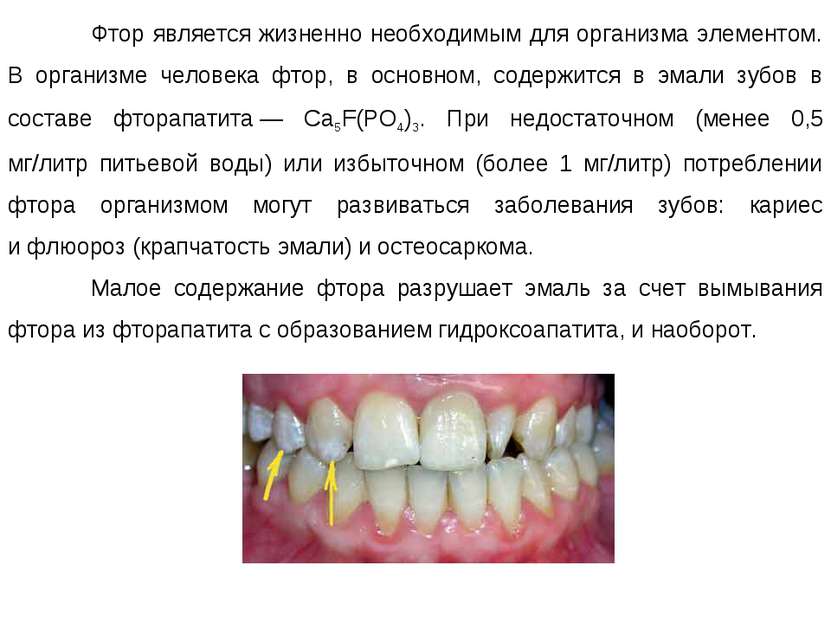
 Фтор является жизненно необходимым для организма элементом. В организме человека фтор, в основном, содержится в эмали зубов в составе фторапатита — Ca5F(PO4)3. При недостаточном (менее 0,5 мг/литр питьевой воды) или избыточном (более 1 мг/литр) потреблении фтора организмом могут развиваться заболевания зубов: кариес и флюороз (крапчатость эмали) и остеосаркома. Малое содержание фтора разрушает эмаль за счет вымывания фтора из фторапатита с образованием гидроксоапатита, и наоборот.
Фтор является жизненно необходимым для организма элементом. В организме человека фтор, в основном, содержится в эмали зубов в составе фторапатита — Ca5F(PO4)3. При недостаточном (менее 0,5 мг/литр питьевой воды) или избыточном (более 1 мг/литр) потреблении фтора организмом могут развиваться заболевания зубов: кариес и флюороз (крапчатость эмали) и остеосаркома. Малое содержание фтора разрушает эмаль за счет вымывания фтора из фторапатита с образованием гидроксоапатита, и наоборот.
Cлайд 36
 Астат. Будучи схожим по химическим свойствам с иодом, астат радиотоксичен. При попадании в организм концентрируется в печени. Как и иод, астат способен накапливаться в щитовидной железе. Альфа-излучение астата поражает близлежащие ткани, приводит к нарушению их функции и в перспективе — к образованию опухолей. Кроме того, частичное накопление астата наблюдается в молочных железах. Для профилактики кариеса рекомендуется использовать зубные пасты с добавками фторидов (натрия и/или олова) или употреблять фторированную воду (до концентрации 1 мг/л), или применять местные аппликации 1-2 % раствором фторида натрия или фторида олова. Такие действия могут сократить вероятность появления кариеса на 30-50% . Предельно допустимая концентрация связанного фтора в воздухе промышленных помещениях равна 0,0005 мг/литр воздуха.
Астат. Будучи схожим по химическим свойствам с иодом, астат радиотоксичен. При попадании в организм концентрируется в печени. Как и иод, астат способен накапливаться в щитовидной железе. Альфа-излучение астата поражает близлежащие ткани, приводит к нарушению их функции и в перспективе — к образованию опухолей. Кроме того, частичное накопление астата наблюдается в молочных железах. Для профилактики кариеса рекомендуется использовать зубные пасты с добавками фторидов (натрия и/или олова) или употреблять фторированную воду (до концентрации 1 мг/л), или применять местные аппликации 1-2 % раствором фторида натрия или фторида олова. Такие действия могут сократить вероятность появления кариеса на 30-50% . Предельно допустимая концентрация связанного фтора в воздухе промышленных помещениях равна 0,0005 мг/литр воздуха.