X
Код презентации скопируйте его
Аммиак состав, строение, свойства, применение
Скачать эту презентациюПрезентация на тему Аммиак состав, строение, свойства, применение
Скачать эту презентациюCлайд 1
 Аммиак: состав, строение, свойства, применение NH3 Лукуша Елена Фёдоровна, учитель химии МБОУ «Морская средняя школа» городского округа Судак, Республики Крым
Аммиак: состав, строение, свойства, применение NH3 Лукуша Елена Фёдоровна, учитель химии МБОУ «Морская средняя школа» городского округа Судак, Республики Крым
Cлайд 2
 Аммиак может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке караванных путей. В очень жарком климате мочевина (NH2)2CO, разлагается особенно быстро. Одним из основных продуктов разложения и является аммиак. Оазис «Аммон» в Северной Африке
Аммиак может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке караванных путей. В очень жарком климате мочевина (NH2)2CO, разлагается особенно быстро. Одним из основных продуктов разложения и является аммиак. Оазис «Аммон» в Северной Африке
Cлайд 3
 По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех верующих людей, поклоняющихся богу Амону. Люди во время своих ритуальных обрядов нюхали NH4Cl, который при нагревании издаёт запах аммиака. Бог Аммон в образе барана
По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех верующих людей, поклоняющихся богу Амону. Люди во время своих ритуальных обрядов нюхали NH4Cl, который при нагревании издаёт запах аммиака. Бог Аммон в образе барана
Cлайд 4
 Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый - химик, академик Яков Дмитриевич Захаров, который впервые разработал также и систему русской химической номенклатуры. 1781-1852 г.
Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый - химик, академик Яков Дмитриевич Захаров, который впервые разработал также и систему русской химической номенклатуры. 1781-1852 г.
Cлайд 6
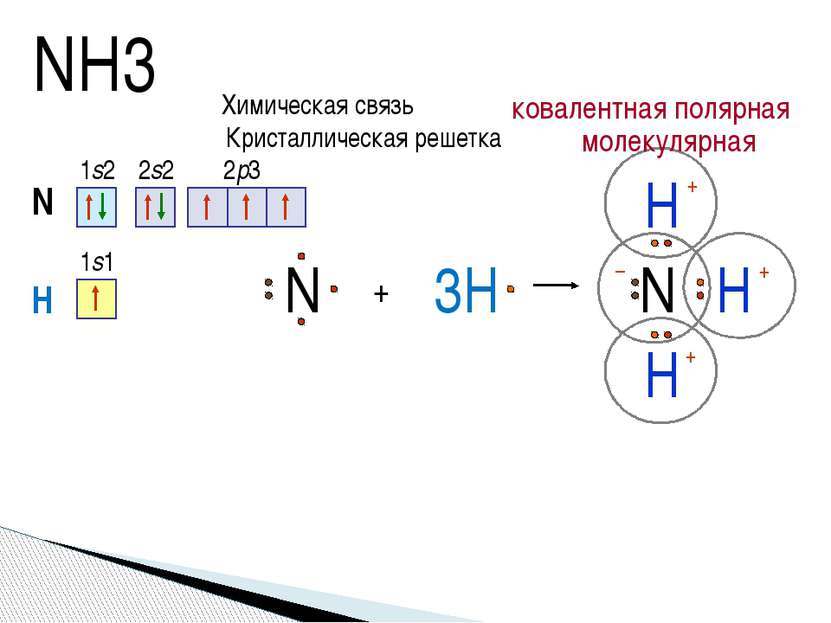
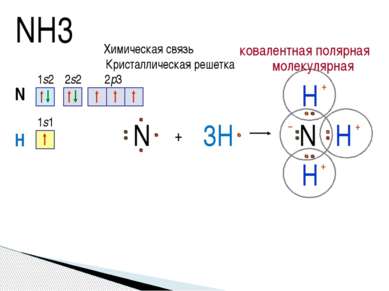 NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ +δ –δ Химическая связь ковалентная полярная Кристаллическая решетка молекулярная
NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ +δ –δ Химическая связь ковалентная полярная Кристаллическая решетка молекулярная
Cлайд 7
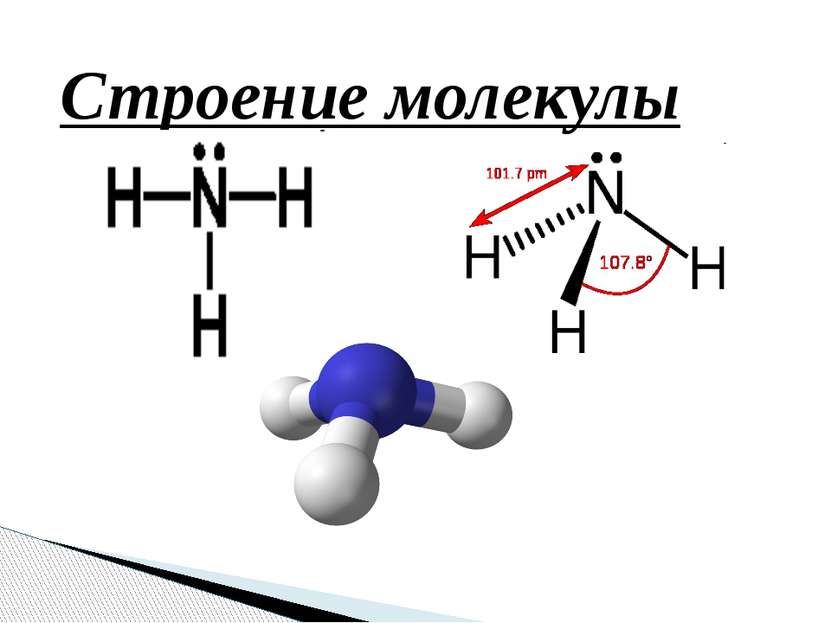
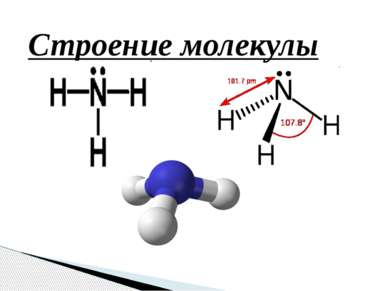
 Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота участвуют в образовании полярных ковалентных связей с 1s-электроном трёх атомов водорода (связи N−H), четвёртая пара внешних электронов является неподелённой, она может образовать донорно-акцепторную связь с ионом водорода, образуя ион аммония NH4+
Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота участвуют в образовании полярных ковалентных связей с 1s-электроном трёх атомов водорода (связи N−H), четвёртая пара внешних электронов является неподелённой, она может образовать донорно-акцепторную связь с ионом водорода, образуя ион аммония NH4+
Cлайд 8
 Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха (М=17 г/моль) хорошо растворяется в воде (1200 объёмов при 0 °C) и 700 объёмов (при 20 °C) в объёме воды температура плавления -77.73 °C температура кипения -33.34 °C ЯДОВИТ!
Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха (М=17 г/моль) хорошо растворяется в воде (1200 объёмов при 0 °C) и 700 объёмов (при 20 °C) в объёме воды температура плавления -77.73 °C температура кипения -33.34 °C ЯДОВИТ!
Cлайд 9
 По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы.
По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы.
Cлайд 10
 Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl + Ca(OH)2= 2NH3↑ + СaCl2+ 2H2O (NH4)2SO4 + 2NaOH = 2NH3↑ + Na2SO4 + 2H2O Гидроксид аммония неустойчивое основание, разлагается: NH4OH ↔ NH3↑ + H2O При получении аммиака держите пробирку - приёмник дном кверху, так как аммиак легче воздуха:
Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl + Ca(OH)2= 2NH3↑ + СaCl2+ 2H2O (NH4)2SO4 + 2NaOH = 2NH3↑ + Na2SO4 + 2H2O Гидроксид аммония неустойчивое основание, разлагается: NH4OH ↔ NH3↑ + H2O При получении аммиака держите пробирку - приёмник дном кверху, так как аммиак легче воздуха:
Cлайд 11
 Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г) + 45,9 кДж Условия: катализатор – пористое железо температура – 450 – 500 ˚С давление – 25 – 30 МПа Это так называемый процесс Габера (немецкий физик, разработал физико-химические основы метода).
Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г) + 45,9 кДж Условия: катализатор – пористое железо температура – 450 – 500 ˚С давление – 25 – 30 МПа Это так называемый процесс Габера (немецкий физик, разработал физико-химические основы метода).
Cлайд 12
 Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления); 2) без изменения степени окисления атома азота (присоединение).
Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления); 2) без изменения степени окисления атома азота (присоединение).
Cлайд 13
 Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0→ N+2 NH3-сильный восстановитель
Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0→ N+2 NH3-сильный восстановитель
Cлайд 14
 с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление амииака (катализатор Pt – Rh, температура) 4NH3 + 5O2 → 4NO + 6H2O
с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление амииака (катализатор Pt – Rh, температура) 4NH3 + 5O2 → 4NO + 6H2O
Cлайд 17
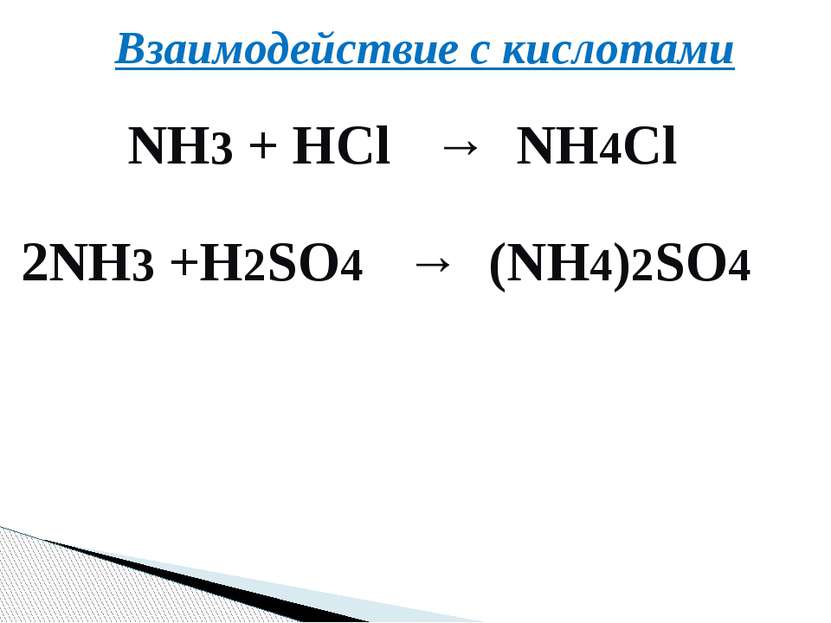
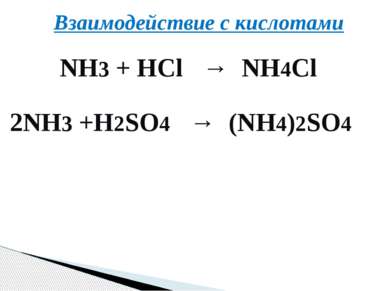
 Реакции без изменения степени окисления атома азота (присоединение - образование иона аммония NH4+ по донорно-акцепторному механизму
Реакции без изменения степени окисления атома азота (присоединение - образование иона аммония NH4+ по донорно-акцепторному механизму
Cлайд 19
 Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как при растворении аммиака частично образуется гидроксид аммония NH4OH.
Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как при растворении аммиака частично образуется гидроксид аммония NH4OH.