X
Код презентации скопируйте его
Реакции ионного обмена (9 класс)
Скачать эту презентациюПрезентация на тему Реакции ионного обмена (9 класс)
Скачать эту презентациюCлайд 1
 МБОУ «ИВАНЧИКОВСКАЯ СОШ» ЛЬГОВСКОГО РАЙОНА КУРСКОЙ ОБЛАСТИ конспект урока химии «Реакции ионного обмена» ( 2-я образовательная ступень) 9 класс Составила учитель химии Митина Валентина Тихоновна. 2015-2016 учебный год
МБОУ «ИВАНЧИКОВСКАЯ СОШ» ЛЬГОВСКОГО РАЙОНА КУРСКОЙ ОБЛАСТИ конспект урока химии «Реакции ионного обмена» ( 2-я образовательная ступень) 9 класс Составила учитель химии Митина Валентина Тихоновна. 2015-2016 учебный год
Cлайд 2
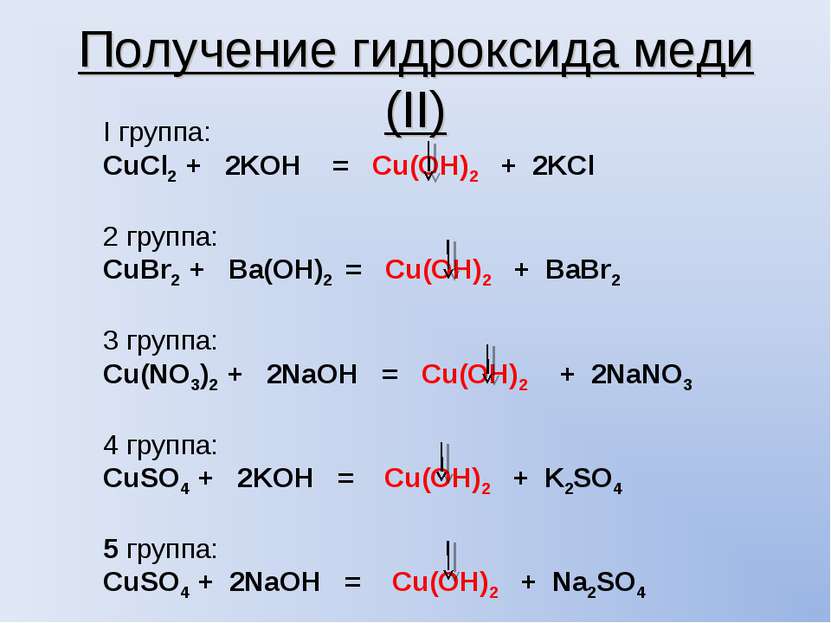
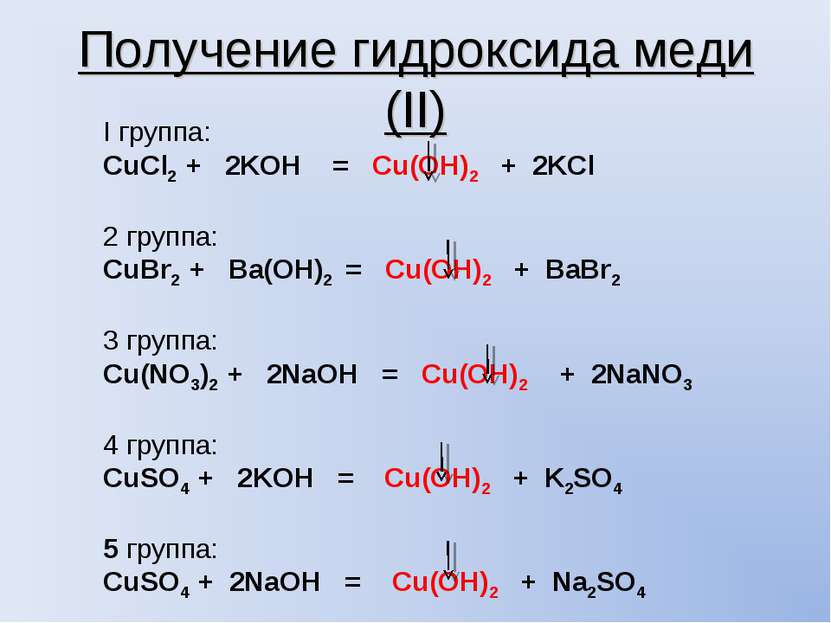
 Получение гидроксида меди (II) I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2 + Ba(OH)2 = Cu(OH)2 + BaBr2 3 группа: Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3 4 группа: CuSO4 + 2KOH = Cu(OH)2 + K2SO4 5 группа: CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Получение гидроксида меди (II) I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2 + Ba(OH)2 = Cu(OH)2 + BaBr2 3 группа: Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3 4 группа: CuSO4 + 2KOH = Cu(OH)2 + K2SO4 5 группа: CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Cлайд 5
 1) ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИИ В МОЛЕКУЛЯРНОЙ ФОРМЕ FeCI3 + 3NaOH = Fe(OH)3 + 3 NaCI 2) СОСТАВИТЬ ПОЛНОЕ ИОННОЕ УРАВНЕНИЕ Диссоциированные вещества записываются в виде ионов, а уходящие из среды реакции либо малодиссоциированные – в молекулярной форме Fe3+ + 3 CI- + 3Na+ + 3OH- = Fe(OH)3 + 3Na+ + 3CI- 3) ОПРЕДЕЛИТЬ ИОНЫ, НЕ ПРИНИМАЮЩИЕ УЧАСТИЕ В РЕАКЦИИ, ВЫЧЕРКНУТЬ ИХ Fe3+ + 3 CI- + 3Na+ + OH- = Fe(OH)3 + 3Na+ + 3CI- 4) СОСТАВИТЬ СОКРАЩЕННОЕ ИОННОЕ УРАВНЕНИЕ, ВЫРАЖАЮЩЕГО СУЩНОСТЬ РЕАКЦИИ Fe3+ + 3OH- = Fe(OH)3 АЛГОРИТМ СОСТАВЛЕНИЯ ИОННЫХ УРАВНЕНИЙ
1) ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИИ В МОЛЕКУЛЯРНОЙ ФОРМЕ FeCI3 + 3NaOH = Fe(OH)3 + 3 NaCI 2) СОСТАВИТЬ ПОЛНОЕ ИОННОЕ УРАВНЕНИЕ Диссоциированные вещества записываются в виде ионов, а уходящие из среды реакции либо малодиссоциированные – в молекулярной форме Fe3+ + 3 CI- + 3Na+ + 3OH- = Fe(OH)3 + 3Na+ + 3CI- 3) ОПРЕДЕЛИТЬ ИОНЫ, НЕ ПРИНИМАЮЩИЕ УЧАСТИЕ В РЕАКЦИИ, ВЫЧЕРКНУТЬ ИХ Fe3+ + 3 CI- + 3Na+ + OH- = Fe(OH)3 + 3Na+ + 3CI- 4) СОСТАВИТЬ СОКРАЩЕННОЕ ИОННОЕ УРАВНЕНИЕ, ВЫРАЖАЮЩЕГО СУЩНОСТЬ РЕАКЦИИ Fe3+ + 3OH- = Fe(OH)3 АЛГОРИТМ СОСТАВЛЕНИЯ ИОННЫХ УРАВНЕНИЙ
Cлайд 6
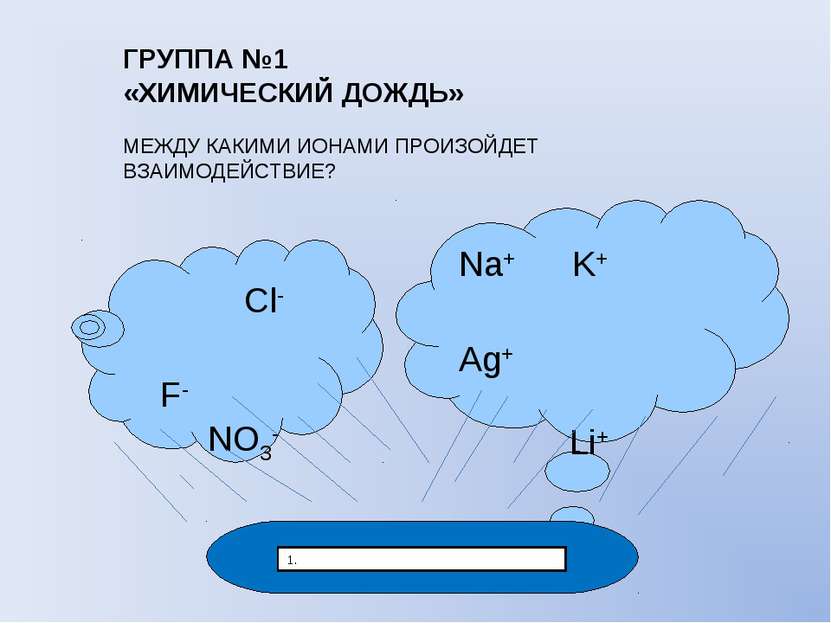
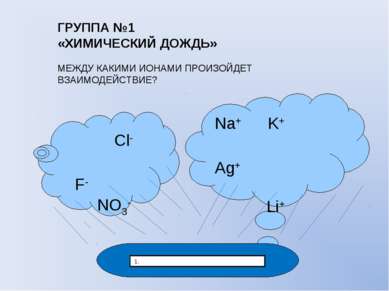 Cl- F- NO3- Na+ K+ Ag+ Li+ 1. ГРУППА №1 «ХИМИЧЕСКИЙ ДОЖДЬ» МЕЖДУ КАКИМИ ИОНАМИ ПРОИЗОЙДЕТ ВЗАИМОДЕЙСТВИЕ?
Cl- F- NO3- Na+ K+ Ag+ Li+ 1. ГРУППА №1 «ХИМИЧЕСКИЙ ДОЖДЬ» МЕЖДУ КАКИМИ ИОНАМИ ПРОИЗОЙДЕТ ВЗАИМОДЕЙСТВИЕ?
Cлайд 7
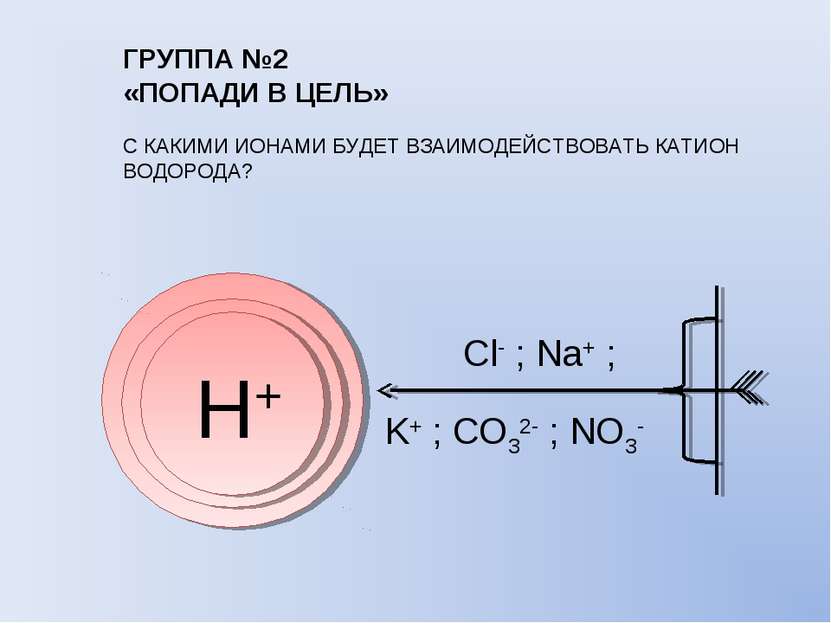
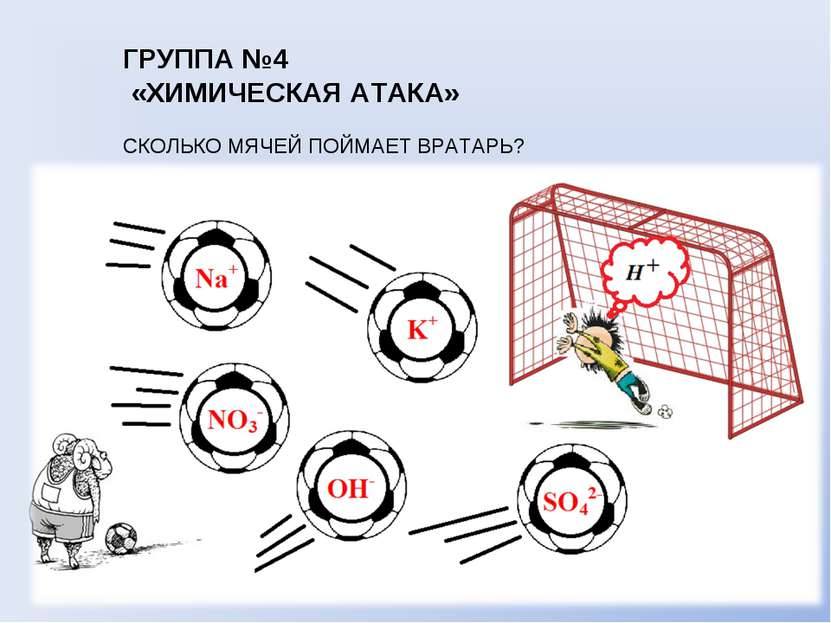
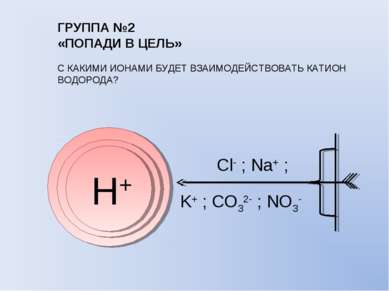 ГРУППА №2 «ПОПАДИ В ЦЕЛЬ» С КАКИМИ ИОНАМИ БУДЕТ ВЗАИМОДЕЙСТВОВАТЬ КАТИОН ВОДОРОДА? Н+ Cl- ; Na+ ; K+ ; CO32- ; NO3-
ГРУППА №2 «ПОПАДИ В ЦЕЛЬ» С КАКИМИ ИОНАМИ БУДЕТ ВЗАИМОДЕЙСТВОВАТЬ КАТИОН ВОДОРОДА? Н+ Cl- ; Na+ ; K+ ; CO32- ; NO3-
Cлайд 8
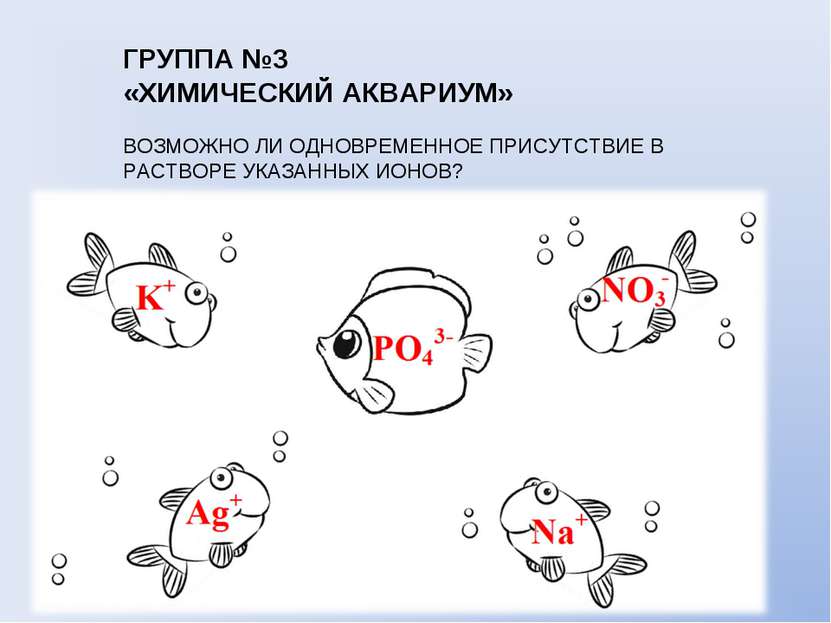
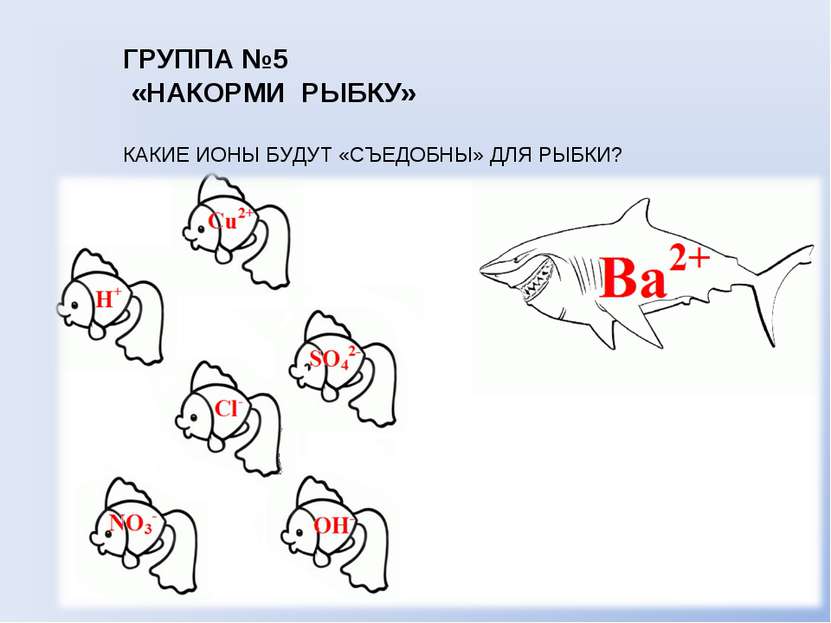
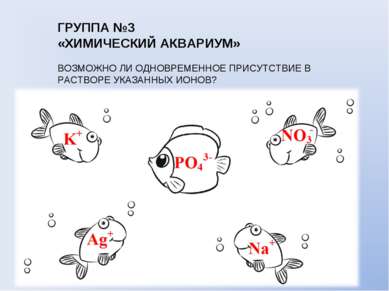 ГРУППА №3 «ХИМИЧЕСКИЙ АКВАРИУМ» ВОЗМОЖНО ЛИ ОДНОВРЕМЕННОЕ ПРИСУТСТВИЕ В РАСТВОРЕ УКАЗАННЫХ ИОНОВ?
ГРУППА №3 «ХИМИЧЕСКИЙ АКВАРИУМ» ВОЗМОЖНО ЛИ ОДНОВРЕМЕННОЕ ПРИСУТСТВИЕ В РАСТВОРЕ УКАЗАННЫХ ИОНОВ?
Cлайд 11
 ПРИЗНАКИ НЕОБРАТИМОСТИ РЕАКЦИЙ ИОННОГО ОБМЕНА ОБРАЗОВАНИЕ ОСАДКА Cu 2++ 2OH- = Cu(OH)2 ОБРАЗОВАНИЕ ГАЗООБРАЗНОГО ВЕЩЕСТВА CO32- + 2H+ = CO2 + H2O ОБРАЗОВАНИЕ МАЛОДИССОЦИИРОВАННОГО ВЕЩЕСТВА H+ + OH- = H2O
ПРИЗНАКИ НЕОБРАТИМОСТИ РЕАКЦИЙ ИОННОГО ОБМЕНА ОБРАЗОВАНИЕ ОСАДКА Cu 2++ 2OH- = Cu(OH)2 ОБРАЗОВАНИЕ ГАЗООБРАЗНОГО ВЕЩЕСТВА CO32- + 2H+ = CO2 + H2O ОБРАЗОВАНИЕ МАЛОДИССОЦИИРОВАННОГО ВЕЩЕСТВА H+ + OH- = H2O
Cлайд 12
 Получение гидроксида меди (II) I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2 + Ba(OH)2 = Cu(OH)2 + BaBr2 3 группа: Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3 4 группа: CuSO4 + 2KOH = Cu(OH)2 + K2SO4 5 группа: CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Получение гидроксида меди (II) I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2 + Ba(OH)2 = Cu(OH)2 + BaBr2 3 группа: Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3 4 группа: CuSO4 + 2KOH = Cu(OH)2 + K2SO4 5 группа: CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Cлайд 13
 Краткое ионное уравнение получения гидроксида меди (II) из растворов солей меди Cu 2++ 2OH- = Cu(OH)2
Краткое ионное уравнение получения гидроксида меди (II) из растворов солей меди Cu 2++ 2OH- = Cu(OH)2