X
Код презентации скопируйте его
Соли. Физические свойства солей.
Скачать эту презентациюПрезентация на тему Соли. Физические свойства солей.
Скачать эту презентациюCлайд 5
 Угадайте вещество Вещество, без которого невозможна жизнь растений, животных и человека. Это химическое соединение необходимо для существования в крови эритроцитов, сокращения мышц, переваривания пищи в желудке. В год каждый человек потребляет от 3 до 5 кг. этого вещества. 4. Это вещество- символ гостеприимства и радушия русской нации. Говорят, чтобы узнать человека, надо с ним пуд этого вещества съесть.
Угадайте вещество Вещество, без которого невозможна жизнь растений, животных и человека. Это химическое соединение необходимо для существования в крови эритроцитов, сокращения мышц, переваривания пищи в желудке. В год каждый человек потребляет от 3 до 5 кг. этого вещества. 4. Это вещество- символ гостеприимства и радушия русской нации. Говорят, чтобы узнать человека, надо с ним пуд этого вещества съесть.
Cлайд 7
 Состав солей NaCl K2S MgSO4 Соли –это сложные или простые вещества? Проанализируйте состав солей. Можно ли считать эти вещества производными кислот и оснований? Сформулируйте определение данного класса соединений.
Состав солей NaCl K2S MgSO4 Соли –это сложные или простые вещества? Проанализируйте состав солей. Можно ли считать эти вещества производными кислот и оснований? Сформулируйте определение данного класса соединений.
Cлайд 8
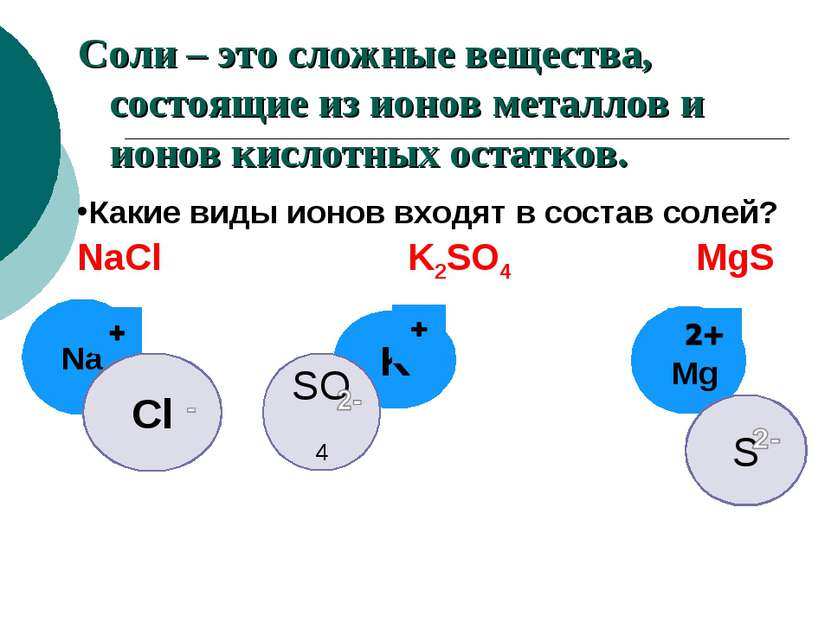
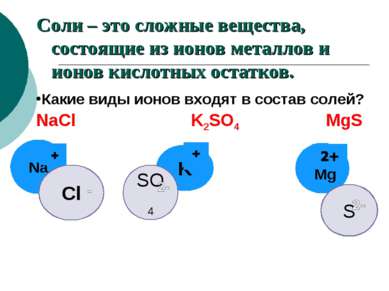 Соли – это сложные вещества, состоящие из ионов металлов и ионов кислотных остатков. NaCl K2SO4 MgS Какие виды ионов входят в состав солей? Mg
Соли – это сложные вещества, состоящие из ионов металлов и ионов кислотных остатков. NaCl K2SO4 MgS Какие виды ионов входят в состав солей? Mg
Cлайд 9
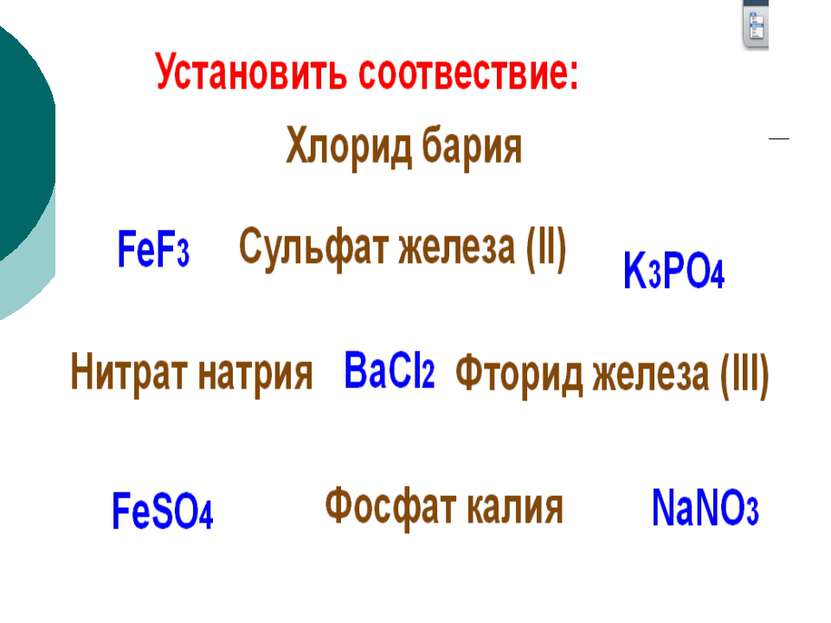
 Алгоритм (№1) называния соли по формуле Определить название кислотного остатка. К названию соли добавить русское название металла в родительном падеже, указать в скобках римской цифрой степень окисления металла (если она непостоянна). Название соли = название кислотного ост-ка + название металла (в родительном падеже) + с. о. металла(если она непостоянна).
Алгоритм (№1) называния соли по формуле Определить название кислотного остатка. К названию соли добавить русское название металла в родительном падеже, указать в скобках римской цифрой степень окисления металла (если она непостоянна). Название соли = название кислотного ост-ка + название металла (в родительном падеже) + с. о. металла(если она непостоянна).
Cлайд 10
 Названия солей ион кислотного остатка (в именительном падеже) с суффиксами: – ид для безкислородной соли; -ат для высшей степени окисления неметалла; -ит для низшей степени окисления неметалла; Al2S3 – сульфид алюминия FeBr2 – бромид железа (II) FeBr3 – бромид железа (III) Na2S+6O4– сульфат натрия Na2S+4O3 - сульфит натрия Fe+2 (N+3O2)2 – нитрит железа (II) Fe +3 (N+5O3) 3 – нитрат железа (III)
Названия солей ион кислотного остатка (в именительном падеже) с суффиксами: – ид для безкислородной соли; -ат для высшей степени окисления неметалла; -ит для низшей степени окисления неметалла; Al2S3 – сульфид алюминия FeBr2 – бромид железа (II) FeBr3 – бромид железа (III) Na2S+6O4– сульфат натрия Na2S+4O3 - сульфит натрия Fe+2 (N+3O2)2 – нитрит железа (II) Fe +3 (N+5O3) 3 – нитрат железа (III)
Cлайд 13
 Составление формулы соли 1. Записать химические знаки металла и кислотного остатка, указать их заряды Сa2+ PO43- 2. Найти наименьшее общее кратное значений зарядов Сa2+ PO43- 2*3 = 6 3. Разделить полученное число: а) на заряд металла и записать индекс справа внизу от знака металла; б) на заряд кислотного остатка и записать индекс кислотного остатка 2*3 = 6 6 : 2 = 3 (индекс) Сa2+3 PO43- 6 : 3 = 2 (индекс) Сa2+3(PO43-)2 4. Проверка: произведение значения заряда металла на его индекс должно быть равно аналогичному произведению кислотного остатка Сa2+3(PO43-)2 (2+) ∙ 3 = 6+ (3 -) ∙ 2 = 6 – (6 +) + (6-)= 0 Порядок действий Пример *
Составление формулы соли 1. Записать химические знаки металла и кислотного остатка, указать их заряды Сa2+ PO43- 2. Найти наименьшее общее кратное значений зарядов Сa2+ PO43- 2*3 = 6 3. Разделить полученное число: а) на заряд металла и записать индекс справа внизу от знака металла; б) на заряд кислотного остатка и записать индекс кислотного остатка 2*3 = 6 6 : 2 = 3 (индекс) Сa2+3 PO43- 6 : 3 = 2 (индекс) Сa2+3(PO43-)2 4. Проверка: произведение значения заряда металла на его индекс должно быть равно аналогичному произведению кислотного остатка Сa2+3(PO43-)2 (2+) ∙ 3 = 6+ (3 -) ∙ 2 = 6 – (6 +) + (6-)= 0 Порядок действий Пример *
Cлайд 14
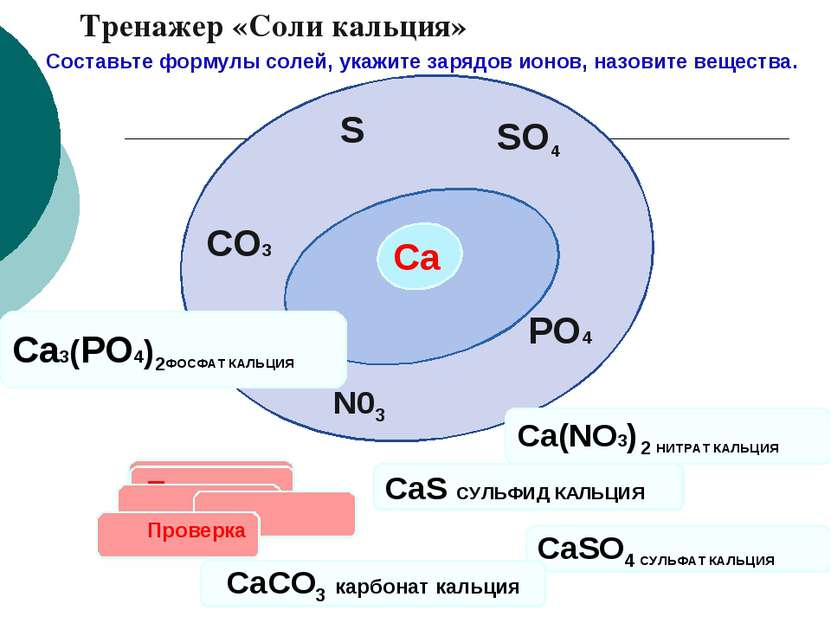
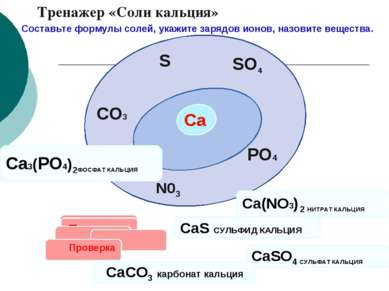 Са SO4 N03 PO4 S CO3 Проверка CaS СУЛЬФИД КАЛЬЦИЯ CaSO4 СУЛЬФАТ КАЛЬЦИЯ Проверка Са3(PO4)2ФОСФАТ КАЛЬЦИЯ Ca(NO3) 2 НИТРАТ КАЛЬЦИЯ CaCO3 карбонат кальция Тренажер «Соли кальция» Составьте формулы солей, укажите зарядов ионов, назовите вещества. Проверка
Са SO4 N03 PO4 S CO3 Проверка CaS СУЛЬФИД КАЛЬЦИЯ CaSO4 СУЛЬФАТ КАЛЬЦИЯ Проверка Са3(PO4)2ФОСФАТ КАЛЬЦИЯ Ca(NO3) 2 НИТРАТ КАЛЬЦИЯ CaCO3 карбонат кальция Тренажер «Соли кальция» Составьте формулы солей, укажите зарядов ионов, назовите вещества. Проверка
Cлайд 16
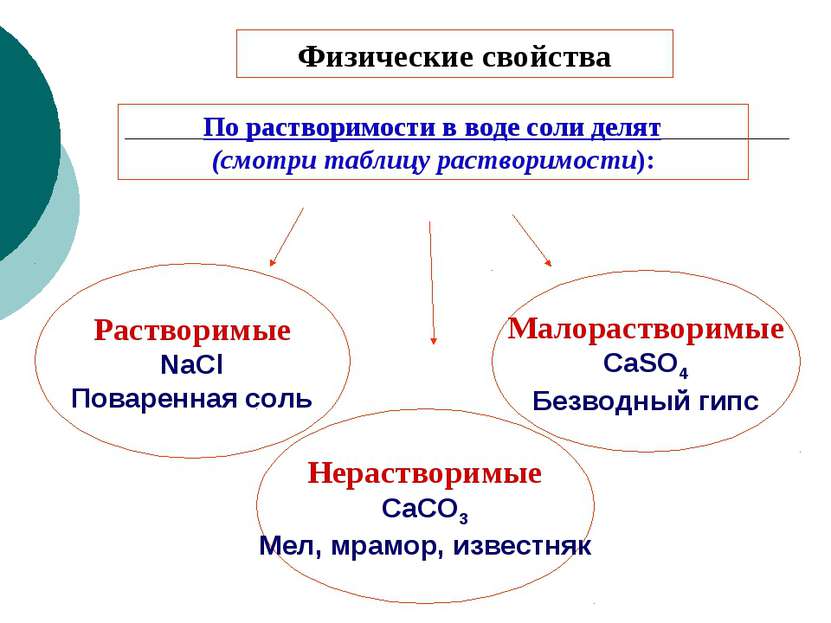
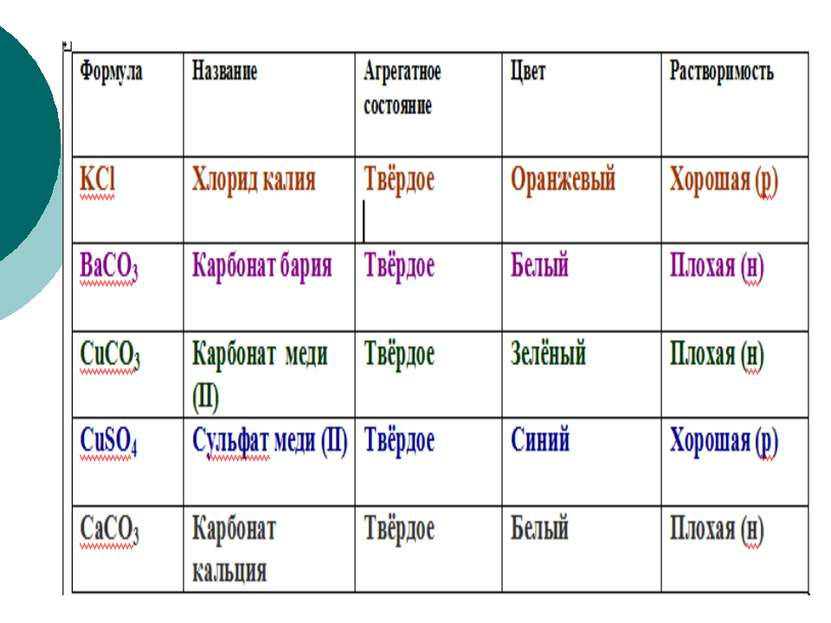
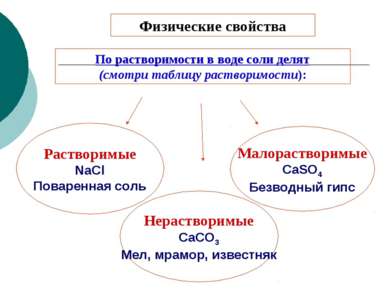 Физические свойства Растворимые NaCl Поваренная соль По растворимости в воде соли делят (смотри таблицу растворимости): Нерастворимые CaCO3 Мел, мрамор, известняк Малорастворимые CaSO4 Безводный гипс
Физические свойства Растворимые NaCl Поваренная соль По растворимости в воде соли делят (смотри таблицу растворимости): Нерастворимые CaCO3 Мел, мрамор, известняк Малорастворимые CaSO4 Безводный гипс