X
Код презентации скопируйте его
Виды химической связи (11 класс)
Скачать эту презентациюПрезентация на тему Виды химической связи (11 класс)
Скачать эту презентациюCлайд 2
 Химическая связь – это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.
Химическая связь – это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.
Cлайд 3
 это связь, возникающая между атомами за счет образования общих электронных пар. По степени смещенности общих электронных пар к одному из связанных ими атомов ковалентная связь может быть полярной и неполярной.
это связь, возникающая между атомами за счет образования общих электронных пар. По степени смещенности общих электронных пар к одному из связанных ими атомов ковалентная связь может быть полярной и неполярной.
Cлайд 4
 КНС образуют атомы одного и того же химического элемента. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому наружные неспаренные электроны. Образуются общие электронные пары. Электронная пара принадлежит в равной мере обоим атомам. Примеры образования КНС: H . + . H H : H H-H H2 .. .. .. .. : F . + . F : : F : F : F-F F2 .. .. .. .. . . : O : + : O : : O :: O : O=O O2 . . .. ..
КНС образуют атомы одного и того же химического элемента. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому наружные неспаренные электроны. Образуются общие электронные пары. Электронная пара принадлежит в равной мере обоим атомам. Примеры образования КНС: H . + . H H : H H-H H2 .. .. .. .. : F . + . F : : F : F : F-F F2 .. .. .. .. . . : O : + : O : : O :: O : O=O O2 . . .. ..
Cлайд 5
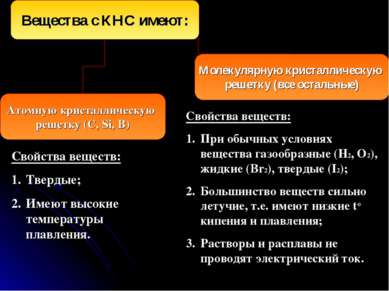 Свойства веществ: Твердые; Имеют высокие температуры плавления. Свойства веществ: При обычных условиях вещества газообразные (H2, O2), жидкие (Br2), твердые (I2); Большинство веществ сильно летучие, т.е. имеют низкие to кипения и плавления; Растворы и расплавы не проводят электрический ток.
Свойства веществ: Твердые; Имеют высокие температуры плавления. Свойства веществ: При обычных условиях вещества газообразные (H2, O2), жидкие (Br2), твердые (I2); Большинство веществ сильно летучие, т.е. имеют низкие to кипения и плавления; Растворы и расплавы не проводят электрический ток.
Cлайд 6
 КПС образуют атомы разных неметаллов (с разной электороотрицательностью). Электроотрицательность (ЭО)- это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов. Самый электроотрицательный элемент – F. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому свои наружные неспаренные электроны. Образуются общие электронные пары. Общая электронная пара смещена к более электроотрицательному элементу. Примеры образования связи. .. .. + - H + . Cl H . Cl : H Cl + - Диполь .. ..
КПС образуют атомы разных неметаллов (с разной электороотрицательностью). Электроотрицательность (ЭО)- это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов. Самый электроотрицательный элемент – F. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому свои наружные неспаренные электроны. Образуются общие электронные пары. Общая электронная пара смещена к более электроотрицательному элементу. Примеры образования связи. .. .. + - H + . Cl H . Cl : H Cl + - Диполь .. ..
Cлайд 7
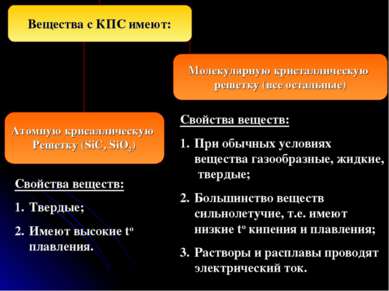 Свойства веществ: При обычных условиях вещества газообразные, жидкие, твердые; Большинство веществ сильнолетучие, т.е. имеют низкие to кипения и плавления; Растворы и расплавы проводят электрический ток. Свойства веществ: Твердые; Имеют высокие to плавления.
Свойства веществ: При обычных условиях вещества газообразные, жидкие, твердые; Большинство веществ сильнолетучие, т.е. имеют низкие to кипения и плавления; Растворы и расплавы проводят электрический ток. Свойства веществ: Твердые; Имеют высокие to плавления.
Cлайд 8
 ИС образуется между атомами металлов и неметаллов, т.е. между атомами резко отличающимися друг от друга по электроотрицательности. Механизм образования связи. Атом неметалла забирает наружные электроны у атома металла и превращается в анион (отрицательно заряженный ион). Атом металла теряет электроны и превращается в катион (положительно заряженный ион). Ионы связаны электростатическими силами. Пример образования связи. .. .. Na + . Cl : [ Na ] + [ . Cl : ]- или Na+ Cl- .. ..
ИС образуется между атомами металлов и неметаллов, т.е. между атомами резко отличающимися друг от друга по электроотрицательности. Механизм образования связи. Атом неметалла забирает наружные электроны у атома металла и превращается в анион (отрицательно заряженный ион). Атом металла теряет электроны и превращается в катион (положительно заряженный ион). Ионы связаны электростатическими силами. Пример образования связи. .. .. Na + . Cl : [ Na ] + [ . Cl : ]- или Na+ Cl- .. ..
Cлайд 9
 Свойства веществ: Все вещества при обычных условиях твердые. Имеют высокие температуры кипения и плавления. Расплавы и растворы проводят электрический ток.
Свойства веществ: Все вещества при обычных условиях твердые. Имеют высокие температуры кипения и плавления. Расплавы и растворы проводят электрический ток.
Cлайд 10
 Металлическая связь – связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке. Схема образования металлической связи (М – металл): _ М0 – ne M n+ Свойства веществ: Твердость, ковкость, электрическая проводимость и теплопроводность, ковкость, пластичность, металлический блеск.
Металлическая связь – связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке. Схема образования металлической связи (М – металл): _ М0 – ne M n+ Свойства веществ: Твердость, ковкость, электрическая проводимость и теплопроводность, ковкость, пластичность, металлический блеск.