X
Код презентации скопируйте его
Хламидии
Скачать эту презентациюПрезентация на тему Хламидии
Скачать эту презентациюCлайд 2
 Ошибки на этапе диагностики Не устанавливается топический диагноз - 87% Диагноз хламидийной инфекции устанавливается на основании ТОЛЬКО серологических методов - 21-45% При осложненных процессах урогенитального тракта (ВЗОМТ/эпидидимоорхит) не проводится исследование на хламидии – 91% Не проводится обследование на другие ИППП – 24-89%
Ошибки на этапе диагностики Не устанавливается топический диагноз - 87% Диагноз хламидийной инфекции устанавливается на основании ТОЛЬКО серологических методов - 21-45% При осложненных процессах урогенитального тракта (ВЗОМТ/эпидидимоорхит) не проводится исследование на хламидии – 91% Не проводится обследование на другие ИППП – 24-89%
Cлайд 3
 Этап диагностики Использование методов лабораторной диагностики, не дающих возможности установить верный диагноз – ПИФ, серология и новые несертифицированные методы диагностики Недообследование пациентов в тех клинических ситуациях, когда это требуется – недостаток методических материалов или отсутствие контроля за их исполнением
Этап диагностики Использование методов лабораторной диагностики, не дающих возможности установить верный диагноз – ПИФ, серология и новые несертифицированные методы диагностики Недообследование пациентов в тех клинических ситуациях, когда это требуется – недостаток методических материалов или отсутствие контроля за их исполнением
Cлайд 7
 ДИАГНОСТИКА Верификация диагноза базируется на результатах лабораторных исследований с помощью одного из методов: - молекулярно биологических; - выделения в культуре клеток. Другие методы лабораторных исследований, в том числе прямая иммунофлюоресценция (ПИФ), иммуноферментный анализ (ИФА) для обнаружения антител к C.trachomatis, микроскопический и морфологический методы НЕДОПУСТИМО использовать для диагностки хламидийной инфекции !!! С позиций доказательной медицины применение биологических, химических и алиментарных провокаций с целью повышения эффективности диагностики хламидийной инфекции нецелесообразно. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
ДИАГНОСТИКА Верификация диагноза базируется на результатах лабораторных исследований с помощью одного из методов: - молекулярно биологических; - выделения в культуре клеток. Другие методы лабораторных исследований, в том числе прямая иммунофлюоресценция (ПИФ), иммуноферментный анализ (ИФА) для обнаружения антител к C.trachomatis, микроскопический и морфологический методы НЕДОПУСТИМО использовать для диагностки хламидийной инфекции !!! С позиций доказательной медицины применение биологических, химических и алиментарных провокаций с целью повышения эффективности диагностики хламидийной инфекции нецелесообразно. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 11
 КРАТНОСТЬ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ: ДО НАЧАЛА ЛЕЧЕНИЯ ПОСЛЕ ОКОНЧАНИЯ ЛЕЧЕНИЯ : - ЧЕРЕЗ 14 дней – на основании культурального метода исследования и методов амплификации РНК (NASBA) - НЕ РАНЕЕ ЧЕМ ЧЕРЕЗ МЕСЯЦ – на основании методов амплификации ДНК (ПЦР, ПЦР-RТ)
КРАТНОСТЬ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ: ДО НАЧАЛА ЛЕЧЕНИЯ ПОСЛЕ ОКОНЧАНИЯ ЛЕЧЕНИЯ : - ЧЕРЕЗ 14 дней – на основании культурального метода исследования и методов амплификации РНК (NASBA) - НЕ РАНЕЕ ЧЕМ ЧЕРЕЗ МЕСЯЦ – на основании методов амплификации ДНК (ПЦР, ПЦР-RТ)
Cлайд 12
 Ошибки на этапе лечения Превышение разовых и курсовых доз антибактериальных препаратов – 87% Назначаются препараты, в спектре действия которых (согласно инструкции) не указаны хламидии – 23% Проводятся несколько (повторные) курсов антибактериальной терапии – 92%
Ошибки на этапе лечения Превышение разовых и курсовых доз антибактериальных препаратов – 87% Назначаются препараты, в спектре действия которых (согласно инструкции) не указаны хламидии – 23% Проводятся несколько (повторные) курсов антибактериальной терапии – 92%
Cлайд 13
 Ошибки на этапе лечения При лечении осложнений (ВЗОМТ/эпидидимит) – не включаются антибактериальные препараты, способные перекрыть спектром действия C. trachomatis – 42% Применение - иммуномодуляторов – 97%; - провокации – 39%; - физиотерапии (без показаний) – 67%
Ошибки на этапе лечения При лечении осложнений (ВЗОМТ/эпидидимит) – не включаются антибактериальные препараты, способные перекрыть спектром действия C. trachomatis – 42% Применение - иммуномодуляторов – 97%; - провокации – 39%; - физиотерапии (без показаний) – 67%
Cлайд 14
 Этап лечения Выбор препарата, дозировки и продолжительности терапии Использование сочетаний препаратов, не оправданных с точки зрения доказательной медицины
Этап лечения Выбор препарата, дозировки и продолжительности терапии Использование сочетаний препаратов, не оправданных с точки зрения доказательной медицины
Cлайд 15
 ЛЕЧЕНИЕ Показания к проведению лечения Показанием к проведению лечения является идентификация C. trachomatis с помощью молекулярно-биологических методов или культурального метода у пациента либо у его полового партнера. Одновременное лечение половых партнеров является обязательным. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
ЛЕЧЕНИЕ Показания к проведению лечения Показанием к проведению лечения является идентификация C. trachomatis с помощью молекулярно-биологических методов или культурального метода у пациента либо у его полового партнера. Одновременное лечение половых партнеров является обязательным. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 16
 Общие замечания по фармакотерапии Выбор препаратов проводится с учетом анамнестических данных (аллергические реакции, индивидуальная непереносимость препаратов, наличие сопутствующих инфекций). Лечение беременных, больных хламидийной инфекцией, осуществляется на любом сроке беременности антибактериальными препаратами с учетом их влияния на плод при участии акушер-гинекологов. Лечение новорожденных, родившихся от матерей, больных хламидийной инфекцией, проводится при участии неонатологов. Лечение хламидийной инфекции у детей с массой тела более 45 кг проводится в соответствии со схемами назначения у взрослых с учетом противопоказаний. С позиций доказательной медицины проведение дополнительной терапии (системной энзимотерапии, иммуномодулирующей, местными антисептическими препаратами) не рекомендовано. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Общие замечания по фармакотерапии Выбор препаратов проводится с учетом анамнестических данных (аллергические реакции, индивидуальная непереносимость препаратов, наличие сопутствующих инфекций). Лечение беременных, больных хламидийной инфекцией, осуществляется на любом сроке беременности антибактериальными препаратами с учетом их влияния на плод при участии акушер-гинекологов. Лечение новорожденных, родившихся от матерей, больных хламидийной инфекцией, проводится при участии неонатологов. Лечение хламидийной инфекции у детей с массой тела более 45 кг проводится в соответствии со схемами назначения у взрослых с учетом противопоказаний. С позиций доказательной медицины проведение дополнительной терапии (системной энзимотерапии, иммуномодулирующей, местными антисептическими препаратами) не рекомендовано. Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 18
 Естественное течение неосложнённой C. trachomatis инфекции Длительное бессимптомное/малосимптомное течение Спонтанное разрешение в 20%1-4 Возможность развития, при хронизации, защитного иммунитета1,5 (лимфоциты Th-2, секретирующие IL-4) Развитие осложнений - риск развития ВЗОМТ ≈ 1%6 Особенности эффективно пролеченной АБ инфекции: Реинфекция в течение 1 года - от 4-5%7 до 10-20%1 1Geisler WM, et al. JID 2013; 207:1850-6; 2Geisler WM, et al. STD 2008; 35:119–23 3Joyner JL, et al. STD 2002; 29:196–200; 4Rogers SM, et al. STD 2008; 84:23–8; 5Morrison RP, et al. Infect Immun 2002; 70:2741–51; 6Paavonen J. Ann Med 2012; 44(1):18-28; 7Wikstrom E, et al. STD 2012; 39:968-72
Естественное течение неосложнённой C. trachomatis инфекции Длительное бессимптомное/малосимптомное течение Спонтанное разрешение в 20%1-4 Возможность развития, при хронизации, защитного иммунитета1,5 (лимфоциты Th-2, секретирующие IL-4) Развитие осложнений - риск развития ВЗОМТ ≈ 1%6 Особенности эффективно пролеченной АБ инфекции: Реинфекция в течение 1 года - от 4-5%7 до 10-20%1 1Geisler WM, et al. JID 2013; 207:1850-6; 2Geisler WM, et al. STD 2008; 35:119–23 3Joyner JL, et al. STD 2002; 29:196–200; 4Rogers SM, et al. STD 2008; 84:23–8; 5Morrison RP, et al. Infect Immun 2002; 70:2741–51; 6Paavonen J. Ann Med 2012; 44(1):18-28; 7Wikstrom E, et al. STD 2012; 39:968-72
Cлайд 19
 Доказательство спонтанного разрешения неосложнённой C. trachomatis инфекции 1Geisler WM, et al. JID 2013; 207:1850-6 Через 15 сут. (6–47) Через 183 сут. (35-365) Скрининг: Осмотр, НАСБА N=245, 22 (16–54) лет; BV 31% Визит 2, N=200. Осмотр, НАСБА Осмотр, НАСБА. Начало лечения. У 22% - спонтанное разрешение (Гр-1) - нет АТ Гр-1 Пациенты со спонтанным разрешением - 4,5% (2/44) Гр-2 - реинфекция у 19,9% (31/156) ОР 5.2 95% ДИ 1,2 - 33,0; P = ,016
Доказательство спонтанного разрешения неосложнённой C. trachomatis инфекции 1Geisler WM, et al. JID 2013; 207:1850-6 Через 15 сут. (6–47) Через 183 сут. (35-365) Скрининг: Осмотр, НАСБА N=245, 22 (16–54) лет; BV 31% Визит 2, N=200. Осмотр, НАСБА Осмотр, НАСБА. Начало лечения. У 22% - спонтанное разрешение (Гр-1) - нет АТ Гр-1 Пациенты со спонтанным разрешением - 4,5% (2/44) Гр-2 - реинфекция у 19,9% (31/156) ОР 5.2 95% ДИ 1,2 - 33,0; P = ,016
Cлайд 20
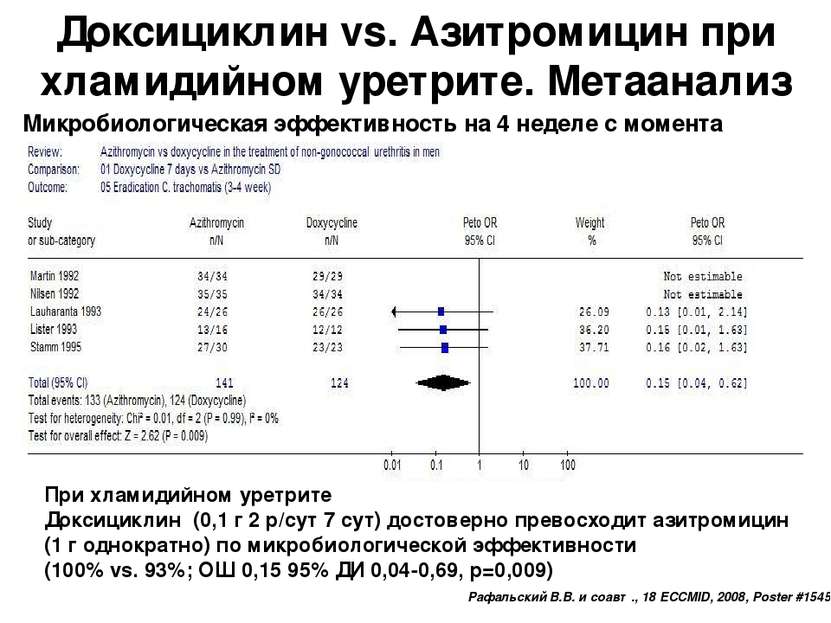
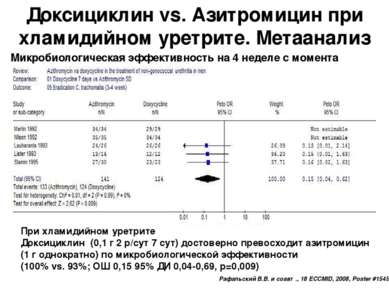 Доксициклин vs. Азитромицин при хламидийном уретрите. Метаанализ Микробиологическая эффективность на 4 неделе с момента начала терапии При хламидийном уретрите Доксициклин (0,1 г 2 р/сут 7 сут) достоверно превосходит азитромицин (1 г однократно) по микробиологической эффективности (100% vs. 93%; ОШ 0,15 95% ДИ 0,04-0,69, p=0,009) Рафальский В.В. и соавт., 18 ECCMID, 2008, Poster #1545
Доксициклин vs. Азитромицин при хламидийном уретрите. Метаанализ Микробиологическая эффективность на 4 неделе с момента начала терапии При хламидийном уретрите Доксициклин (0,1 г 2 р/сут 7 сут) достоверно превосходит азитромицин (1 г однократно) по микробиологической эффективности (100% vs. 93%; ОШ 0,15 95% ДИ 0,04-0,69, p=0,009) Рафальский В.В. и соавт., 18 ECCMID, 2008, Poster #1545
Cлайд 21
 Азитромицин и УГИ C. trachomatis Исследования двойным слепым методом Nilsen A. MC, DB, Rand. Azi 1,0 (n=35) vs. DOX 7d (n=34) Одинаковая эффективность Stamm W. 11 STI клиник, DB, Rand 2:1. Azi 1,0 (n=30) vs. DOXY 7d (n=21) Одинаковая эффективность (83% vs. 90%) Stamm W. 11 STI клиник, DB, Rand Azi 1,0 (n=11) vs. Рифалазил (n=12) Одинаковая эффективность (64% vs. 83%) Schwebke J. DB, Rand Azi 1,0 (n=53) vs. DOXY (n=58) Худшая эффективность Azi (77% vs. 95%, P=0.011) АНИМАЦИЯ!!! Красным подчёркнуты исследования, не касающиеся применения азитро при хламидийных УГИ. Nilsen, A., A. Halsos, et al. (1992). "A double blind study of single dose azithromycin and doxycycline in the treatment of chlamydial urethritis in males." Genitourin Med 68(5): 325-327. OBJECTIVE: To compare the efficacy and safety of azithromycin and doxycycline in the treatment of males with uncomplicated urethritis caused by chlamydia trachomatis. DESIGN: A multicentre, double-blind, randomised treatment study. SUBJECTS: 130 male outpatients with clinical signs and symptoms of urethritis. SETTING: STD clinics at four Norwegian University Hospitals. METHODS: Patients were randomly allocated to 1000 mg azithromycin as single dose or doxycycline 100 mg twice daily for 7 days. Clinical, bacteriological and safety assessments were made at entry and after 1 and 2 weeks. Safety data were also repeated after 4 weeks. RESULTS: Demographic data were similar in both groups. At the week 1 assessment bacteriological eradication was achieved in 44 of 44 evaluable azithromycintreated patients and in 42 of 42 in the doxycycline group. At the week 2 assessment the corresponding figures were 35 of 35 and 34 of 34 respectively. CONCLUSION: Azithromycin 1000 mg single dose was as effective as doxycycline 100 mg twice daily for 7 days in male patients with chlamydial urethritis. Stamm, W. E., C. B. Hicks, et al. (1995). "Azithromycin for empirical treatment of the nongonococcal urethritis syndrome in men. A randomized double-blind study." Jama 274(7): 545-549. OBJECTIVE: To evaluate the use of single-dose azithromycin for empirical treatment of nongonococcal urethritis. DESIGN: Randomized, double-blind, multicenter trial comparing azithromycin vs doxycycline therapy, with a 2:1 randomization ratio. Patients were evaluated clinically and microbiologically for Chlamydia trachomatis and Ureaplasma urealyticum infection before therapy and at 2 and 5 weeks after study entry. SETTING: Eleven sexually transmitted disease clinics throughout the United States. PATIENTS: A total of 452 men aged 18 years or older with symptomatic nongonococcal urethritis of less than 14 days' duration. INTERVENTION: Patients were treated with either 1.0 g of azithromycin as a single oral dose or 100 mg of doxycycline taken orally twice daily for 7 days. MAIN OUTCOME MEASURES: Clinical resolution of symptoms and signs of nongonococcal urethritis, microbiological cure of C trachomatis and U urealyticum, and occurrence of adverse experiences. RESULTS: Of the 452 patients enrolled, 248 in the azithromycin-treated group and 123 in the doxycycline-treated group were evaluable for clinical response. The two treatment groups were comparable in terms of age, weight, ethnic distribution, sexual preference, sexual activity, and history of prior nongonococcal urethritis or gonorrhea. Sixteen percent of the azithromycin group and 24% of the doxycycline group were culture positive for C trachomatis before therapy, while 38% and 28%, respectively, were culture positive for U urealyticum. The cumulative clinical cure rate was 81% (95% confidence interval [CI], 75% to 85%) in the azithromycin-treated group and 77% (95% CI, 69% to 84%) in the doxycycline-treated group. Clinical cure rates in the two groups were also comparable when patients were stratified by presence or absence of infection with C trachomatis or U urealyticum prior to therapy. Among those infected with C trachomatis, overall microbiological cure rates were 83% (95% CI, 65% to 94%) for azithromycin-treated patients (n = 30) and 90% (95% CI, 68% to 98%) for doxycycline-treated patients (n = 21). Among those infected with U urealyticum, overall microbiological cure rates were 45% (95% CI, 34% to 57%) for azithromycin-treated patients (n = 75) and 47% (95% CI, 30% to 65%) for doxycycline-treated patients (n = 32). Adverse reactions were generally mild to moderate and occurred in 23% of the azithromycin-treated group and 29% of the doxycycline-treated group. CONCLUSIONS: For empirical treatment of the acute nongonococcal urethritis syndrome in men, a single oral dose of azithromycin was as effective as a standard 7-day course of doxycycline in achieving clinical cure. Further, clinical cure rates were comparable with either regimen, regardless of the presence or absence of Chlamydia or Ureaplasma infection. Stamm, W. E., B. E. Batteiger, et al. (2007). "A randomized, double-blind study comparing single-dose rifalazil with single-dose azithromycin for the empirical treatment of nongonococcal urethritis in men." Sex Transm Dis 34(8): 545-552. OBJECTIVES: To determine the safety and effectiveness of single-dose rifalazil, a new rifamycin, for the treatment of nongonococcal urethritis (NGU). STUDY DESIGN: Randomized, double-blind trial comparing rifalazil, 2.5, 12.5 or 25 mg, with 1.0 g azithromycin for the treatment of NGU. One hundred and seventy men were evaluated for Chlamydia trachomatis, Ureaplasma urealyticum, and Mycoplasma genitalium infection before therapy and 2- and 5-weeks posttreatment. RESULTS: C. trachomatis, M. genitalium, and U. urealyticum were present in 42%, 24%, and 28% of subjects, respectively. Microbiologic eradication of C. trachomatis with rifalazil 25 mg at 2- and 5- weeks was 85% and 83%, respectively. Rifalazil was ineffective in eradicating M. genitalium and U. urealyticum. Overall clinical cure rates at 2- and 5-weeks were 86% (95% CI 67-96) and 59% (39-78) in the rifalazil-treated 25 mg group, and 77% (56-91) and 63% (41-81) in the azithromycin-treated group. CONCLUSIONS: Rifalazil was well tolerated and eradicates C. trachomatis but not M. genitalium and U. ureaplasma in men with NGU. Terada, M., E. Ohki, et al. (2010). "[Clinical application of azithromycin extended-release (ER) formulation to treat female sexually transmitted infection]." Jpn J Antibiot 63(2): 93-104. The prevalence of female sexually transmitted infection (STI) in Japan is in the decreasing tendency after 2002, however it still actualizes as a social problem. Azithromycin, which is 15-member macrolide antimicrobial agent, has indication to treat the chlamydia STI in a single dose of 1 g. In April 2009, a single dose of 2 g of azithromycin extended release (ER) formulation, which is improved formulation by the viewpoint of pharmacokinetics-pharmacodynamics, was approved and has indications to treat not only chlamydial STI but also gonococcal STI. We considered the clinical application of azithromycin ER to treat female STI, including our new our own experiences because the clinical studies of azithromycin ER for STI had not been conducted. In conclusion, azithromycin ER was suggested theoretically becoming one of the choices of new treatment STI caused by not only chlamydia but also gonococcus, more clinical consideration to treat STI will be necessary in the future. Schwebke, J. R., A. Rompalo, et al. (2011). "Re-evaluating the treatment of nongonococcal urethritis: emphasizing emerging pathogens--a randomized clinical trial." Clin Infect Dis 52(2): 163-170. BACKGROUND: Nongonococcal urethritis (NGU) is a common chlamydia-associated syndrome in men; however, Trichomonas vaginalis and Mycoplasma genitalium are associated with its etiology and should be considered in approaches to therapy. We sought to determine whether the addition of tinidazole, an anti-trichomonal agent, to the treatment regimen would result in higher cure rates than those achieved with treatment with doxycycline or azithromycin alone. A secondary aim was to compare the efficacy of doxycycline therapy and with that of azithromycin therapy. METHODS: Randomized, controlled, double-blinded phase IIB trial of men with NGU. Participants were randomized to receive doxycycline plus or minus tinidazole or azithromycin plus or minus tinidazole and were observed for up to 45 days. RESULTS: The prevalences of Chlamydia trachomatis, M. genitalium, and T. vaginalis were 43%, 31%, and 13%, respectively. No pathogens were identified in 29% of participants. Clinical cure rates at the first follow-up visit were 74.5% (111 of 149 patients) for doxycycline-containing regimens and 68.6% (107 of 156 patients) for azithromycin-containing regimens. By the final visit, cure rates were 49% (73 of 149 patients) for doxycycline-containing regimens and 43.6% (68 of 156 patients) for azithromycin-containing regimens. There were no significant differences in clinical response rates among the treatment arms. However, the chlamydia clearance rate was 94.8% (55 of 58 patients) for the doxycycline arm and 77.4% (41 of 53 patients) for the azithromycin arm (P = .011), and the M. genitalium clearance rate was 30.8% (12 of 39 patients) for the doxycycline arm and 66.7% (30 of 45 patients) for the azithromycin arm (P = .002). CONCLUSIONS: Addition of tinidazole to the treatment regimen did not result in higher cure rates but effectively eradicated trichomonas. Clinical cure rates were not significantly different between patients treated with doxycycline and those treated with azithromycin; however, doxycycline had significantly better efficacy against Chlamydia, whereas azithromycin was superior to doxycycline for the treatment of M. genitalium.
Азитромицин и УГИ C. trachomatis Исследования двойным слепым методом Nilsen A. MC, DB, Rand. Azi 1,0 (n=35) vs. DOX 7d (n=34) Одинаковая эффективность Stamm W. 11 STI клиник, DB, Rand 2:1. Azi 1,0 (n=30) vs. DOXY 7d (n=21) Одинаковая эффективность (83% vs. 90%) Stamm W. 11 STI клиник, DB, Rand Azi 1,0 (n=11) vs. Рифалазил (n=12) Одинаковая эффективность (64% vs. 83%) Schwebke J. DB, Rand Azi 1,0 (n=53) vs. DOXY (n=58) Худшая эффективность Azi (77% vs. 95%, P=0.011) АНИМАЦИЯ!!! Красным подчёркнуты исследования, не касающиеся применения азитро при хламидийных УГИ. Nilsen, A., A. Halsos, et al. (1992). "A double blind study of single dose azithromycin and doxycycline in the treatment of chlamydial urethritis in males." Genitourin Med 68(5): 325-327. OBJECTIVE: To compare the efficacy and safety of azithromycin and doxycycline in the treatment of males with uncomplicated urethritis caused by chlamydia trachomatis. DESIGN: A multicentre, double-blind, randomised treatment study. SUBJECTS: 130 male outpatients with clinical signs and symptoms of urethritis. SETTING: STD clinics at four Norwegian University Hospitals. METHODS: Patients were randomly allocated to 1000 mg azithromycin as single dose or doxycycline 100 mg twice daily for 7 days. Clinical, bacteriological and safety assessments were made at entry and after 1 and 2 weeks. Safety data were also repeated after 4 weeks. RESULTS: Demographic data were similar in both groups. At the week 1 assessment bacteriological eradication was achieved in 44 of 44 evaluable azithromycintreated patients and in 42 of 42 in the doxycycline group. At the week 2 assessment the corresponding figures were 35 of 35 and 34 of 34 respectively. CONCLUSION: Azithromycin 1000 mg single dose was as effective as doxycycline 100 mg twice daily for 7 days in male patients with chlamydial urethritis. Stamm, W. E., C. B. Hicks, et al. (1995). "Azithromycin for empirical treatment of the nongonococcal urethritis syndrome in men. A randomized double-blind study." Jama 274(7): 545-549. OBJECTIVE: To evaluate the use of single-dose azithromycin for empirical treatment of nongonococcal urethritis. DESIGN: Randomized, double-blind, multicenter trial comparing azithromycin vs doxycycline therapy, with a 2:1 randomization ratio. Patients were evaluated clinically and microbiologically for Chlamydia trachomatis and Ureaplasma urealyticum infection before therapy and at 2 and 5 weeks after study entry. SETTING: Eleven sexually transmitted disease clinics throughout the United States. PATIENTS: A total of 452 men aged 18 years or older with symptomatic nongonococcal urethritis of less than 14 days' duration. INTERVENTION: Patients were treated with either 1.0 g of azithromycin as a single oral dose or 100 mg of doxycycline taken orally twice daily for 7 days. MAIN OUTCOME MEASURES: Clinical resolution of symptoms and signs of nongonococcal urethritis, microbiological cure of C trachomatis and U urealyticum, and occurrence of adverse experiences. RESULTS: Of the 452 patients enrolled, 248 in the azithromycin-treated group and 123 in the doxycycline-treated group were evaluable for clinical response. The two treatment groups were comparable in terms of age, weight, ethnic distribution, sexual preference, sexual activity, and history of prior nongonococcal urethritis or gonorrhea. Sixteen percent of the azithromycin group and 24% of the doxycycline group were culture positive for C trachomatis before therapy, while 38% and 28%, respectively, were culture positive for U urealyticum. The cumulative clinical cure rate was 81% (95% confidence interval [CI], 75% to 85%) in the azithromycin-treated group and 77% (95% CI, 69% to 84%) in the doxycycline-treated group. Clinical cure rates in the two groups were also comparable when patients were stratified by presence or absence of infection with C trachomatis or U urealyticum prior to therapy. Among those infected with C trachomatis, overall microbiological cure rates were 83% (95% CI, 65% to 94%) for azithromycin-treated patients (n = 30) and 90% (95% CI, 68% to 98%) for doxycycline-treated patients (n = 21). Among those infected with U urealyticum, overall microbiological cure rates were 45% (95% CI, 34% to 57%) for azithromycin-treated patients (n = 75) and 47% (95% CI, 30% to 65%) for doxycycline-treated patients (n = 32). Adverse reactions were generally mild to moderate and occurred in 23% of the azithromycin-treated group and 29% of the doxycycline-treated group. CONCLUSIONS: For empirical treatment of the acute nongonococcal urethritis syndrome in men, a single oral dose of azithromycin was as effective as a standard 7-day course of doxycycline in achieving clinical cure. Further, clinical cure rates were comparable with either regimen, regardless of the presence or absence of Chlamydia or Ureaplasma infection. Stamm, W. E., B. E. Batteiger, et al. (2007). "A randomized, double-blind study comparing single-dose rifalazil with single-dose azithromycin for the empirical treatment of nongonococcal urethritis in men." Sex Transm Dis 34(8): 545-552. OBJECTIVES: To determine the safety and effectiveness of single-dose rifalazil, a new rifamycin, for the treatment of nongonococcal urethritis (NGU). STUDY DESIGN: Randomized, double-blind trial comparing rifalazil, 2.5, 12.5 or 25 mg, with 1.0 g azithromycin for the treatment of NGU. One hundred and seventy men were evaluated for Chlamydia trachomatis, Ureaplasma urealyticum, and Mycoplasma genitalium infection before therapy and 2- and 5-weeks posttreatment. RESULTS: C. trachomatis, M. genitalium, and U. urealyticum were present in 42%, 24%, and 28% of subjects, respectively. Microbiologic eradication of C. trachomatis with rifalazil 25 mg at 2- and 5- weeks was 85% and 83%, respectively. Rifalazil was ineffective in eradicating M. genitalium and U. urealyticum. Overall clinical cure rates at 2- and 5-weeks were 86% (95% CI 67-96) and 59% (39-78) in the rifalazil-treated 25 mg group, and 77% (56-91) and 63% (41-81) in the azithromycin-treated group. CONCLUSIONS: Rifalazil was well tolerated and eradicates C. trachomatis but not M. genitalium and U. ureaplasma in men with NGU. Terada, M., E. Ohki, et al. (2010). "[Clinical application of azithromycin extended-release (ER) formulation to treat female sexually transmitted infection]." Jpn J Antibiot 63(2): 93-104. The prevalence of female sexually transmitted infection (STI) in Japan is in the decreasing tendency after 2002, however it still actualizes as a social problem. Azithromycin, which is 15-member macrolide antimicrobial agent, has indication to treat the chlamydia STI in a single dose of 1 g. In April 2009, a single dose of 2 g of azithromycin extended release (ER) formulation, which is improved formulation by the viewpoint of pharmacokinetics-pharmacodynamics, was approved and has indications to treat not only chlamydial STI but also gonococcal STI. We considered the clinical application of azithromycin ER to treat female STI, including our new our own experiences because the clinical studies of azithromycin ER for STI had not been conducted. In conclusion, azithromycin ER was suggested theoretically becoming one of the choices of new treatment STI caused by not only chlamydia but also gonococcus, more clinical consideration to treat STI will be necessary in the future. Schwebke, J. R., A. Rompalo, et al. (2011). "Re-evaluating the treatment of nongonococcal urethritis: emphasizing emerging pathogens--a randomized clinical trial." Clin Infect Dis 52(2): 163-170. BACKGROUND: Nongonococcal urethritis (NGU) is a common chlamydia-associated syndrome in men; however, Trichomonas vaginalis and Mycoplasma genitalium are associated with its etiology and should be considered in approaches to therapy. We sought to determine whether the addition of tinidazole, an anti-trichomonal agent, to the treatment regimen would result in higher cure rates than those achieved with treatment with doxycycline or azithromycin alone. A secondary aim was to compare the efficacy of doxycycline therapy and with that of azithromycin therapy. METHODS: Randomized, controlled, double-blinded phase IIB trial of men with NGU. Participants were randomized to receive doxycycline plus or minus tinidazole or azithromycin plus or minus tinidazole and were observed for up to 45 days. RESULTS: The prevalences of Chlamydia trachomatis, M. genitalium, and T. vaginalis were 43%, 31%, and 13%, respectively. No pathogens were identified in 29% of participants. Clinical cure rates at the first follow-up visit were 74.5% (111 of 149 patients) for doxycycline-containing regimens and 68.6% (107 of 156 patients) for azithromycin-containing regimens. By the final visit, cure rates were 49% (73 of 149 patients) for doxycycline-containing regimens and 43.6% (68 of 156 patients) for azithromycin-containing regimens. There were no significant differences in clinical response rates among the treatment arms. However, the chlamydia clearance rate was 94.8% (55 of 58 patients) for the doxycycline arm and 77.4% (41 of 53 patients) for the azithromycin arm (P = .011), and the M. genitalium clearance rate was 30.8% (12 of 39 patients) for the doxycycline arm and 66.7% (30 of 45 patients) for the azithromycin arm (P = .002). CONCLUSIONS: Addition of tinidazole to the treatment regimen did not result in higher cure rates but effectively eradicated trichomonas. Clinical cure rates were not significantly different between patients treated with doxycycline and those treated with azithromycin; however, doxycycline had significantly better efficacy against Chlamydia, whereas azithromycin was superior to doxycycline for the treatment of M. genitalium.
Cлайд 22
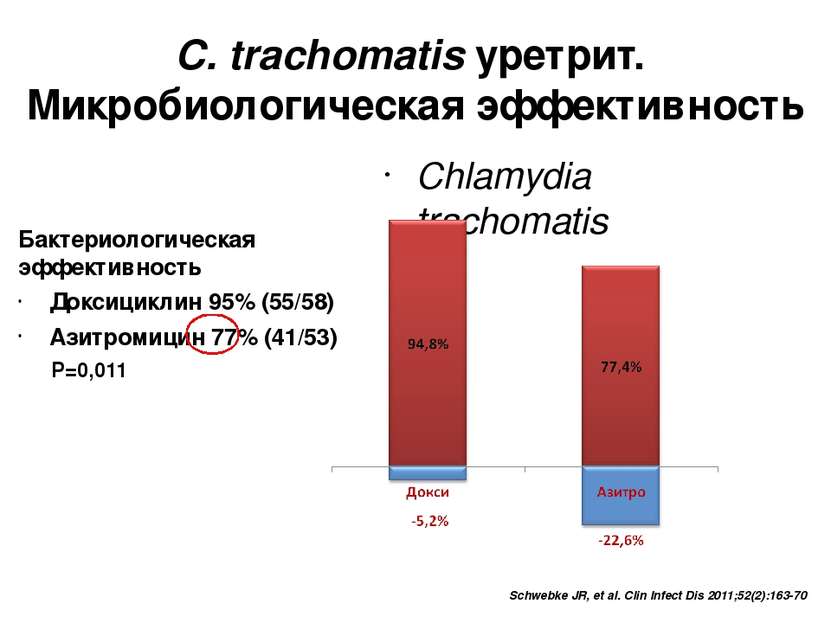
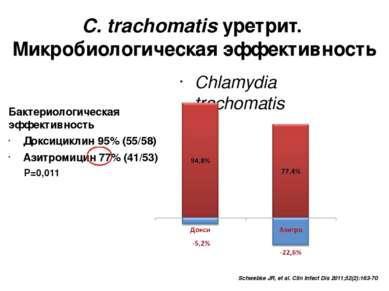 Бактериологическая эффективность Доксициклин 95% (55/58) Азитромицин 77% (41/53) P=0,011 C. trachomatis уретрит. Микробиологическая эффективность Chlamydia trachomatis Schwebke JR, et al. Clin Infect Dis 2011;52(2):163-70 С улучшением чувствительности и специфичности диагностикумов, эффективность препарата падает
Бактериологическая эффективность Доксициклин 95% (55/58) Азитромицин 77% (41/53) P=0,011 C. trachomatis уретрит. Микробиологическая эффективность Chlamydia trachomatis Schwebke JR, et al. Clin Infect Dis 2011;52(2):163-70 С улучшением чувствительности и специфичности диагностикумов, эффективность препарата падает
Cлайд 23
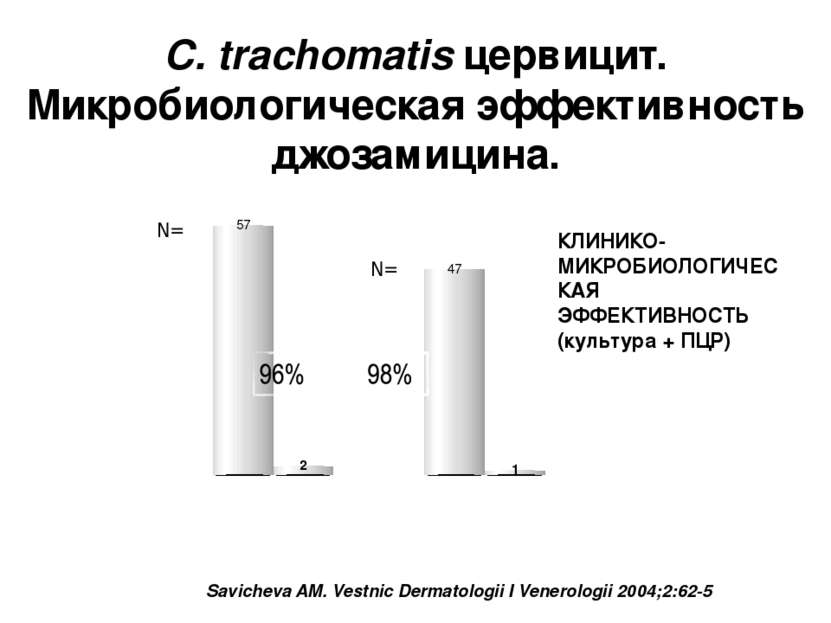
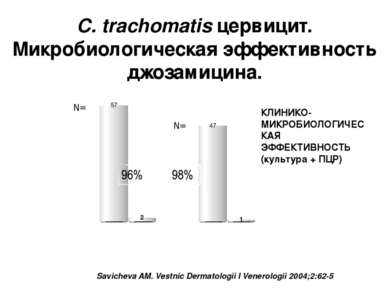 C. trachomatis цервицит. Микробиологическая эффективность джозамицина. Savicheva AM. Vestnic Dermatologii I Venerologii 2004;2:62-5 КЛИНИКО-МИКРОБИОЛОГИЧЕСКАЯ ЭФФЕКТИВНОСТЬ (культура + ПЦР) N= N= AmpliSens Chlamydia trachomatis (RUS) and DNA Sorb (RUS) A. Gushin
C. trachomatis цервицит. Микробиологическая эффективность джозамицина. Savicheva AM. Vestnic Dermatologii I Venerologii 2004;2:62-5 КЛИНИКО-МИКРОБИОЛОГИЧЕСКАЯ ЭФФЕКТИВНОСТЬ (культура + ПЦР) N= N= AmpliSens Chlamydia trachomatis (RUS) and DNA Sorb (RUS) A. Gushin
Cлайд 24
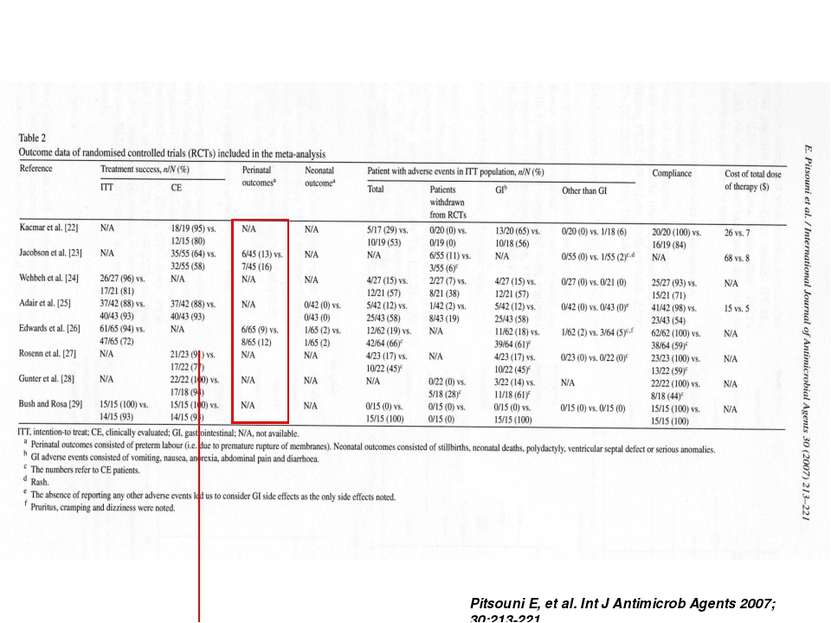
 Pitsouni E, et al. Single-dose azithromycin versus erythromycin or amoxicillin for Chlamydia trachomatis infection during pregnancy: a meta-analysis of randomised controlled trials. Int J Antimicrob Agents 2007;30(3):213-21 Одинаковая эффективность азитромицина, эритромицина и амоксициллина: Azi vs. гр. сравнения: 344 пациентки, ОШ 1,45; 95% ДИ 0,82-2,57 Azi vs. Eri: 200 пациенток ОШ 1,46; 95% ДИ 0,56-3,78 Эффективность азитромицина непостоянна - от 63% до 100% Лечение неосложнённой УГИ (C. trachomatis) у беременных женщин азитромицином 1) Adair, C. D., M. Gunter, et al. (1998). "Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin." Obstet Gynecol 91(2): 165-168. OBJECTIVE: To determine side effect profiles and cure rates of azithromycin compared with erythromycin in the treatment of chlamydial cervicitis complicating pregnancy. METHODS: Pregnant patients with positive DNA antigen assays for Chlamydia trachomatis were randomized to either azithromycin, 1 g oral slurry in a single dose, or erythromycin, 500 mg every 6 hours for 7 days. Repeat assays were planned for 3 weeks after therapy. Side effects, compliance, and treatment efficacy were assessed. RESULTS: One hundred six women were enrolled, and eighty-five women completed the protocol. Significantly fewer gastrointestinal side effects were noted in the azithromycin group than in the erythromycin group (11.9% versus 58.1%, P < or = .01). Enhanced compliance was noted with azithromycin, because it was given in a single observed dose. Similar treatment efficacy was noted between azithromycin and erythromycin (88.1% versus 93.0%, P > .05). CONCLUSION: Compared with erythromycin, azithromycin is associated with significantly fewer gastrointestinal side effects in pregnancy. This association, along with the ease of administration and similar efficacy, suggests that azithromycin should be considered for the initial treatment of chlamydial cervicitis in pregnancy. 2) Jacobson, G. F., A. M. Autry, et al. (2001). "A randomized controlled trial comparing amoxicillin and azithromycin for the treatment of Chlamydia trachomatis in pregnancy." Am J Obstet Gynecol 184(7): 1352-1354; discussion 1354-1356. OBJECTIVE: Our goal was to compare the efficacy of azithromycin with that of amoxicillin for the treatment of Chlamydia trachomatis infection during pregnancy. STUDY DESIGN: A randomized controlled trial of pregnant women with cervical C trachomatis infection receiving care at two inner-city, university-based prenatal clinics. Pregnant women were randomly assigned to receive either oral amoxicillin, 500 mg, three times daily for 7 days, or oral azithromycin, 1 g, in a single dose. Partners were referred for treatment. Tests of cure were scheduled 4 weeks after initiation of treatment. Statistical analysis was performed by using the Student t test and chi2 analysis. RESULTS: One hundred twenty-nine pregnant women were enrolled, and 110 (85%) completed the protocol. There was similar treatment efficacy between amoxicillin and azithromycin (58% vs 64%, respectively,P =.56). In the amoxicillin group 3 women (5.5%) were intolerant, compared with 6 (10.9%) in the azithromycin group (P =.31). CONCLUSION: Amoxicillin and azithromycin are equally efficacious in the treatment of cervical C trachomatis during pregnancy.
Pitsouni E, et al. Single-dose azithromycin versus erythromycin or amoxicillin for Chlamydia trachomatis infection during pregnancy: a meta-analysis of randomised controlled trials. Int J Antimicrob Agents 2007;30(3):213-21 Одинаковая эффективность азитромицина, эритромицина и амоксициллина: Azi vs. гр. сравнения: 344 пациентки, ОШ 1,45; 95% ДИ 0,82-2,57 Azi vs. Eri: 200 пациенток ОШ 1,46; 95% ДИ 0,56-3,78 Эффективность азитромицина непостоянна - от 63% до 100% Лечение неосложнённой УГИ (C. trachomatis) у беременных женщин азитромицином 1) Adair, C. D., M. Gunter, et al. (1998). "Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin." Obstet Gynecol 91(2): 165-168. OBJECTIVE: To determine side effect profiles and cure rates of azithromycin compared with erythromycin in the treatment of chlamydial cervicitis complicating pregnancy. METHODS: Pregnant patients with positive DNA antigen assays for Chlamydia trachomatis were randomized to either azithromycin, 1 g oral slurry in a single dose, or erythromycin, 500 mg every 6 hours for 7 days. Repeat assays were planned for 3 weeks after therapy. Side effects, compliance, and treatment efficacy were assessed. RESULTS: One hundred six women were enrolled, and eighty-five women completed the protocol. Significantly fewer gastrointestinal side effects were noted in the azithromycin group than in the erythromycin group (11.9% versus 58.1%, P < or = .01). Enhanced compliance was noted with azithromycin, because it was given in a single observed dose. Similar treatment efficacy was noted between azithromycin and erythromycin (88.1% versus 93.0%, P > .05). CONCLUSION: Compared with erythromycin, azithromycin is associated with significantly fewer gastrointestinal side effects in pregnancy. This association, along with the ease of administration and similar efficacy, suggests that azithromycin should be considered for the initial treatment of chlamydial cervicitis in pregnancy. 2) Jacobson, G. F., A. M. Autry, et al. (2001). "A randomized controlled trial comparing amoxicillin and azithromycin for the treatment of Chlamydia trachomatis in pregnancy." Am J Obstet Gynecol 184(7): 1352-1354; discussion 1354-1356. OBJECTIVE: Our goal was to compare the efficacy of azithromycin with that of amoxicillin for the treatment of Chlamydia trachomatis infection during pregnancy. STUDY DESIGN: A randomized controlled trial of pregnant women with cervical C trachomatis infection receiving care at two inner-city, university-based prenatal clinics. Pregnant women were randomly assigned to receive either oral amoxicillin, 500 mg, three times daily for 7 days, or oral azithromycin, 1 g, in a single dose. Partners were referred for treatment. Tests of cure were scheduled 4 weeks after initiation of treatment. Statistical analysis was performed by using the Student t test and chi2 analysis. RESULTS: One hundred twenty-nine pregnant women were enrolled, and 110 (85%) completed the protocol. There was similar treatment efficacy between amoxicillin and azithromycin (58% vs 64%, respectively,P =.56). In the amoxicillin group 3 women (5.5%) were intolerant, compared with 6 (10.9%) in the azithromycin group (P =.31). CONCLUSION: Amoxicillin and azithromycin are equally efficacious in the treatment of cervical C trachomatis during pregnancy.
Cлайд 25
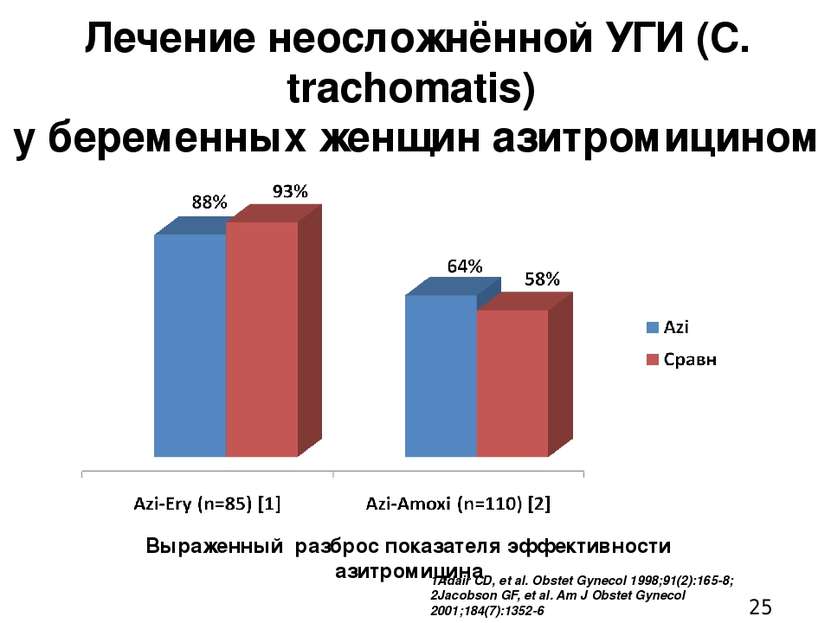
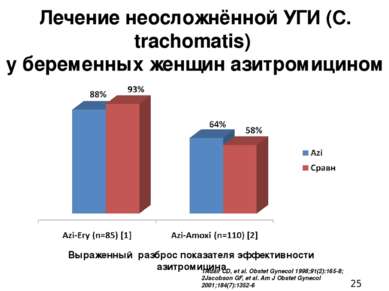 Лечение неосложнённой УГИ (C. trachomatis) у беременных женщин азитромицином 1Adair CD, et al. Obstet Gynecol 1998;91(2):165-8; 2Jacobson GF, et al. Am J Obstet Gynecol 2001;184(7):1352-6 Выраженный разброс показателя эффективности азитромицина 1) Adair, C. D., M. Gunter, et al. (1998). "Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin." Obstet Gynecol 91(2): 165-168. OBJECTIVE: To determine side effect profiles and cure rates of azithromycin compared with erythromycin in the treatment of chlamydial cervicitis complicating pregnancy. METHODS: Pregnant patients with positive DNA antigen assays for Chlamydia trachomatis were randomized to either azithromycin, 1 g oral slurry in a single dose, or erythromycin, 500 mg every 6 hours for 7 days. Repeat assays were planned for 3 weeks after therapy. Side effects, compliance, and treatment efficacy were assessed. RESULTS: One hundred six women were enrolled, and eighty-five women completed the protocol. Significantly fewer gastrointestinal side effects were noted in the azithromycin group than in the erythromycin group (11.9% versus 58.1%, P < or = .01). Enhanced compliance was noted with azithromycin, because it was given in a single observed dose. Similar treatment efficacy was noted between azithromycin and erythromycin (88.1% versus 93.0%, P > .05). CONCLUSION: Compared with erythromycin, azithromycin is associated with significantly fewer gastrointestinal side effects in pregnancy. This association, along with the ease of administration and similar efficacy, suggests that azithromycin should be considered for the initial treatment of chlamydial cervicitis in pregnancy. 2) Jacobson, G. F., A. M. Autry, et al. (2001). "A randomized controlled trial comparing amoxicillin and azithromycin for the treatment of Chlamydia trachomatis in pregnancy." Am J Obstet Gynecol 184(7): 1352-1354; discussion 1354-1356. OBJECTIVE: Our goal was to compare the efficacy of azithromycin with that of amoxicillin for the treatment of Chlamydia trachomatis infection during pregnancy. STUDY DESIGN: A randomized controlled trial of pregnant women with cervical C trachomatis infection receiving care at two inner-city, university-based prenatal clinics. Pregnant women were randomly assigned to receive either oral amoxicillin, 500 mg, three times daily for 7 days, or oral azithromycin, 1 g, in a single dose. Partners were referred for treatment. Tests of cure were scheduled 4 weeks after initiation of treatment. Statistical analysis was performed by using the Student t test and chi2 analysis. RESULTS: One hundred twenty-nine pregnant women were enrolled, and 110 (85%) completed the protocol. There was similar treatment efficacy between amoxicillin and azithromycin (58% vs 64%, respectively,P =.56). In the amoxicillin group 3 women (5.5%) were intolerant, compared with 6 (10.9%) in the azithromycin group (P =.31). CONCLUSION: Amoxicillin and azithromycin are equally efficacious in the treatment of cervical C trachomatis during pregnancy.
Лечение неосложнённой УГИ (C. trachomatis) у беременных женщин азитромицином 1Adair CD, et al. Obstet Gynecol 1998;91(2):165-8; 2Jacobson GF, et al. Am J Obstet Gynecol 2001;184(7):1352-6 Выраженный разброс показателя эффективности азитромицина 1) Adair, C. D., M. Gunter, et al. (1998). "Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin." Obstet Gynecol 91(2): 165-168. OBJECTIVE: To determine side effect profiles and cure rates of azithromycin compared with erythromycin in the treatment of chlamydial cervicitis complicating pregnancy. METHODS: Pregnant patients with positive DNA antigen assays for Chlamydia trachomatis were randomized to either azithromycin, 1 g oral slurry in a single dose, or erythromycin, 500 mg every 6 hours for 7 days. Repeat assays were planned for 3 weeks after therapy. Side effects, compliance, and treatment efficacy were assessed. RESULTS: One hundred six women were enrolled, and eighty-five women completed the protocol. Significantly fewer gastrointestinal side effects were noted in the azithromycin group than in the erythromycin group (11.9% versus 58.1%, P < or = .01). Enhanced compliance was noted with azithromycin, because it was given in a single observed dose. Similar treatment efficacy was noted between azithromycin and erythromycin (88.1% versus 93.0%, P > .05). CONCLUSION: Compared with erythromycin, azithromycin is associated with significantly fewer gastrointestinal side effects in pregnancy. This association, along with the ease of administration and similar efficacy, suggests that azithromycin should be considered for the initial treatment of chlamydial cervicitis in pregnancy. 2) Jacobson, G. F., A. M. Autry, et al. (2001). "A randomized controlled trial comparing amoxicillin and azithromycin for the treatment of Chlamydia trachomatis in pregnancy." Am J Obstet Gynecol 184(7): 1352-1354; discussion 1354-1356. OBJECTIVE: Our goal was to compare the efficacy of azithromycin with that of amoxicillin for the treatment of Chlamydia trachomatis infection during pregnancy. STUDY DESIGN: A randomized controlled trial of pregnant women with cervical C trachomatis infection receiving care at two inner-city, university-based prenatal clinics. Pregnant women were randomly assigned to receive either oral amoxicillin, 500 mg, three times daily for 7 days, or oral azithromycin, 1 g, in a single dose. Partners were referred for treatment. Tests of cure were scheduled 4 weeks after initiation of treatment. Statistical analysis was performed by using the Student t test and chi2 analysis. RESULTS: One hundred twenty-nine pregnant women were enrolled, and 110 (85%) completed the protocol. There was similar treatment efficacy between amoxicillin and azithromycin (58% vs 64%, respectively,P =.56). In the amoxicillin group 3 women (5.5%) were intolerant, compared with 6 (10.9%) in the azithromycin group (P =.31). CONCLUSION: Amoxicillin and azithromycin are equally efficacious in the treatment of cervical C trachomatis during pregnancy.
Cлайд 26
 Хламидия, гипоксия и эффективность АБ Концентрация О2 в очагах воспаления (цервицит, вагинит1 и др.) снижена Влияние Ɣ-IF на формирование аберрантных (персистирующих) форм C.trachomatis в условиях гипоксии снижено2 Чувствительность C. trachomatis к АБ в условиях нормоксии и гипоксии различна3 1Juul N, et al. J Bacteriol 2007;189:6723–6 2Roth A, et al. Proc Natl Acad Sci USA.2010;107:19502–7 3Shima K, et al. AAC 2013; 57:2828-30 Roth A, et al. Proc Natl Acad Sci USA 2010;107:19502–7
Хламидия, гипоксия и эффективность АБ Концентрация О2 в очагах воспаления (цервицит, вагинит1 и др.) снижена Влияние Ɣ-IF на формирование аберрантных (персистирующих) форм C.trachomatis в условиях гипоксии снижено2 Чувствительность C. trachomatis к АБ в условиях нормоксии и гипоксии различна3 1Juul N, et al. J Bacteriol 2007;189:6723–6 2Roth A, et al. Proc Natl Acad Sci USA.2010;107:19502–7 3Shima K, et al. AAC 2013; 57:2828-30 Roth A, et al. Proc Natl Acad Sci USA 2010;107:19502–7
Cлайд 27
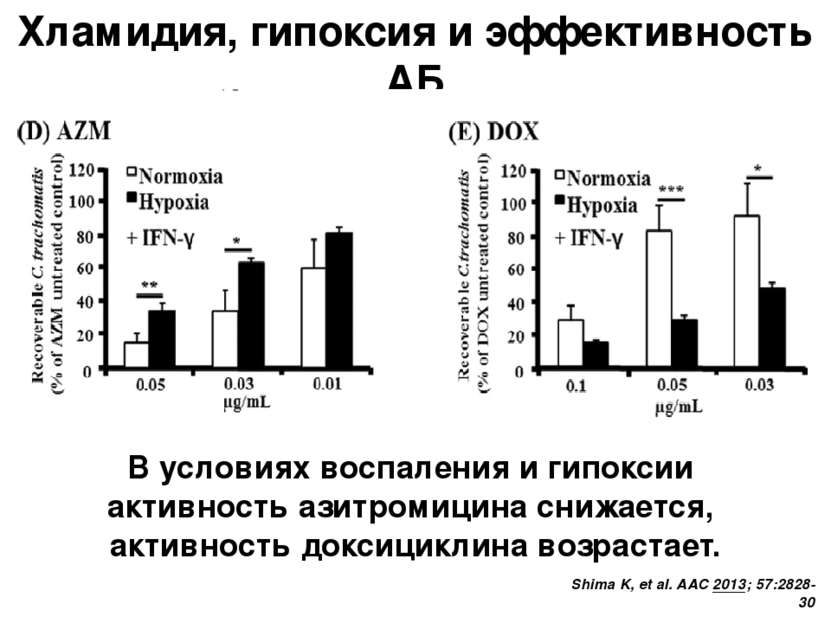
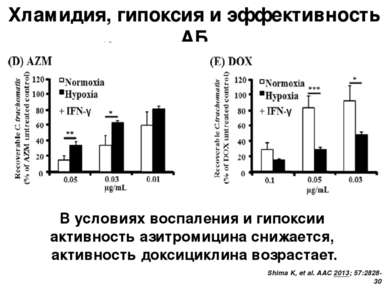 Хламидия, гипоксия и эффективность АБ Shima K, et al. AAC 2013; 57:2828-30 В условиях воспаления и гипоксии активность азитромицина снижается, активность доксициклина возрастает. Roth A, Konig P, van Zandbergen G, Klinger M, Hellwig-Burgel T, Daubener W, Bohlmann MK, Rupp J. 2010. Hypoxia abrogates antichla- mydial properties of IFN-gamma in human fallopian tube cells in vitro and ex vivo. Proc. Natl. Acad. Sci. U. S. A. 107:19502–19507. О влиянии гипоксии на Т-лимфоцит зависимое IF-g опосредованное подавление хламидий
Хламидия, гипоксия и эффективность АБ Shima K, et al. AAC 2013; 57:2828-30 В условиях воспаления и гипоксии активность азитромицина снижается, активность доксициклина возрастает. Roth A, Konig P, van Zandbergen G, Klinger M, Hellwig-Burgel T, Daubener W, Bohlmann MK, Rupp J. 2010. Hypoxia abrogates antichla- mydial properties of IFN-gamma in human fallopian tube cells in vitro and ex vivo. Proc. Natl. Acad. Sci. U. S. A. 107:19502–19507. О влиянии гипоксии на Т-лимфоцит зависимое IF-g опосредованное подавление хламидий
Cлайд 28
 Разночтение результатов определения чувствительности хламидии 1990 г. Оригинальное исследование сообщает о резистентности к доксициклину1 2013 г. Контроль «резистентных» штаммов методом секвенирования генома и посева на клеточную питательную среду McCoy Подвергнутые воздействию доксициклина «устойчивые» штаммы не продемонстрировали роста через неделю после удаления АБ Гены резистентности не выявлены «Свечение» при ПИФ являлось ложно-положительной реакцией 1Jones RB, et al. J Infect Dis 1990; 162:1309-15 2O'Neill CE, et al. Microbiology 2013;159:748-56
Разночтение результатов определения чувствительности хламидии 1990 г. Оригинальное исследование сообщает о резистентности к доксициклину1 2013 г. Контроль «резистентных» штаммов методом секвенирования генома и посева на клеточную питательную среду McCoy Подвергнутые воздействию доксициклина «устойчивые» штаммы не продемонстрировали роста через неделю после удаления АБ Гены резистентности не выявлены «Свечение» при ПИФ являлось ложно-положительной реакцией 1Jones RB, et al. J Infect Dis 1990; 162:1309-15 2O'Neill CE, et al. Microbiology 2013;159:748-56
Cлайд 29
 Исследование in vivo, посвящённое эмбриотоксическому и тератогенному влиянию макролидов (АЗИТРОМИЦИН, СПИРАМИЦИН, КЛАРИТРОМИЦИН) на плод (животная модель): Был определен больший тератогенный потенциал азитромицина Karabulut AK, Uysal, II, Acar H, Fazliogullari Z. Investigation of developmental toxicity and teratogenicity of macrolide antibiotics in cultured rat embryos. Anat Histol Embryol 2008;37(5):369-75 ДОКАЗАНА ЛИ БЕЗОПАСНОСТЬ АЗАЛИДА В ЭКСПЕРИМЕНТЕ НА ЖИВОТНЫХ ? Karabulut, A. K., Uysal, II, et al. (2008). "Investigation of Developmental Toxicity and Teratogenicity of Macrolide Antibiotics in Cultured Rat Embryos." Anat Histol Embryol. Macrolides are considered to be one of the safest anti-infective groups in clinical use, with severe adverse reactions being rare. However, there are limited data about their embryotoxicity and teratogenicity. We aimed to investigate and compare the effects of these agents on embryonic growth and development. Rat embryos were cultured in vitro for 48 h in rat serum. Whole rat serum was used as a culture medium for the control group while different concentrations of spiramycin and azithromycin (1.25-6.25 mug/ml), and clarithromycin (2.5-30 mug/ml) were added to rat serum for the experimental groups. Dose-dependent effects of macrolides on embryonic developmental parameters were compared using morphological methods. Embryos were evaluated for the presence of any malformations. After morphological examination of the embryos, total DNA was extracted from the cells using standard procedures to determine fragmentation of nuclear DNA of embryonic cells. When compared with the control embryos, the macrolides significantly decreased all growth and developmental parameters dose dependently. While clarithromycin was found to cause more developmental toxicity than spiramycin and azithromycin, azitromycin was determined to have more teratogenicity potential. Compared with controls, there was no difference regarding the fragmentation of nuclear DNA of all the agents used. According to these results, when the toxic and teratogenic potential of the used agents compared, because of the lower toxic and teratogenic effects observed with spiramycin, this agent may be preferred for parturients.
Исследование in vivo, посвящённое эмбриотоксическому и тератогенному влиянию макролидов (АЗИТРОМИЦИН, СПИРАМИЦИН, КЛАРИТРОМИЦИН) на плод (животная модель): Был определен больший тератогенный потенциал азитромицина Karabulut AK, Uysal, II, Acar H, Fazliogullari Z. Investigation of developmental toxicity and teratogenicity of macrolide antibiotics in cultured rat embryos. Anat Histol Embryol 2008;37(5):369-75 ДОКАЗАНА ЛИ БЕЗОПАСНОСТЬ АЗАЛИДА В ЭКСПЕРИМЕНТЕ НА ЖИВОТНЫХ ? Karabulut, A. K., Uysal, II, et al. (2008). "Investigation of Developmental Toxicity and Teratogenicity of Macrolide Antibiotics in Cultured Rat Embryos." Anat Histol Embryol. Macrolides are considered to be one of the safest anti-infective groups in clinical use, with severe adverse reactions being rare. However, there are limited data about their embryotoxicity and teratogenicity. We aimed to investigate and compare the effects of these agents on embryonic growth and development. Rat embryos were cultured in vitro for 48 h in rat serum. Whole rat serum was used as a culture medium for the control group while different concentrations of spiramycin and azithromycin (1.25-6.25 mug/ml), and clarithromycin (2.5-30 mug/ml) were added to rat serum for the experimental groups. Dose-dependent effects of macrolides on embryonic developmental parameters were compared using morphological methods. Embryos were evaluated for the presence of any malformations. After morphological examination of the embryos, total DNA was extracted from the cells using standard procedures to determine fragmentation of nuclear DNA of embryonic cells. When compared with the control embryos, the macrolides significantly decreased all growth and developmental parameters dose dependently. While clarithromycin was found to cause more developmental toxicity than spiramycin and azithromycin, azitromycin was determined to have more teratogenicity potential. Compared with controls, there was no difference regarding the fragmentation of nuclear DNA of all the agents used. According to these results, when the toxic and teratogenic potential of the used agents compared, because of the lower toxic and teratogenic effects observed with spiramycin, this agent may be preferred for parturients.
Cлайд 34
 Руководство по лечению C. trachomatis ИППП. IUSTI 2010 В тех странах, где препарат доступен, Джозамицин показал безопасность и эффективность и также может быть применен (рассмотрен).
Руководство по лечению C. trachomatis ИППП. IUSTI 2010 В тех странах, где препарат доступен, Джозамицин показал безопасность и эффективность и также может быть применен (рассмотрен).
Cлайд 35
 Джозамицин в США. Причина отказа FDA в регистрации, 2006 http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId= В 2006 г швейцарская компания подала заявление на регистрацию используемого в Европе 16-членного макролида –джозамицина. Основой для отказа FDA послужило отсутствие в регистрационной форме информаци о том, что препарат обладает дополнительными преимуществами по сравнению с другими макролидами, уже зарегистрированными в США. К сожалению, к тому моменту, впрочем как и сейчас, работ, подтверждающих преимущество препарата при M. genitalium инфекции, равно как и его преимущество с точки зрения индукции мутаций, определяющих резистентность к макролидам, недостаточно. Однако, это именно те аргументы, которые определяют преимущество препарата перед 14 и 15 членными представителями семейства макролидов http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId=
Джозамицин в США. Причина отказа FDA в регистрации, 2006 http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId= В 2006 г швейцарская компания подала заявление на регистрацию используемого в Европе 16-членного макролида –джозамицина. Основой для отказа FDA послужило отсутствие в регистрационной форме информаци о том, что препарат обладает дополнительными преимуществами по сравнению с другими макролидами, уже зарегистрированными в США. К сожалению, к тому моменту, впрочем как и сейчас, работ, подтверждающих преимущество препарата при M. genitalium инфекции, равно как и его преимущество с точки зрения индукции мутаций, определяющих резистентность к макролидам, недостаточно. Однако, это именно те аргументы, которые определяют преимущество препарата перед 14 и 15 членными представителями семейства макролидов http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId=
Cлайд 36
 Сумамед в США. Причина отказа FDA в регистрации, 2002 http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=112-0029807-4&DocId=4&LineId=1&SfxId=#.UcD8J1b66Ys.mailto В 2006 г швейцарская компания подала заявление на регистрацию используемого в Европе 16-членного макролида –джозамицина. Основой для отказа FDA послужило отсутствие в регистрационной форме информаци о том, что препарат обладает дополнительными преимуществами по сравнению с другими макролидами, уже зарегистрированными в США. К сожалению, к тому моменту, впрочем как и сейчас, работ, подтверждающих преимущество препарата при M. genitalium инфекции, равно как и его преимущество с точки зрения индукции мутаций, определяющих резистентность к макролидам, недостаточно. Однако, это именно те аргументы, которые определяют преимущество препарата перед 14 и 15 членными представителями семейства макролидов http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId=
Сумамед в США. Причина отказа FDA в регистрации, 2002 http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=112-0029807-4&DocId=4&LineId=1&SfxId=#.UcD8J1b66Ys.mailto В 2006 г швейцарская компания подала заявление на регистрацию используемого в Европе 16-членного макролида –джозамицина. Основой для отказа FDA послужило отсутствие в регистрационной форме информаци о том, что препарат обладает дополнительными преимуществами по сравнению с другими макролидами, уже зарегистрированными в США. К сожалению, к тому моменту, впрочем как и сейчас, работ, подтверждающих преимущество препарата при M. genitalium инфекции, равно как и его преимущество с точки зрения индукции мутаций, определяющих резистентность к макролидам, недостаточно. Однако, это именно те аргументы, которые определяют преимущество препарата перед 14 и 15 членными представителями семейства макролидов http://www.accessdata.fda.gov/scripts/importrefusals/ir_detail.cfm?EntryId=DO7-0110115-9&DocId=1&LineId=1&SfxId=
Cлайд 37
 ВЕРОЯТНЫЕ ПРИЧИНЫ НЕЭФФЕКТИВНОСТИ КОРОТКИХ КУРСОВ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ 1,7 Гетеротипичная резистентность Наблюдается при высокой «бактериальной нагрузке» - уретрит, цервицит (±) Наличие в микробной популяции персистеров и/или мутантов 23S рРНК2-6 Эффект недостаточной дозы бактериостатика Гомотипичная (мутация) резистентность Определение ДНК/РНК высокочувствительными МАНК в сроки ≤5 нед может сопровождаться ложноположительным ответом1,7 1 Horner PJ. Sex Transm Infect 2012; 88:154-6; 2 Horner P. Sex Transm Infect 2006; 82:340-3 3 Suchland RJ, et al. AAC 2003; 47:636-42; 4 Wang SA, et al. J Infect Dis 2005; 191:917-23 5 Balaban NQ, et al. Science 2004:1099390; 6 Wyrick PB. J Infect Dis 2010; 201 Suppl 2:S88-95 7 Dukers-Muijrers NH, et al.PLoS One 2012; 7:e34108
ВЕРОЯТНЫЕ ПРИЧИНЫ НЕЭФФЕКТИВНОСТИ КОРОТКИХ КУРСОВ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ 1,7 Гетеротипичная резистентность Наблюдается при высокой «бактериальной нагрузке» - уретрит, цервицит (±) Наличие в микробной популяции персистеров и/или мутантов 23S рРНК2-6 Эффект недостаточной дозы бактериостатика Гомотипичная (мутация) резистентность Определение ДНК/РНК высокочувствительными МАНК в сроки ≤5 нед может сопровождаться ложноположительным ответом1,7 1 Horner PJ. Sex Transm Infect 2012; 88:154-6; 2 Horner P. Sex Transm Infect 2006; 82:340-3 3 Suchland RJ, et al. AAC 2003; 47:636-42; 4 Wang SA, et al. J Infect Dis 2005; 191:917-23 5 Balaban NQ, et al. Science 2004:1099390; 6 Wyrick PB. J Infect Dis 2010; 201 Suppl 2:S88-95 7 Dukers-Muijrers NH, et al.PLoS One 2012; 7:e34108
Cлайд 38
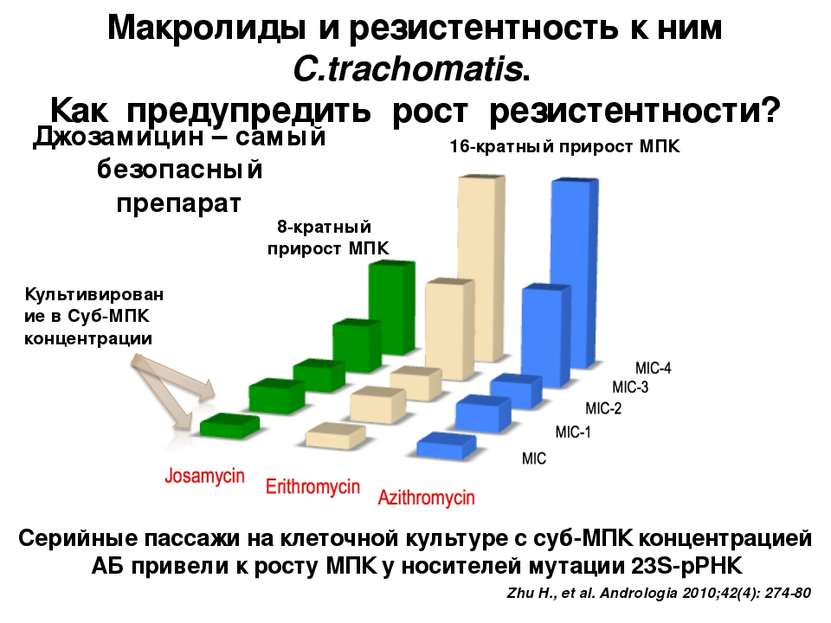
 Макролиды и резистентность к ним C.trachomatis. Как предупредить рост резистентности? Zhu H., et al. Andrologia 2010;42(4): 274-80 Серийные пассажи на клеточной культуре с суб-МПК концентрацией АБ привели к росту МПК у носителей мутации 23S-рРНК 16-кратный прирост МПК 8-кратный прирост МПК Культивирование в Суб-МПК концентрации Джозамицин – самый безопасный препарат
Макролиды и резистентность к ним C.trachomatis. Как предупредить рост резистентности? Zhu H., et al. Andrologia 2010;42(4): 274-80 Серийные пассажи на клеточной культуре с суб-МПК концентрацией АБ привели к росту МПК у носителей мутации 23S-рРНК 16-кратный прирост МПК 8-кратный прирост МПК Культивирование в Суб-МПК концентрации Джозамицин – самый безопасный препарат
Cлайд 39
 Схемы лечения Лечение хламидийной инфекции нижнего отдела мочеполовой системы (А56.0), аноректальной области (А 56.3), хламидийного фарингита (А 56.4), хламидийного конъюнктивита (А 74.0) Препараты выбора: Доксициклина моногидрат 100 мг внутрь 2 раза в сутки в течение 7 дней или Джозамицин 500 мг внутрь 3 раза в сутки в течение 7 дней или Азитромицин 1,0 г внутрь однократно Альтернативные препараты: Левофлоксацин 500 мг внутрь 1 раз в сутки в течение 7 дней или Офлоксацин 400 мг внутрь 2 раза в сутки в течение 7 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Схемы лечения Лечение хламидийной инфекции нижнего отдела мочеполовой системы (А56.0), аноректальной области (А 56.3), хламидийного фарингита (А 56.4), хламидийного конъюнктивита (А 74.0) Препараты выбора: Доксициклина моногидрат 100 мг внутрь 2 раза в сутки в течение 7 дней или Джозамицин 500 мг внутрь 3 раза в сутки в течение 7 дней или Азитромицин 1,0 г внутрь однократно Альтернативные препараты: Левофлоксацин 500 мг внутрь 1 раз в сутки в течение 7 дней или Офлоксацин 400 мг внутрь 2 раза в сутки в течение 7 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 40
 Схемы лечения Лечение хламидийной инфекции верхних отделов мочеполовой системы, органов малого таза и других органов (А 56.1, А 56.8) Длительность курса терапии зависит от степени клинических проявлений воспалительных процессов мочеполовых органов, результатов лабораторных и инструментальных исследований. В зависимости от вышеперечисленных факторов длительность терапии может варьировать от 14 до 21 дня. Препараты выбора: Доксициклина моногидрат 100 мг внутрь 2 раза в сутки в течение 14-21 дней или Джозамицин 500 мг внутрь 3 раза в сутки в течение 14-21 дней Альтернативные препараты: Левофлоксацин 500 мг внутрь 1 раз в сутки в течение 14-21 дней или Офлоксацин 400 мг внутрь 2 раза в сутки в течение 14-21 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Схемы лечения Лечение хламидийной инфекции верхних отделов мочеполовой системы, органов малого таза и других органов (А 56.1, А 56.8) Длительность курса терапии зависит от степени клинических проявлений воспалительных процессов мочеполовых органов, результатов лабораторных и инструментальных исследований. В зависимости от вышеперечисленных факторов длительность терапии может варьировать от 14 до 21 дня. Препараты выбора: Доксициклина моногидрат 100 мг внутрь 2 раза в сутки в течение 14-21 дней или Джозамицин 500 мг внутрь 3 раза в сутки в течение 14-21 дней Альтернативные препараты: Левофлоксацин 500 мг внутрь 1 раз в сутки в течение 14-21 дней или Офлоксацин 400 мг внутрь 2 раза в сутки в течение 14-21 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 41
 Особые ситуации Лечение беременных: Джозамицин 500 мг внутрь 3 раза в сутки в течение 7 дней по показаниям после врачебной оценки пользы/риска Лечение детей (с массой тела менее 45 кг): Джозамицин 50 мг/кг массы тела в 3 приема в течение 7 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Особые ситуации Лечение беременных: Джозамицин 500 мг внутрь 3 раза в сутки в течение 7 дней по показаниям после врачебной оценки пользы/риска Лечение детей (с массой тела менее 45 кг): Джозамицин 50 мг/кг массы тела в 3 приема в течение 7 дней Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с
Cлайд 42
 Ошибки организационные на всех этапах ведения пациентов Не обследуются контактные лица (при неосложненных формах) – 51% При ВЗОМТ/эпидидимите не проводится обследование контактных лиц – 86% Не привлекается консультант-дерматовенеролог при ведения пациентов с осложненными формами хламидийной инфекции Не регистрируются осложнения (это не регламентировано – но как узнать статистику и планировать профилактические мероприятия ..???..)
Ошибки организационные на всех этапах ведения пациентов Не обследуются контактные лица (при неосложненных формах) – 51% При ВЗОМТ/эпидидимите не проводится обследование контактных лиц – 86% Не привлекается консультант-дерматовенеролог при ведения пациентов с осложненными формами хламидийной инфекции Не регистрируются осложнения (это не регламентировано – но как узнать статистику и планировать профилактические мероприятия ..???..)
Cлайд 43
 Организация лечебного процесса на всех этапах ведения пациентов Слабое взаимодействие врачей разных специальностей, вовлеченных в процесс лечения больных с ИППП Недостаток методических материалов или отсутствие контроля за их исполнением Неспособность существующей системы контроля качества лечебной работы реально постоянно контролировать работу медицинского персонала на всех этапах ведения пациентов
Организация лечебного процесса на всех этапах ведения пациентов Слабое взаимодействие врачей разных специальностей, вовлеченных в процесс лечения больных с ИППП Недостаток методических материалов или отсутствие контроля за их исполнением Неспособность существующей системы контроля качества лечебной работы реально постоянно контролировать работу медицинского персонала на всех этапах ведения пациентов
Cлайд 45
 Возможные предпосылки развития аберрантных (персистентных) форм хламидий Хламидии могут ингибировать слияние фагосом с лизосомами Фагоцитоз при хламидийной инфекции непродуктивный - - рост хламидий в моноцитах останавливается в промежуточном состоянии на стадии между элементарными и ретикулярными тельцами [*] На этом этапе в цитоплазме моноцитов обнаруживается липополисахарид клеточной стенки и отсутствует главный белок наружной мембраны (МОМР) [*] * Koehler L., Nettelnbreker E., On N., Drommer W., Zeidler Н. Persistent, nonproductive infection of human peripheral monocytes with Chlamydia trechomatis serovar К is due to an intracellular growth arrest at an eriy stage of the chlamydial development. Abstracts of Proceedings of the 8th International Symposium of Human Chlamydial Infections. Gouvieux-Chantilly. France. 12-24 June 1994; 427-430
Возможные предпосылки развития аберрантных (персистентных) форм хламидий Хламидии могут ингибировать слияние фагосом с лизосомами Фагоцитоз при хламидийной инфекции непродуктивный - - рост хламидий в моноцитах останавливается в промежуточном состоянии на стадии между элементарными и ретикулярными тельцами [*] На этом этапе в цитоплазме моноцитов обнаруживается липополисахарид клеточной стенки и отсутствует главный белок наружной мембраны (МОМР) [*] * Koehler L., Nettelnbreker E., On N., Drommer W., Zeidler Н. Persistent, nonproductive infection of human peripheral monocytes with Chlamydia trechomatis serovar К is due to an intracellular growth arrest at an eriy stage of the chlamydial development. Abstracts of Proceedings of the 8th International Symposium of Human Chlamydial Infections. Gouvieux-Chantilly. France. 12-24 June 1994; 427-430
Cлайд 46
 Макрофаги презентируют Т-хелперам липополисахаридный антиген и не презентируют основной протективный антиген хламидий МОМР ↓ Иммунный ответ заведомо формируется к вариабельному ЛПС и оказывается неспецифическим по отношению к Chlamydia trachomatis Возможные предпосылки развития аберрантных (персистентных) форм хламидий
Макрофаги презентируют Т-хелперам липополисахаридный антиген и не презентируют основной протективный антиген хламидий МОМР ↓ Иммунный ответ заведомо формируется к вариабельному ЛПС и оказывается неспецифическим по отношению к Chlamydia trachomatis Возможные предпосылки развития аберрантных (персистентных) форм хламидий
Cлайд 47
 Возможные предпосылки развития аберрантных (персистентных) форм хламидий Высокие дозы Ɣ -ИФ полностью ингибируют рост хламидий. Низкие - индуцируют развитие морфологически аберрантных форм включений [1] [2] Воздействие Ɣ -ИФ на эпителиальные клетки приводит к активации синтеза фермента (индол-2,3-диоксигеназы) ↓ Запуск О 2 и NADPH+H+-зависимого фенил-кинурениновый цикла деградации триптофана на наружной мембране митохондрий в цитозоле ↓ Истощение внутриклеточного пула триптофана приводит к возникновению аберрантных форм 1. Битти В.Л., Моррисон Р.П., Бирн Д.И. Персистенция хламидий: от клеточных культур до патогенеза хламидийной инфекции. ЗППП 6,1995; 3-18 2. Beatty W. L., Belinger T. A., Le K. D., Desai A. A., Morrison R. P., Byme G. I. Chlamydial persistence: mechanism of induction and parallels to a stress-relate response. Abstracts of Proceedings of the 8й International Symposium of Human Chlamydial Infections. Gouvieux-Chanrilly. France. 12-24 June 1994; 415-418
Возможные предпосылки развития аберрантных (персистентных) форм хламидий Высокие дозы Ɣ -ИФ полностью ингибируют рост хламидий. Низкие - индуцируют развитие морфологически аберрантных форм включений [1] [2] Воздействие Ɣ -ИФ на эпителиальные клетки приводит к активации синтеза фермента (индол-2,3-диоксигеназы) ↓ Запуск О 2 и NADPH+H+-зависимого фенил-кинурениновый цикла деградации триптофана на наружной мембране митохондрий в цитозоле ↓ Истощение внутриклеточного пула триптофана приводит к возникновению аберрантных форм 1. Битти В.Л., Моррисон Р.П., Бирн Д.И. Персистенция хламидий: от клеточных культур до патогенеза хламидийной инфекции. ЗППП 6,1995; 3-18 2. Beatty W. L., Belinger T. A., Le K. D., Desai A. A., Morrison R. P., Byme G. I. Chlamydial persistence: mechanism of induction and parallels to a stress-relate response. Abstracts of Proceedings of the 8й International Symposium of Human Chlamydial Infections. Gouvieux-Chanrilly. France. 12-24 June 1994; 415-418
Cлайд 48
 Медиаторы персистенции C. trachomatis Медиатор Эффект Низкие концентрацииƔ-интерферона Резкое снижение количества эндогенного триптофана (активация фермента индоламин-2,3-диоксигеназы, расщепляющего триптофан до N-формилкинуренина) ФНО-a Опосредованный, путем активацииb-ИФ (блокирует репродукцию внутриклеточных микроорганизмов, путем усиления экспрессии мембранных белков клеток) Дефицит эндогенного триптофана Необходим для построения МОМР ДефицитцГМФи высокое количествоцАМФ Отсутствие активации ферментов необходимых для дифференциации РТ в ЭТ Дефицит и/или действие антагонистов Са2+ Нарушение агрегации эндосомальных вакуолей L-изолейцин Эффект возможно обусловлен включением продукта метаболизма a -метилбутарила-СоА в синтез жирных кислот С. trachomatis с последующим встраиванием "чужих" триглицеридов в клеточную мембрану, приводя к ее дестабилизации Дефицит цистеина Незаменима аминокислота, контролирующая дифференциацию РТ в ЭТ (включается в 3 важнейших для дифференциации белка), уменьшение числадисульфидныхмостиков - факторов прочности клеточной стенки.
Медиаторы персистенции C. trachomatis Медиатор Эффект Низкие концентрацииƔ-интерферона Резкое снижение количества эндогенного триптофана (активация фермента индоламин-2,3-диоксигеназы, расщепляющего триптофан до N-формилкинуренина) ФНО-a Опосредованный, путем активацииb-ИФ (блокирует репродукцию внутриклеточных микроорганизмов, путем усиления экспрессии мембранных белков клеток) Дефицит эндогенного триптофана Необходим для построения МОМР ДефицитцГМФи высокое количествоцАМФ Отсутствие активации ферментов необходимых для дифференциации РТ в ЭТ Дефицит и/или действие антагонистов Са2+ Нарушение агрегации эндосомальных вакуолей L-изолейцин Эффект возможно обусловлен включением продукта метаболизма a -метилбутарила-СоА в синтез жирных кислот С. trachomatis с последующим встраиванием "чужих" триглицеридов в клеточную мембрану, приводя к ее дестабилизации Дефицит цистеина Незаменима аминокислота, контролирующая дифференциацию РТ в ЭТ (включается в 3 важнейших для дифференциации белка), уменьшение числадисульфидныхмостиков - факторов прочности клеточной стенки.
Cлайд 49
 Про БТШ … Из видоспецифических белков наиболее важен стрессовый белок, выполняющий функцию защиты и сопровождения, — белок теплового шока – БТШ (Heat shock proteins) с молекулярным весом 60 килодальтон. Количество белков теплового шока в клетке составляет 1-2% от общего количества белков, но при стрессе или воспалении их количество увеличивается в 4-5 раз. На 50% БТШ- 60 хламидий гомологичен БТШ человека, индуцирует образование специфических антител и состояние гиперчувствительности замедленного типа.
Про БТШ … Из видоспецифических белков наиболее важен стрессовый белок, выполняющий функцию защиты и сопровождения, — белок теплового шока – БТШ (Heat shock proteins) с молекулярным весом 60 килодальтон. Количество белков теплового шока в клетке составляет 1-2% от общего количества белков, но при стрессе или воспалении их количество увеличивается в 4-5 раз. На 50% БТШ- 60 хламидий гомологичен БТШ человека, индуцирует образование специфических антител и состояние гиперчувствительности замедленного типа.
Cлайд 50
 Критериями диагностики «персистентной формы хламидийной инфекции» является обнаружение антител класса G в сыворотке крови к рекомбинантному белку теплового шока – HSP60. У женщин, имеющих положительную иммунореактивность по отношению к эпитопам hsp60, установлена большая частота сальпингитов и спаек (Hjelholt A., Christiansen G., Johannesson T. et al., 2011., Ellinidi A.N., Ellinidi V.N., Davydova N.I. et al., 2007; Михнина Е.А., Давыдова Н.И., Эллиниди А.Н. и др., 2012) Михнина Е.А., 2012 г.
Критериями диагностики «персистентной формы хламидийной инфекции» является обнаружение антител класса G в сыворотке крови к рекомбинантному белку теплового шока – HSP60. У женщин, имеющих положительную иммунореактивность по отношению к эпитопам hsp60, установлена большая частота сальпингитов и спаек (Hjelholt A., Christiansen G., Johannesson T. et al., 2011., Ellinidi A.N., Ellinidi V.N., Davydova N.I. et al., 2007; Михнина Е.А., Давыдова Н.И., Эллиниди А.Н. и др., 2012) Михнина Е.А., 2012 г.
Cлайд 52
 Электронная микроскопия Могут обнаруживаться : гигантские ретикулярные тельца с расширенным периплазматическим пространством; деление протопласта ретикулярного тельца и отшнуровка мелких шаровидных форм в периплазматическом пространстве; мелковакуолярные включения, лежащие на периферии клеток, медленно транспортирующиеся в перинуклеарную зону; огромное количество мембранных пузырьков неправильной формы внутри ретикулярных телец. Брагина Е.Е., Дмитриев Г.А., Кисина В.И. Структурно-функциональные особенности жизненного цикла хламидий in vivo. Вестник дерматологии и венерологии 6, 1995; 18-20 Брагина Е.Е., Дмитриев Г.А. Морфологические особенности строения элементарных и ретикулярных телец хламидий при персистирующем хламидиозе. Тезисы докладов научно-практической конференции, посвященной 75-летию ЦНИКВИ. Москва, 1996; 12-13 Гомберг М.А., Соловьев А.М., Еремина О.Ф. Иммунологические подходы к лечению больных хронической персистирующей хламидийной урогенитальной инфекцией. ЗППП 4,1996; 32-37
Электронная микроскопия Могут обнаруживаться : гигантские ретикулярные тельца с расширенным периплазматическим пространством; деление протопласта ретикулярного тельца и отшнуровка мелких шаровидных форм в периплазматическом пространстве; мелковакуолярные включения, лежащие на периферии клеток, медленно транспортирующиеся в перинуклеарную зону; огромное количество мембранных пузырьков неправильной формы внутри ретикулярных телец. Брагина Е.Е., Дмитриев Г.А., Кисина В.И. Структурно-функциональные особенности жизненного цикла хламидий in vivo. Вестник дерматологии и венерологии 6, 1995; 18-20 Брагина Е.Е., Дмитриев Г.А. Морфологические особенности строения элементарных и ретикулярных телец хламидий при персистирующем хламидиозе. Тезисы докладов научно-практической конференции, посвященной 75-летию ЦНИКВИ. Москва, 1996; 12-13 Гомберг М.А., Соловьев А.М., Еремина О.Ф. Иммунологические подходы к лечению больных хронической персистирующей хламидийной урогенитальной инфекцией. ЗППП 4,1996; 32-37
Cлайд 53
 Культуральное исследование В одном пассаже на культуре клеток хламидии при персистентной инфекции, как правило, не выделяются вследствие неинфекционности и непродуктивности персистентных включений При многократном перевивании может наступить реверсия микроорганизмов с образованием типичных элементарных и ретикулярных телец в связи со снятием влияния факторов персистенции. Брагина Е.Е., Дмитриев Г.А. Морфологические особенности строения элементарных и ретикулярных телец хламидий при персистирующем хламидиозе. Тезисы докладов научно-практической конференции, посвященной 75-летию ЦНИКВИ. Москва, 1996; 12-13 Брагина Е.Е., Орлова О.Е., Дмитриев Г.А. Некоторые особенности жизненного цикла хламидий. Атипичные формы существования (обзор литературы) 3ППП 1,1998;3-9 Koehler L., Nettelnbreker E., On N., Drommer W., Zeidler Н. Persistent, nonproductive infection of human peripheral monocytes with Chlamydia trаchomatis serovar К is due to an intracellular growth arrest at an eriy stage of the chlamydial development. Abstracts of Proceedings of the 8th International Symposium of Human Chlamydial Infections. Gouvieux-Chantilly. France. 12-24 June 1994; 427-430
Культуральное исследование В одном пассаже на культуре клеток хламидии при персистентной инфекции, как правило, не выделяются вследствие неинфекционности и непродуктивности персистентных включений При многократном перевивании может наступить реверсия микроорганизмов с образованием типичных элементарных и ретикулярных телец в связи со снятием влияния факторов персистенции. Брагина Е.Е., Дмитриев Г.А. Морфологические особенности строения элементарных и ретикулярных телец хламидий при персистирующем хламидиозе. Тезисы докладов научно-практической конференции, посвященной 75-летию ЦНИКВИ. Москва, 1996; 12-13 Брагина Е.Е., Орлова О.Е., Дмитриев Г.А. Некоторые особенности жизненного цикла хламидий. Атипичные формы существования (обзор литературы) 3ППП 1,1998;3-9 Koehler L., Nettelnbreker E., On N., Drommer W., Zeidler Н. Persistent, nonproductive infection of human peripheral monocytes with Chlamydia trаchomatis serovar К is due to an intracellular growth arrest at an eriy stage of the chlamydial development. Abstracts of Proceedings of the 8th International Symposium of Human Chlamydial Infections. Gouvieux-Chantilly. France. 12-24 June 1994; 427-430
Cлайд 54
 Серологические методы Реакция непрямой гемагглютинации (РНГА) с родоспецифическим диагностикумом. У лиц с персистентной инфекцией РНГА в 4 раза превышает диагностический титр. Не менее информативна и РНИФ с типоспецифичными антигенами.
Серологические методы Реакция непрямой гемагглютинации (РНГА) с родоспецифическим диагностикумом. У лиц с персистентной инфекцией РНГА в 4 раза превышает диагностический титр. Не менее информативна и РНИФ с типоспецифичными антигенами.
Cлайд 55
 Серологические методы Уровень противохламидийных антител класса IgG оказывается в 2-4 раза выше у лиц с экстрагенитальными проявлениями хламидийной инфекции, по сравнению с группой лиц с неосложненными хламидийными уретритами Ghaem-Maghami S., Lewis D. J.„ Hay P. E. Characterisation of immune responses to human genital Chlamydial infections. Abstracts of Proceedings of the 3rd Meeting of the European Society for Chlamydial Research. Vienna. Austria. 11-14 September 1996; 81
Серологические методы Уровень противохламидийных антител класса IgG оказывается в 2-4 раза выше у лиц с экстрагенитальными проявлениями хламидийной инфекции, по сравнению с группой лиц с неосложненными хламидийными уретритами Ghaem-Maghami S., Lewis D. J.„ Hay P. E. Characterisation of immune responses to human genital Chlamydial infections. Abstracts of Proceedings of the 3rd Meeting of the European Society for Chlamydial Research. Vienna. Austria. 11-14 September 1996; 81
Cлайд 56
 Тест детекции антигена hsp 60 кДа, в связи с его гиперпродукцией при персистирующей инфекции. HSP 60 может быть наработан в инфицированной культуре клеток, инкубированных в условиях воздействия медиаторов персистенции Глазкова Л.К. Генитальная хламидийная инфекция: этиология, эпидемиология, патогенез, диагностика, клиника и терапия. // Руководство для врачей. Екатеринбург. Изд-во Урал. мед. ин-та, - 2004.
Тест детекции антигена hsp 60 кДа, в связи с его гиперпродукцией при персистирующей инфекции. HSP 60 может быть наработан в инфицированной культуре клеток, инкубированных в условиях воздействия медиаторов персистенции Глазкова Л.К. Генитальная хламидийная инфекция: этиология, эпидемиология, патогенез, диагностика, клиника и терапия. // Руководство для врачей. Екатеринбург. Изд-во Урал. мед. ин-та, - 2004.
Cлайд 58
 «Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»?
«Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»?
Cлайд 59
 «Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»? Каковы клинические проявления хронического воспалительного процесса при хронически протекающей хламидийной инфекции?
«Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»? Каковы клинические проявления хронического воспалительного процесса при хронически протекающей хламидийной инфекции?
Cлайд 60
 «Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»? Каковы клинические проявления хронического воспалительного процесса при хронически протекающей хламидийной инфекции? Каковы критерии лабораторной диагностики «персистирующей хламидийной инфекции»?
«Персистирующая хламидийная инфекция» Существует ли такой диагноз в МКБ? Каковы клинические проявления «персистирующей хламидийной инфекции»? Каковы клинические проявления хронического воспалительного процесса при хронически протекающей хламидийной инфекции? Каковы критерии лабораторной диагностики «персистирующей хламидийной инфекции»?
Cлайд 61
 Вопросы терапии Аберантные (персистирующие) формы хламидий не реагируют на антибиотик так, как нормально развивающиеся тельца. Аберрантные (персистирующие) формы С.trachomatis имеют сниженное количество МОМР. А МОМР действует не только как антиген, но также как и пора в клеточной стенке. В отсутствии МОМР большие гидрофильные молекулы, включая также и многие антибиотики, не транспортируются внутрь хламидий Битти В.Л., Моррисон Р.П., Бирн Д.И. Персистенция хламидий: от клеточных культур до патогенеза хламидийной инфекции. ЗППП 6,1995; 3-18
Вопросы терапии Аберантные (персистирующие) формы хламидий не реагируют на антибиотик так, как нормально развивающиеся тельца. Аберрантные (персистирующие) формы С.trachomatis имеют сниженное количество МОМР. А МОМР действует не только как антиген, но также как и пора в клеточной стенке. В отсутствии МОМР большие гидрофильные молекулы, включая также и многие антибиотики, не транспортируются внутрь хламидий Битти В.Л., Моррисон Р.П., Бирн Д.И. Персистенция хламидий: от клеточных культур до патогенеза хламидийной инфекции. ЗППП 6,1995; 3-18
Cлайд 62
 …для эффективного лечения персистирующей хламидийной инфекции необходимо подключить патогенетическую терапию, а так как основная роль принадлежит иммунопатологическим механизмам, то взгляд исследователей был обращен в сторону иммуномодуляторов НО… Иммуномодуляторы могут привести к реверсии форм хламидий или восстановить нормальный синтез клеточной стенки хламидий ?????? Вопросы терапии Л.К Глазкова, О.Е. Акилов. Практические аспекты персистирующей хламидийной инфекции/ Русский медицинский сервер
…для эффективного лечения персистирующей хламидийной инфекции необходимо подключить патогенетическую терапию, а так как основная роль принадлежит иммунопатологическим механизмам, то взгляд исследователей был обращен в сторону иммуномодуляторов НО… Иммуномодуляторы могут привести к реверсии форм хламидий или восстановить нормальный синтез клеточной стенки хламидий ?????? Вопросы терапии Л.К Глазкова, О.Е. Акилов. Практические аспекты персистирующей хламидийной инфекции/ Русский медицинский сервер
Cлайд 63
 Критерии эффективности лечения Эффективность иммунотерапии по данным литературы : 69% больных излечиваются (у них не обнаруживаются ЭТ и мелкие цитоплазматические включения) у 23% наблюдается неэффективность проводимой терапии (наличие мелких цитоплазматических включений) у 8% выявляются обычные формы Chlamydia trachomatis, то есть происходит реверсия микроорганизмов. В этом случае необходимо проведение стандартного курса антибиотикотерапии. Гомберг М.А., Соловьев А.М., Еремина О.Ф. Иммунологические подходы к лечению больных хронической персистирующей хламидийной урогенитальной инфекцией. ЗППП 4,1996; 32-37
Критерии эффективности лечения Эффективность иммунотерапии по данным литературы : 69% больных излечиваются (у них не обнаруживаются ЭТ и мелкие цитоплазматические включения) у 23% наблюдается неэффективность проводимой терапии (наличие мелких цитоплазматических включений) у 8% выявляются обычные формы Chlamydia trachomatis, то есть происходит реверсия микроорганизмов. В этом случае необходимо проведение стандартного курса антибиотикотерапии. Гомберг М.А., Соловьев А.М., Еремина О.Ф. Иммунологические подходы к лечению больных хронической персистирующей хламидийной урогенитальной инфекцией. ЗППП 4,1996; 32-37
Cлайд 64
 Тактика некоторых специалистов …….на сегодняшний день мы считаем, что длительный контроль и наблюдение - это принципы тактики ведения больных с урогенитальной «персистентной хламидийной инфекцией». При отсутствии признаков реверсии всем больным через 1,5-2 месяца после первичного обследования следует провести контрольное культуральное исследование на хламидий, а также исследовать состояние иммунной системы. Л.К Глазкова, О.Е. Акилов. Практические аспекты персистирующей хламидийной инфекции/ Русский медицинский сервер
Тактика некоторых специалистов …….на сегодняшний день мы считаем, что длительный контроль и наблюдение - это принципы тактики ведения больных с урогенитальной «персистентной хламидийной инфекцией». При отсутствии признаков реверсии всем больным через 1,5-2 месяца после первичного обследования следует провести контрольное культуральное исследование на хламидий, а также исследовать состояние иммунной системы. Л.К Глазкова, О.Е. Акилов. Практические аспекты персистирующей хламидийной инфекции/ Русский медицинский сервер
Cлайд 65
 Аберрантные (персистентные) формы хламидий – способ выживания микроорганизма в определенных условиях. Спонтанное разрешение хламидийного процесса наблюдается в 20% случаев. При отсутствии клинических признаков воспалительного процесса и наличии неких результатов нерегламентированных лабораторных методов обнаружения аберрантных форм хламидий … Должна ли тактика врача в таких случаях быть агрессивной?
Аберрантные (персистентные) формы хламидий – способ выживания микроорганизма в определенных условиях. Спонтанное разрешение хламидийного процесса наблюдается в 20% случаев. При отсутствии клинических признаков воспалительного процесса и наличии неких результатов нерегламентированных лабораторных методов обнаружения аберрантных форм хламидий … Должна ли тактика врача в таких случаях быть агрессивной?
Cлайд 66
 Заключение Основной подход к диагностике урогенитальной хламидийной инфекции – методы амплификации нуклеиновых кислот Серологические методы являются дополнительными при подозрении на восходящую инфекцию В настоящее время не существует универсальных маркеров «персистирующей хламидийной инфекции», которые могли бы использоваться в диагностике На сегодняшний день нет убедительных данных, обосновывающих необходимость изменения существующих схем диагностики и терапии хламидийной инфекции
Заключение Основной подход к диагностике урогенитальной хламидийной инфекции – методы амплификации нуклеиновых кислот Серологические методы являются дополнительными при подозрении на восходящую инфекцию В настоящее время не существует универсальных маркеров «персистирующей хламидийной инфекции», которые могли бы использоваться в диагностике На сегодняшний день нет убедительных данных, обосновывающих необходимость изменения существующих схем диагностики и терапии хламидийной инфекции