X
Код презентации скопируйте его
Неметаллы. Общая характеристика
Скачать эту презентациюПрезентация на тему Неметаллы. Общая характеристика
Скачать эту презентациюCлайд 2
 Неметаллы Общая характеристика Кислород и кремний составляют 76% от массы земной коры (О – 49%, Si – 27%) C,H,O,N,P,S – биогенные элементы, составляют 98,5% от массы растений и 97,6% от массы тела человека
Неметаллы Общая характеристика Кислород и кремний составляют 76% от массы земной коры (О – 49%, Si – 27%) C,H,O,N,P,S – биогенные элементы, составляют 98,5% от массы растений и 97,6% от массы тела человека
Cлайд 3
 Неметаллы Общая характеристика В состав земной атмосферы входят простые и сложные вещества, образованные элементами-неметаллами (N2-75,5%, O2-23,2%, а также CO2,H2O и др.) Водород – главный элемент Вселенной (Солнце и другие звёзды, газовые облака и т.д.) Из каждых 100 атомов на Земле 17 – это атомы водорода.
Неметаллы Общая характеристика В состав земной атмосферы входят простые и сложные вещества, образованные элементами-неметаллами (N2-75,5%, O2-23,2%, а также CO2,H2O и др.) Водород – главный элемент Вселенной (Солнце и другие звёзды, газовые облака и т.д.) Из каждых 100 атомов на Земле 17 – это атомы водорода.
Cлайд 4
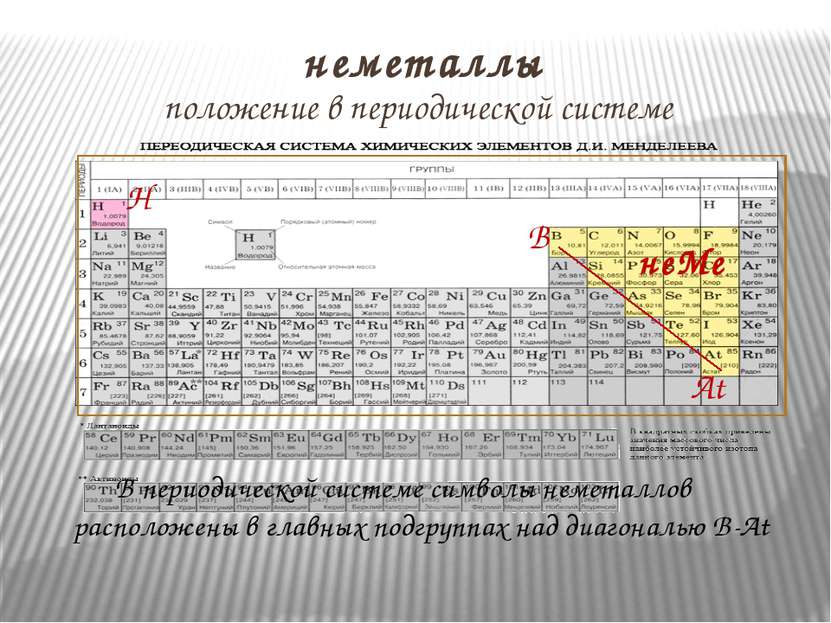
 положение в периодической системе неметаллы B At H неМе В периодической системе символы неметаллов расположены в главных подгруппах над диагональю B-At
положение в периодической системе неметаллы B At H неМе В периодической системе символы неметаллов расположены в главных подгруппах над диагональю B-At
Cлайд 5
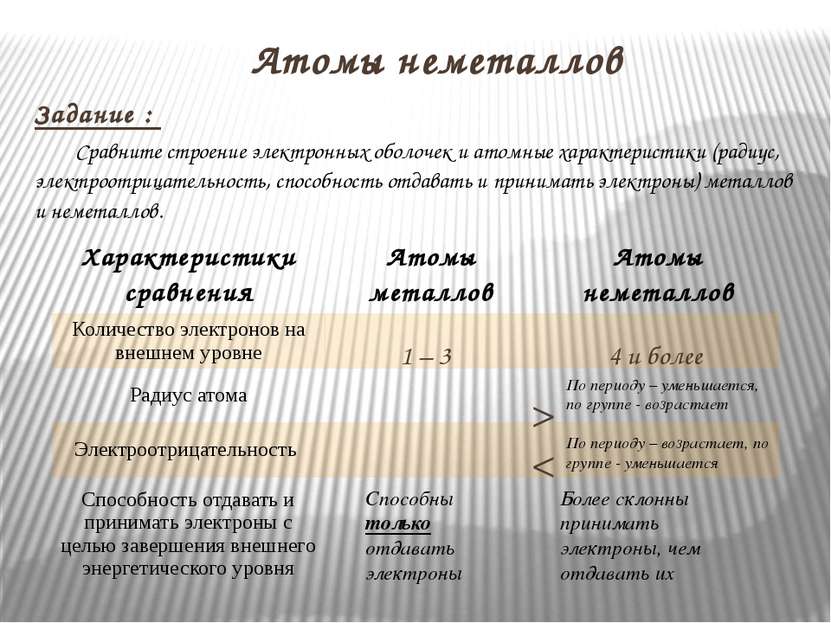
 Задание : Сравните строение электронных оболочек и атомные характеристики (радиус, электроотрицательность, способность отдавать и принимать электроны) металлов и неметаллов. 1 – 3 4 и более > < Атомы неметаллов Способны только отдавать электроны Более склонны принимать электроны, чем отдавать их По периоду – уменьшается, по группе - возрастает По периоду – возрастает, по группе - уменьшается Характеристики сравнения Атомы металлов Атомы неметаллов Количество электронов на внешнем уровне Радиус атома Электроотрицательность Способность отдавать и принимать электроны с целью завершения внешнего энергетического уровня
Задание : Сравните строение электронных оболочек и атомные характеристики (радиус, электроотрицательность, способность отдавать и принимать электроны) металлов и неметаллов. 1 – 3 4 и более > < Атомы неметаллов Способны только отдавать электроны Более склонны принимать электроны, чем отдавать их По периоду – уменьшается, по группе - возрастает По периоду – возрастает, по группе - уменьшается Характеристики сравнения Атомы металлов Атомы неметаллов Количество электронов на внешнем уровне Радиус атома Электроотрицательность Способность отдавать и принимать электроны с целью завершения внешнего энергетического уровня
Cлайд 6
 Простые вещества - неметаллы строение Химическая связь – ковалентная неполярная: Образуется при помощи общих электронных пар; Обобществлённые электроны в равной степени принадлежат связываемым атомам. Задание : Определите вид химической связи в молекулах N2, O2, Cl2, составьте схемы её образования, укажите её особенности
Простые вещества - неметаллы строение Химическая связь – ковалентная неполярная: Образуется при помощи общих электронных пар; Обобществлённые электроны в равной степени принадлежат связываемым атомам. Задание : Определите вид химической связи в молекулах N2, O2, Cl2, составьте схемы её образования, укажите её особенности
Cлайд 7
 Задание : Распределите вещества C, N2,O2, Si, Br2,I2 на две группы на основании данных об агрегатных состояниях и температурах кипения, определите причину различия в свойствах: O2, N2, Br2, I2 C, Si молекулярная крист. решётка атомная крист. решётка Простые вещества - неметаллы строение и физические свойства Газообразные или легколетучие вещества с низкими температурами плавления Твердые нелетучие вещества с высокими температурами плавления
Задание : Распределите вещества C, N2,O2, Si, Br2,I2 на две группы на основании данных об агрегатных состояниях и температурах кипения, определите причину различия в свойствах: O2, N2, Br2, I2 C, Si молекулярная крист. решётка атомная крист. решётка Простые вещества - неметаллы строение и физические свойства Газообразные или легколетучие вещества с низкими температурами плавления Твердые нелетучие вещества с высокими температурами плавления
Cлайд 8
 Простые вещества – неметаллы химические свойства ВЗАИМОДЕЙСТВИЕ АЛЮМИНИЯ С ЙОДОМ ГОРЕНИЕ ФОСФОРА В КИСЛОРОДЕ
Простые вещества – неметаллы химические свойства ВЗАИМОДЕЙСТВИЕ АЛЮМИНИЯ С ЙОДОМ ГОРЕНИЕ ФОСФОРА В КИСЛОРОДЕ
Cлайд 9
 Задание : Запишите уравнения реакций, расставьте степени окисления элементов в веществах, составьте электронный баланс или покажите при помощи стрелки переход электронов, укажите окислитель и восстановитель: 2Al0 + 3I20 = 2Al+3I3-1 ē восстановитель окислитель 4P0 + 5O20 = 2P2+5O5-2 ē восстановитель окислитель Простые вещества – неметаллы химические свойства
Задание : Запишите уравнения реакций, расставьте степени окисления элементов в веществах, составьте электронный баланс или покажите при помощи стрелки переход электронов, укажите окислитель и восстановитель: 2Al0 + 3I20 = 2Al+3I3-1 ē восстановитель окислитель 4P0 + 5O20 = 2P2+5O5-2 ē восстановитель окислитель Простые вещества – неметаллы химические свойства
Cлайд 10
 Подведём итоги Символы неМе расположены в периодической системе в главных подгруппах над диагональю B-At. На внешнем энергетическом уровне содержат от 4 до 8 электронов; имеют меньший радиус и более высокую электроотрицательность, чем атомы металлов. Простые вещества-неметаллы образованы при помощи ковалентной неполярной химической связи, могут иметь атомную или молекулярную кристаллическую решётку. В химических реакциях способны выступать как окислителями, так и восстановителями.
Подведём итоги Символы неМе расположены в периодической системе в главных подгруппах над диагональю B-At. На внешнем энергетическом уровне содержат от 4 до 8 электронов; имеют меньший радиус и более высокую электроотрицательность, чем атомы металлов. Простые вещества-неметаллы образованы при помощи ковалентной неполярной химической связи, могут иметь атомную или молекулярную кристаллическую решётку. В химических реакциях способны выступать как окислителями, так и восстановителями.