X
Код презентации скопируйте его
Парообразование
Скачать эту презентациюПрезентация на тему Парообразование
Скачать эту презентациюCлайд 1
 Презентация учителя физики МОУ СОШ № 288 г. Заозерска Мурманской области Бельтюковой Светланы Викторовны
Презентация учителя физики МОУ СОШ № 288 г. Заозерска Мурманской области Бельтюковой Светланы Викторовны
Cлайд 2
 Подумай… 1. Чем отличаются молекулы холодной и горячей воды? 2. Изменяется ли температура в процессе плавления? Почему? 3. Изменяется ли объем в процессе плавления? 4.Чем твердое состояние вещества от газообразного? 5.Как называется процесс перехода вещества из газообразного состояния в жидкое?
Подумай… 1. Чем отличаются молекулы холодной и горячей воды? 2. Изменяется ли температура в процессе плавления? Почему? 3. Изменяется ли объем в процессе плавления? 4.Чем твердое состояние вещества от газообразного? 5.Как называется процесс перехода вещества из газообразного состояния в жидкое?
Cлайд 3
 Проверь себя: 1. Молекулы холодной и горячей воды отличаются только скоростью движения и расстоянием между ними. 2. Температура в процессе плавления не изменяется, т.к. поступающая теплота идет на разрушение кристаллической решетки и увеличение кинетической энергии молекул. 3. В процессе плавления объем незначительно увеличивается у всех веществ, кроме воды. 4. Твердое состояние вещества от газообразного отличается скоростью и видом движения молекул (в газе движение хаотичное, в твердых телах – колебательное и вращательное), а также характером расположения молекул (в газах молекулы расположены на большом расстоянии друг от друга и при этом постоянно движутся поступательно, а в твердых телах молекулы расположены близко друг к другу, и не могут покинуть свое место) 5. Процесс перехода вещества из газообразного состояния в жидкое называется конденсацией.
Проверь себя: 1. Молекулы холодной и горячей воды отличаются только скоростью движения и расстоянием между ними. 2. Температура в процессе плавления не изменяется, т.к. поступающая теплота идет на разрушение кристаллической решетки и увеличение кинетической энергии молекул. 3. В процессе плавления объем незначительно увеличивается у всех веществ, кроме воды. 4. Твердое состояние вещества от газообразного отличается скоростью и видом движения молекул (в газе движение хаотичное, в твердых телах – колебательное и вращательное), а также характером расположения молекул (в газах молекулы расположены на большом расстоянии друг от друга и при этом постоянно движутся поступательно, а в твердых телах молекулы расположены близко друг к другу, и не могут покинуть свое место) 5. Процесс перехода вещества из газообразного состояния в жидкое называется конденсацией.
Cлайд 4
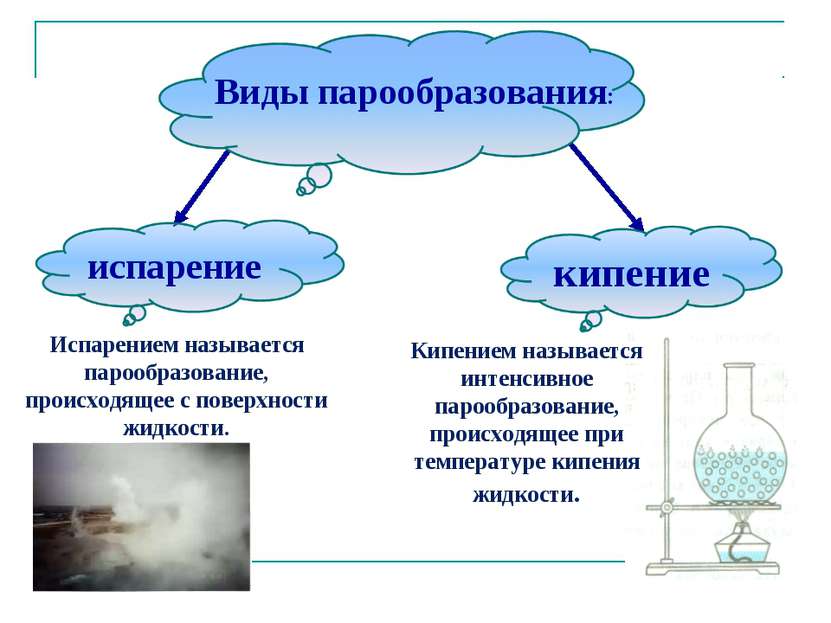
 Испарением называется парообразование, происходящее с поверхности жидкости. Кипением называется интенсивное парообразование, происходящее при температуре кипения жидкости. Виды парообразования:
Испарением называется парообразование, происходящее с поверхности жидкости. Кипением называется интенсивное парообразование, происходящее при температуре кипения жидкости. Виды парообразования:
Cлайд 5
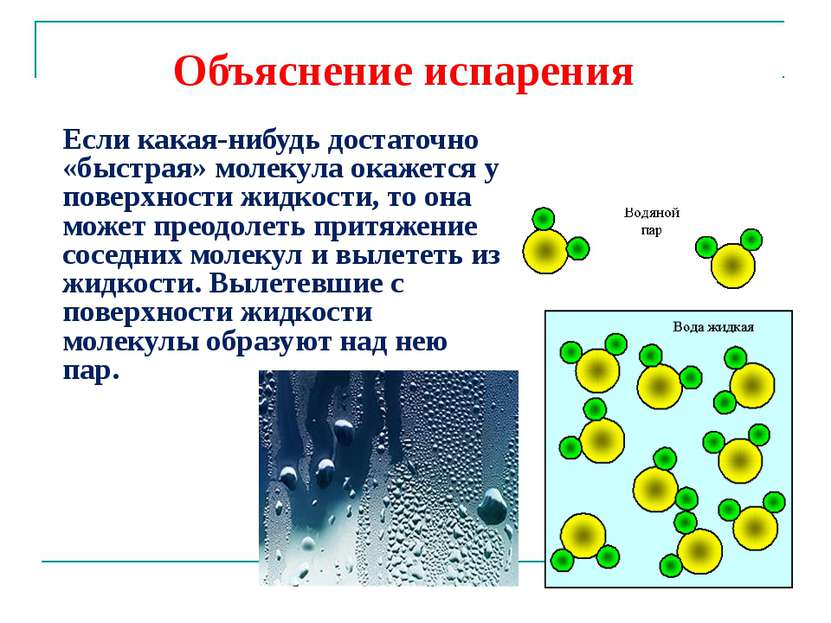
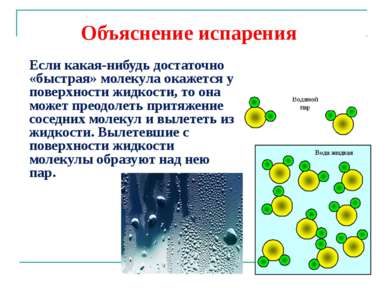 Объяснение испарения Если какая-нибудь достаточно «быстрая» молекула окажется у поверхности жидкости, то она может преодолеть притяжение соседних молекул и вылететь из жидкости. Вылетевшие с поверхности жидкости молекулы образуют над нею пар.
Объяснение испарения Если какая-нибудь достаточно «быстрая» молекула окажется у поверхности жидкости, то она может преодолеть притяжение соседних молекул и вылететь из жидкости. Вылетевшие с поверхности жидкости молекулы образуют над нею пар.
Cлайд 7
 Объяснение кипения При нагревании в жидкости появляются мелкие пузырьки, количество которых быстро растёт. Это пузырьки воздуха, который всегда бывает растворён в воде. Они также содержат и водяной пар. С ростом температуры пузырьки поднимаются на поверхность жидкости, их объём при этом увеличивается. На поверхности они лопаются, и находящийся в них водяной пар выходит в атмосферу – жидкость кипит.
Объяснение кипения При нагревании в жидкости появляются мелкие пузырьки, количество которых быстро растёт. Это пузырьки воздуха, который всегда бывает растворён в воде. Они также содержат и водяной пар. С ростом температуры пузырьки поднимаются на поверхность жидкости, их объём при этом увеличивается. На поверхности они лопаются, и находящийся в них водяной пар выходит в атмосферу – жидкость кипит.
Cлайд 8
 Особенности кипения 1.Кипение всегда происходит при определенной для каждого вещества температуре – температуре кипения. 2.Во время кипения температура жидкости не изменяется. 3.Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости.
Особенности кипения 1.Кипение всегда происходит при определенной для каждого вещества температуре – температуре кипения. 2.Во время кипения температура жидкости не изменяется. 3.Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости.
Cлайд 9
 Расчёт количества теплоты Количество теплоты, необходимое для парообразования, зависит от рода вещества и его массы: Q = L m L- удельная теплота парообразования ( табл.) Количество теплоты, которое затрачивается для перевода жидкости в пар, выделяется в процессе конденсации жидкости из пара.
Расчёт количества теплоты Количество теплоты, необходимое для парообразования, зависит от рода вещества и его массы: Q = L m L- удельная теплота парообразования ( табл.) Количество теплоты, которое затрачивается для перевода жидкости в пар, выделяется в процессе конденсации жидкости из пара.
Cлайд 10
 Какое количество теплоты требуется для испарения 200 г воды, взятой при температуре 200С? В задаче описано два процесса: сначала воду следует нагреть до температуры кипения, затем – испарить. Дано: СИ: Решение: m = 200 г 0,2 кг Q = Q1 + Q2 t1 = 200С Q1 = m c (t2 – t1) t2 = 1000С Q2 = m L с = 4200 Дж/кг0С Q = m c (t2 – t1) + m L L = 2,3·106 МДж/кг Q = m (c (t2 – t1) + L) Q - ? Q = 0,2 (4200(100-20)+ 2,3·106) Q = 527200 Дж = 527,2 кДж Ответ: Q = 527,2 кДж
Какое количество теплоты требуется для испарения 200 г воды, взятой при температуре 200С? В задаче описано два процесса: сначала воду следует нагреть до температуры кипения, затем – испарить. Дано: СИ: Решение: m = 200 г 0,2 кг Q = Q1 + Q2 t1 = 200С Q1 = m c (t2 – t1) t2 = 1000С Q2 = m L с = 4200 Дж/кг0С Q = m c (t2 – t1) + m L L = 2,3·106 МДж/кг Q = m (c (t2 – t1) + L) Q - ? Q = 0,2 (4200(100-20)+ 2,3·106) Q = 527200 Дж = 527,2 кДж Ответ: Q = 527,2 кДж
Cлайд 11
 1. Какое количество теплоты требуется для испарения 20 г эфира, взятого при температуре кипения? 2. Какое количество теплоты требуется для плавления 200 г свинца, взятого при температуре 270С? 3.Какое количество теплоты потребуется для получения изо льда при температуре -50С воды при температуре 200С?
1. Какое количество теплоты требуется для испарения 20 г эфира, взятого при температуре кипения? 2. Какое количество теплоты требуется для плавления 200 г свинца, взятого при температуре 270С? 3.Какое количество теплоты потребуется для получения изо льда при температуре -50С воды при температуре 200С?