X
Код презентации скопируйте его
Строение атома. Опыты Резерфорда
Скачать эту презентациюПрезентация на тему Строение атома. Опыты Резерфорда
Скачать эту презентациюCлайд 1
 Манаева Юлия Александровна МОУ Мирновская СОШ На краю Млечного Пути, вокруг звезды средней величины, вращается голубой шар. Это – Земля, а голубизна – Океан. На планете много веществ и различных химических элементов, которые отличаются друг от друга мельчайшими частицами, именуемыми молекулами и атомами.
Манаева Юлия Александровна МОУ Мирновская СОШ На краю Млечного Пути, вокруг звезды средней величины, вращается голубой шар. Это – Земля, а голубизна – Океан. На планете много веществ и различных химических элементов, которые отличаются друг от друга мельчайшими частицами, именуемыми молекулами и атомами.
Cлайд 2
 Уильям Блейк (1757-1827) Манаева Юлия Александровна МОУ МИрновская СОШ Английский поэт и художник Уильям Блейк (1757-1827)в своем стихотворении призывал
Уильям Блейк (1757-1827) Манаева Юлия Александровна МОУ МИрновская СОШ Английский поэт и художник Уильям Блейк (1757-1827)в своем стихотворении призывал
Cлайд 3
 Уильям Блейк (1757-1827) В одном мгновенье видеть вечность, Огромный мир – в зерне песка, В единой горсти – бесконечность И небо - в чашечке цветка. Манаева Юлия Александровна МОУ МИрновская СОШ Оказывается, любая песчинка – действительно, целая Вселенная, ибо включает в себя почти столько же мельчайших частиц, сколько звезд содержится во всей Метагалактике. Из этих частиц состоит и камень, одиноко лежащий на обочине дороги, и маленький цветок, радующий нас своей красотой, и пушистые облака, неторопливо плывущие по голубому небу. Скажите, а как бы вы, своим сверстникам, таким же подросткам как и вы, только жившим в 5 в. до н.э. смогли бы объяснить этот факт? Какие явления доказывают нам, что любое тело состоит из частиц? Совершенно верно, это и диффузия, и броуновское движение. “Что такое эти атомы и молекулы? Как они устроены? ” – эти вопросы давно задавал себе человек. И искал ответы.
Уильям Блейк (1757-1827) В одном мгновенье видеть вечность, Огромный мир – в зерне песка, В единой горсти – бесконечность И небо - в чашечке цветка. Манаева Юлия Александровна МОУ МИрновская СОШ Оказывается, любая песчинка – действительно, целая Вселенная, ибо включает в себя почти столько же мельчайших частиц, сколько звезд содержится во всей Метагалактике. Из этих частиц состоит и камень, одиноко лежащий на обочине дороги, и маленький цветок, радующий нас своей красотой, и пушистые облака, неторопливо плывущие по голубому небу. Скажите, а как бы вы, своим сверстникам, таким же подросткам как и вы, только жившим в 5 в. до н.э. смогли бы объяснить этот факт? Какие явления доказывают нам, что любое тело состоит из частиц? Совершенно верно, это и диффузия, и броуновское движение. “Что такое эти атомы и молекулы? Как они устроены? ” – эти вопросы давно задавал себе человек. И искал ответы.
Cлайд 4
 В поисках атома… Манаева Юлия Александровна МОУ МИрновская СОШ В истории развития физики одна из самых интересных и увлекательных страниц – это история открытия сложного строения атома. В конце XIX- начале XX в. идеи о строении атома витали в воздухе, различные догадки ученых создавали духовную атмосферу, в которой, в конце концов, и рождалось открытие, ведь в то время ничего о внутреннем строении атома не было известно.
В поисках атома… Манаева Юлия Александровна МОУ МИрновская СОШ В истории развития физики одна из самых интересных и увлекательных страниц – это история открытия сложного строения атома. В конце XIX- начале XX в. идеи о строении атома витали в воздухе, различные догадки ученых создавали духовную атмосферу, в которой, в конце концов, и рождалось открытие, ведь в то время ничего о внутреннем строении атома не было известно.
Cлайд 5
 По легенде Демокрит сидел на берегу реки и собирался съесть яблоко и для этого разрезал его на две части, затем он разрезал каждую часть ещё на две. До каких пор можно рассекать яблоко на части? Задумался Демокрит. Мысль о том, что существует предел такого деления, и побудила назвать мельчайшие частицы материи атомами – неделимыми. Демокрит ок. 460 - 370 до н. э. Атом – мельчайшая частица вещества «неделимый» Манаева Юлия Александровна МОУ МИрновская СОШ Гипотеза о существовании атомов так же стара, как и наша цивилизация. Понятие атома существует уже по крайней мере 25 столетий, а придумал его греческий философ, мыслитель Демокрит, атом – «неделимый».
По легенде Демокрит сидел на берегу реки и собирался съесть яблоко и для этого разрезал его на две части, затем он разрезал каждую часть ещё на две. До каких пор можно рассекать яблоко на части? Задумался Демокрит. Мысль о том, что существует предел такого деления, и побудила назвать мельчайшие частицы материи атомами – неделимыми. Демокрит ок. 460 - 370 до н. э. Атом – мельчайшая частица вещества «неделимый» Манаева Юлия Александровна МОУ МИрновская СОШ Гипотеза о существовании атомов так же стара, как и наша цивилизация. Понятие атома существует уже по крайней мере 25 столетий, а придумал его греческий философ, мыслитель Демокрит, атом – «неделимый».
Cлайд 6
 Михаил Васильевич Ломоносов (1711-1765) Различая два вида частиц материи, он дает им названия “элементы” (равные понятию “атом”) и “корпускулы” (равные понятию “молекула”). Манаева Юлия Александровна МОУ МИрновская СОШ В России идеи о мельчайших частицах вещества развивал Михаил Васильевич Ломоносов (1711-1765). Различая два вида частиц материи, он дает им названия “элементы” (равные понятию “атом”) и “корпускулы” (равные понятию “молекула”). Так, медленно, но верно подкрался XIX век, вместе со своими догадками, терзаниями и открытиями.
Михаил Васильевич Ломоносов (1711-1765) Различая два вида частиц материи, он дает им названия “элементы” (равные понятию “атом”) и “корпускулы” (равные понятию “молекула”). Манаева Юлия Александровна МОУ МИрновская СОШ В России идеи о мельчайших частицах вещества развивал Михаил Васильевич Ломоносов (1711-1765). Различая два вида частиц материи, он дает им названия “элементы” (равные понятию “атом”) и “корпускулы” (равные понятию “молекула”). Так, медленно, но верно подкрался XIX век, вместе со своими догадками, терзаниями и открытиями.
Cлайд 7
 Джозеф Джон Томсон (1856-1940) 1937 год – открытие электрона Атом имеет сложную структуру Манаева Юлия Александровна МОУ МИрновская СОШ 1987 год стал отправной точкой в развитии теории строения атома. Именно тогда английский физик Джозеф ДжонТомсон (1856-1940) проводит эксперимент, в ходе которого открывает электрон. После открытия в 1897 году электрона, входящего в состав атома, был сделан вывод о сложном строении атома.
Джозеф Джон Томсон (1856-1940) 1937 год – открытие электрона Атом имеет сложную структуру Манаева Юлия Александровна МОУ МИрновская СОШ 1987 год стал отправной точкой в развитии теории строения атома. Именно тогда английский физик Джозеф ДжонТомсон (1856-1940) проводит эксперимент, в ходе которого открывает электрон. После открытия в 1897 году электрона, входящего в состав атома, был сделан вывод о сложном строении атома.
Cлайд 8
 Атом – это однородный шар из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду атома, следовательно, атом имеет заряд равный нулю. Пудинг с изюмом – первая модель атома Манаева Юлия Александровна МОУ МИрновская СОШ Первая достаточно разработанная модель атома была предложена английским физиком Дж. Дж. Томсоном в 1903 году. Ее назвали – “пудинг”, начиненный изюмом, где атом – это однородный шар из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду атома, следовательно, атом имеет заряд равный нулю. Для устойчивости атома необходимо, чтобы электроны располагались концентрическими слоями, в каждом слое определенное число электронов. Томсон с помощью данной модели объяснил ряд физических явлений.
Атом – это однородный шар из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду атома, следовательно, атом имеет заряд равный нулю. Пудинг с изюмом – первая модель атома Манаева Юлия Александровна МОУ МИрновская СОШ Первая достаточно разработанная модель атома была предложена английским физиком Дж. Дж. Томсоном в 1903 году. Ее назвали – “пудинг”, начиненный изюмом, где атом – это однородный шар из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду атома, следовательно, атом имеет заряд равный нулю. Для устойчивости атома необходимо, чтобы электроны располагались концентрическими слоями, в каждом слое определенное число электронов. Томсон с помощью данной модели объяснил ряд физических явлений.
Cлайд 9
 Согласны ли вы с этой моделью? Ваша версия строения атома? Манаева Юлия Александровна МОУ МИрновская СОШ
Согласны ли вы с этой моделью? Ваша версия строения атома? Манаева Юлия Александровна МОУ МИрновская СОШ
Cлайд 10
 Главное, нужно было найти чем «прощупать этот атом». И такой щуп был найден - он решил проникнуть внутрь атома с помощью α-частиц, которые имели положительный заряд, массу почти в 7300 раз большую чем масса электрона и очень большую скорость (около 20000км/c). С точки зрения Резерфорда α-частицы должны были легко «пробить» атом и тем самым доказать справедливость модели атома Томсона. Если бы атом был устроен так, как предполагал Дж.Томсон, то Э.Резерфорд увидел бы следующую картину: α- частицы пробивают атом и практически не отклоняясь пролетают сквозь него. Эрнест Резерфорд(1871-1937 гг.) Манаева Юлия Александровна МОУ МИрновская СОШ Модель Томсона нуждалась в экспериментальной проверке. Этой задачей занялся Эрнест Резерфорд(1871-1937 гг.) – английский ученый, ученик Томсона, известный своими исследованиями строения атома и радиоактивности, один из создателей атомной и ядерной физики. Главне, нужно было найти чем «прощупать этот атом». И аткой щуп был найден - он решил проникнуть внутрь атома с помощью α-частиц, которые имели положительный заряд, массу почти в 7300 раз большую чем масса электрона и очень большую скорость (около 20000км/c). С точки зрения Резерфорда α-частицы должны были легко «пробить» атом и тем самым доказать справедливость модели атома Томсона.
Главное, нужно было найти чем «прощупать этот атом». И такой щуп был найден - он решил проникнуть внутрь атома с помощью α-частиц, которые имели положительный заряд, массу почти в 7300 раз большую чем масса электрона и очень большую скорость (около 20000км/c). С точки зрения Резерфорда α-частицы должны были легко «пробить» атом и тем самым доказать справедливость модели атома Томсона. Если бы атом был устроен так, как предполагал Дж.Томсон, то Э.Резерфорд увидел бы следующую картину: α- частицы пробивают атом и практически не отклоняясь пролетают сквозь него. Эрнест Резерфорд(1871-1937 гг.) Манаева Юлия Александровна МОУ МИрновская СОШ Модель Томсона нуждалась в экспериментальной проверке. Этой задачей занялся Эрнест Резерфорд(1871-1937 гг.) – английский ученый, ученик Томсона, известный своими исследованиями строения атома и радиоактивности, один из создателей атомной и ядерной физики. Главне, нужно было найти чем «прощупать этот атом». И аткой щуп был найден - он решил проникнуть внутрь атома с помощью α-частиц, которые имели положительный заряд, массу почти в 7300 раз большую чем масса электрона и очень большую скорость (около 20000км/c). С точки зрения Резерфорда α-частицы должны были легко «пробить» атом и тем самым доказать справедливость модели атома Томсона.
Cлайд 11
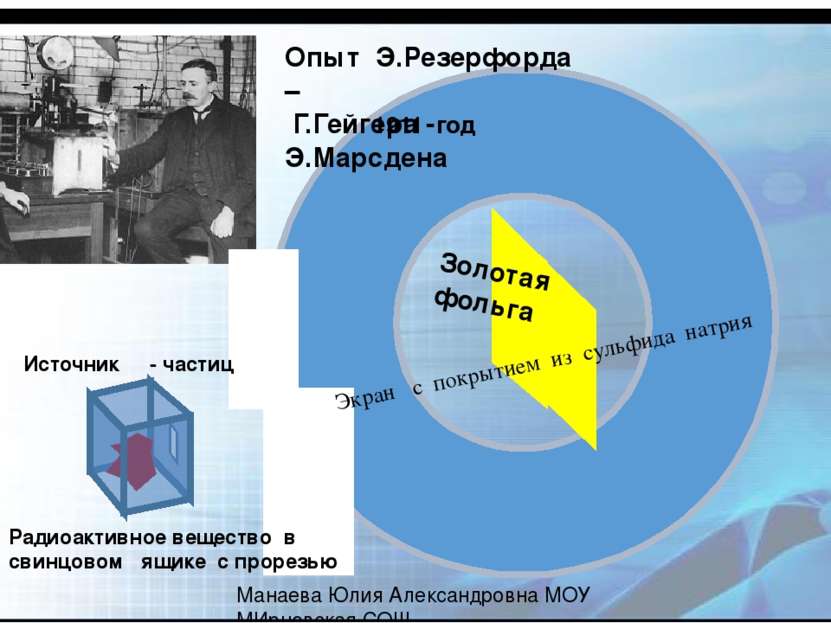
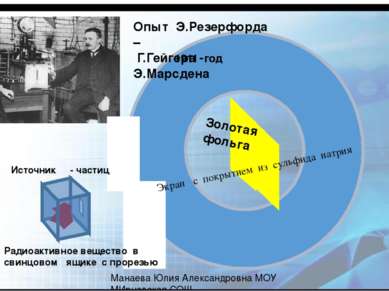 Опыт Э.Резерфорда – Г.Гейгера - Э.Марсдена Радиоактивное вещество в свинцовом ящике с прорезью Золотая фольга Экран с покрытием из сульфида натрия Источник α - частиц 1911 год Манаева Юлия Александровна МОУ МИрновская СОШ Схему экспериментальной установки Резерфорда вы видите на рисунке. В цилиндрическом сосуде с небольшим отверстием находился радиоактивный препарат, испускавший поток α-частиц. Они попадали на золотую фольгу и, проходя через нее, ударялись о люминесцирующий экран. В местах удара частиц на экране возникали вспышки света.
Опыт Э.Резерфорда – Г.Гейгера - Э.Марсдена Радиоактивное вещество в свинцовом ящике с прорезью Золотая фольга Экран с покрытием из сульфида натрия Источник α - частиц 1911 год Манаева Юлия Александровна МОУ МИрновская СОШ Схему экспериментальной установки Резерфорда вы видите на рисунке. В цилиндрическом сосуде с небольшим отверстием находился радиоактивный препарат, испускавший поток α-частиц. Они попадали на золотую фольгу и, проходя через нее, ударялись о люминесцирующий экран. В местах удара частиц на экране возникали вспышки света.
Cлайд 13
 Эрнест Резерфорд(1871-1937 гг.) Результаты эксперимента настолько удивили Резерфорда, что он воскликнул: "... неправдоподобно так же, как если бы вы выстрелили пятнадцатифунтовым снарядом в папиросную бумагу, а снаряд отскочил бы обратно и убил бы вас самих". Манаева Юлия Александровна МОУ МИрновская СОШ То, что некоторые α-частицы отскакивали от фольги назад, противоречило модели Томсона. Результаты эксперимента настолько удивили Резерфорда, что он воскликнул: "... неправдоподобно так же, как если бы вы выстрелили пятнадцатифунтовым снарядом в папиросную бумагу, а снаряд отскочил бы обратно и убил бы вас самих". Частицы возвращались редко: в среднем одна частица из восьми тысяч. Отражение от мишени означало, что частица встретила на пути достойную преграду – массивную и положительно заряженную: только такая может с силой оттолкнуть от себя прилетевшую гостью.
Эрнест Резерфорд(1871-1937 гг.) Результаты эксперимента настолько удивили Резерфорда, что он воскликнул: "... неправдоподобно так же, как если бы вы выстрелили пятнадцатифунтовым снарядом в папиросную бумагу, а снаряд отскочил бы обратно и убил бы вас самих". Манаева Юлия Александровна МОУ МИрновская СОШ То, что некоторые α-частицы отскакивали от фольги назад, противоречило модели Томсона. Результаты эксперимента настолько удивили Резерфорда, что он воскликнул: "... неправдоподобно так же, как если бы вы выстрелили пятнадцатифунтовым снарядом в папиросную бумагу, а снаряд отскочил бы обратно и убил бы вас самих". Частицы возвращались редко: в среднем одна частица из восьми тысяч. Отражение от мишени означало, что частица встретила на пути достойную преграду – массивную и положительно заряженную: только такая может с силой оттолкнуть от себя прилетевшую гостью.
Cлайд 14
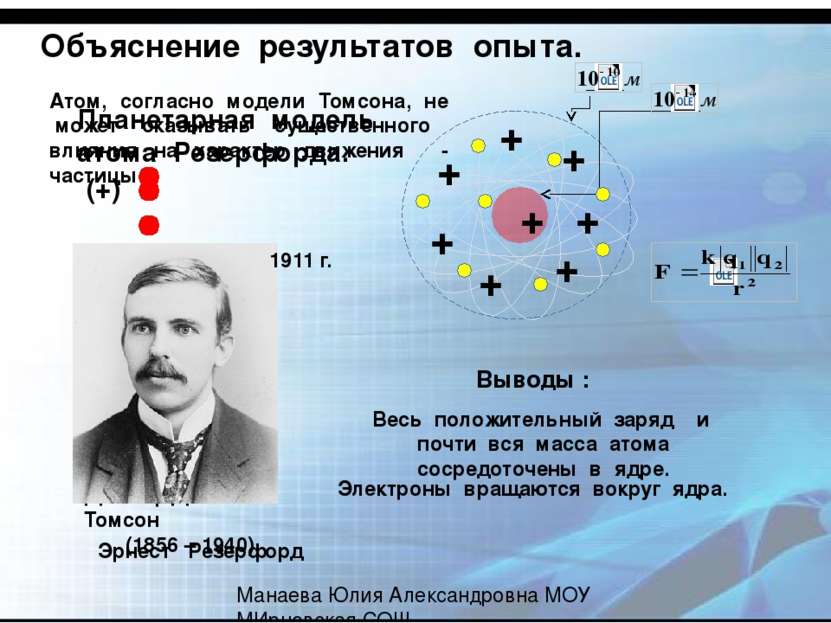
 + + + α (+) Джозеф Джон Томсон (1856 – 1940) + + + + + 1911 г. Весь положительный заряд и почти вся масса атома сосредоточены в ядре. Электроны вращаются вокруг ядра. Выводы : Атом, согласно модели Томсона, не может оказывать существенного влияния на характер движения α - частицы Эрнест Резерфорд Планетарная модель атома Резерфорда. Объяснение результатов опыта. Манаева Юлия Александровна МОУ МИрновская СОШ Частицы возвращались редко: в среднем одна частица из восьми тысяч. Отражение от мишени означало, что частица встретила на пути достойную преграду – массивную и положительно заряженную: только такая может с силой оттолкнуть от себя прилетевшую гостью. Редкость события говорила о крайне малых размерах преграды, именно поэтому лишь немногие частицы попадают в массивную атомную сердцевину. Подавляющее большинство пролетает в отдалении от нее и рассеивается на малые углы. Так было открыто атомное ядро. Эксперимент, который был предназначен на подтверждение теории Томсона, в пух и прах опроверг её. Отношения между Томсоном и Резерфордом были испорчены практически до конца дней.
+ + + α (+) Джозеф Джон Томсон (1856 – 1940) + + + + + 1911 г. Весь положительный заряд и почти вся масса атома сосредоточены в ядре. Электроны вращаются вокруг ядра. Выводы : Атом, согласно модели Томсона, не может оказывать существенного влияния на характер движения α - частицы Эрнест Резерфорд Планетарная модель атома Резерфорда. Объяснение результатов опыта. Манаева Юлия Александровна МОУ МИрновская СОШ Частицы возвращались редко: в среднем одна частица из восьми тысяч. Отражение от мишени означало, что частица встретила на пути достойную преграду – массивную и положительно заряженную: только такая может с силой оттолкнуть от себя прилетевшую гостью. Редкость события говорила о крайне малых размерах преграды, именно поэтому лишь немногие частицы попадают в массивную атомную сердцевину. Подавляющее большинство пролетает в отдалении от нее и рассеивается на малые углы. Так было открыто атомное ядро. Эксперимент, который был предназначен на подтверждение теории Томсона, в пух и прах опроверг её. Отношения между Томсоном и Резерфордом были испорчены практически до конца дней.