X
Код презентации скопируйте его
Основные сведения о строении атомов
Скачать эту презентациюПрезентация на тему Основные сведения о строении атомов
Скачать эту презентациюCлайд 4
 Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит из мельчайших частиц, которые впоследствии были названы «атомами», что в переводе на русский язык означает «неделимый» Долгое время считалось, что атом является неделимой частицей.
Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит из мельчайших частиц, которые впоследствии были названы «атомами», что в переводе на русский язык означает «неделимый» Долгое время считалось, что атом является неделимой частицей.
Cлайд 5
 СТОНЕИ (Стони) Джордж Джонстон (Stoney George Johnstone) (15.II.1826 – 5.VII.1911) — ирландский физик и математик, член Ирландского королевского об-ва (1861), его секретарь на протяжении 20 лет. Ирландский физик СТОНИ на основании опытов пришёл к выводу, что электричество переносится мельчайшими частицами, существующими в атомах всех химических элементов В 1891 предложил название «электрон», что по-гречески означает «янтарь» для элементарного
СТОНЕИ (Стони) Джордж Джонстон (Stoney George Johnstone) (15.II.1826 – 5.VII.1911) — ирландский физик и математик, член Ирландского королевского об-ва (1861), его секретарь на протяжении 20 лет. Ирландский физик СТОНИ на основании опытов пришёл к выводу, что электричество переносится мельчайшими частицами, существующими в атомах всех химических элементов В 1891 предложил название «электрон», что по-гречески означает «янтарь» для элементарного
Cлайд 8
 История открытия строения атома. Дж. Томсон. Доказал, что электроны несут на себе отрицательный заряд, определил массу и скорость движения. е - электрон
История открытия строения атома. Дж. Томсон. Доказал, что электроны несут на себе отрицательный заряд, определил массу и скорость движения. е - электрон
Cлайд 11
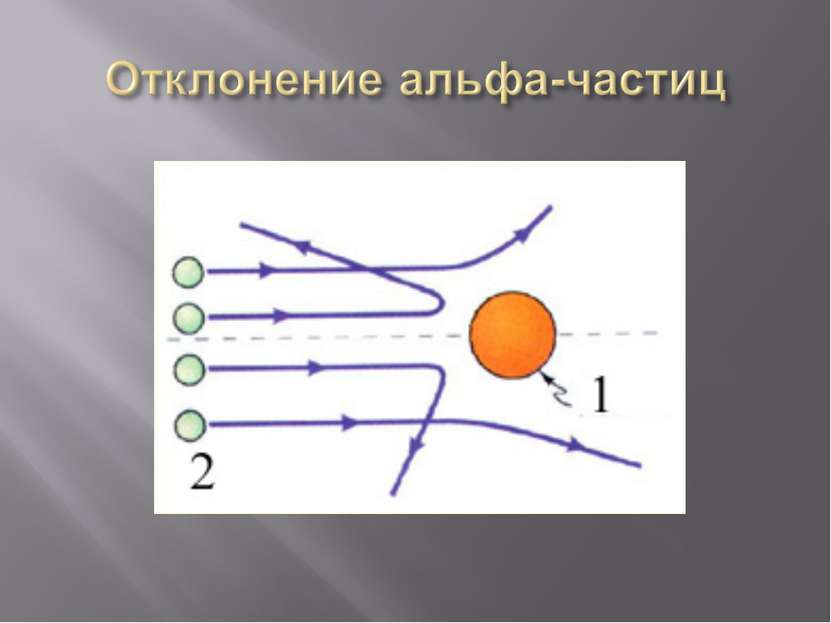
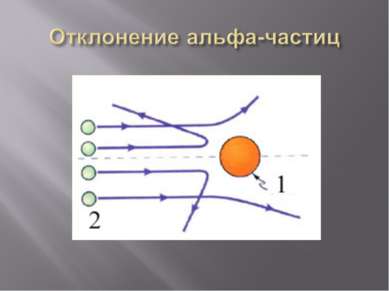
 В 1910 г. Эрнест Резерфорд со своими учениками и коллегами изучал рассеивание альфа-частиц, проходящих через тонкую золотую фольгу и попадавших на экран.
В 1910 г. Эрнест Резерфорд со своими учениками и коллегами изучал рассеивание альфа-частиц, проходящих через тонкую золотую фольгу и попадавших на экран.
Cлайд 12
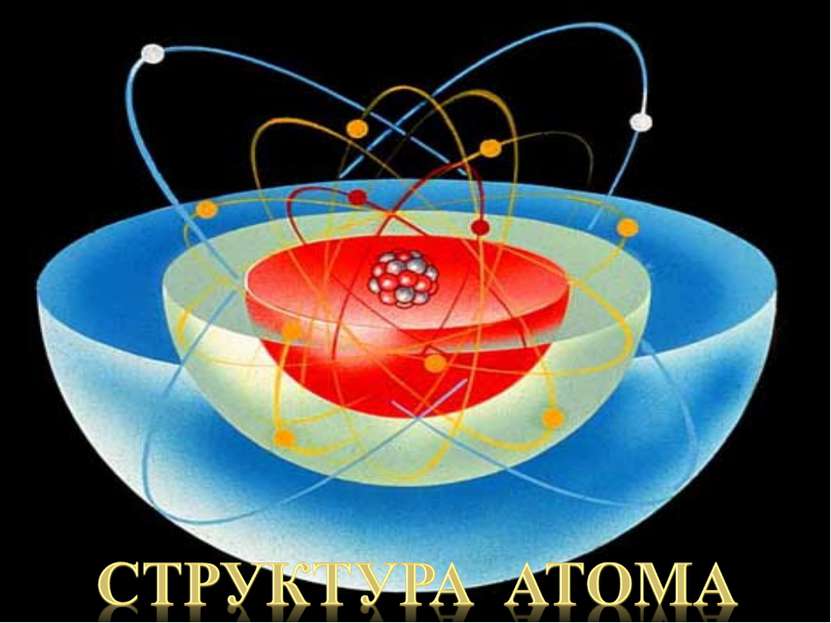
 Доказал, что атом имеет плотное ядро. Предложил планетарную теорию строения атома. Э. Резерфорд
Доказал, что атом имеет плотное ядро. Предложил планетарную теорию строения атома. Э. Резерфорд
Cлайд 25
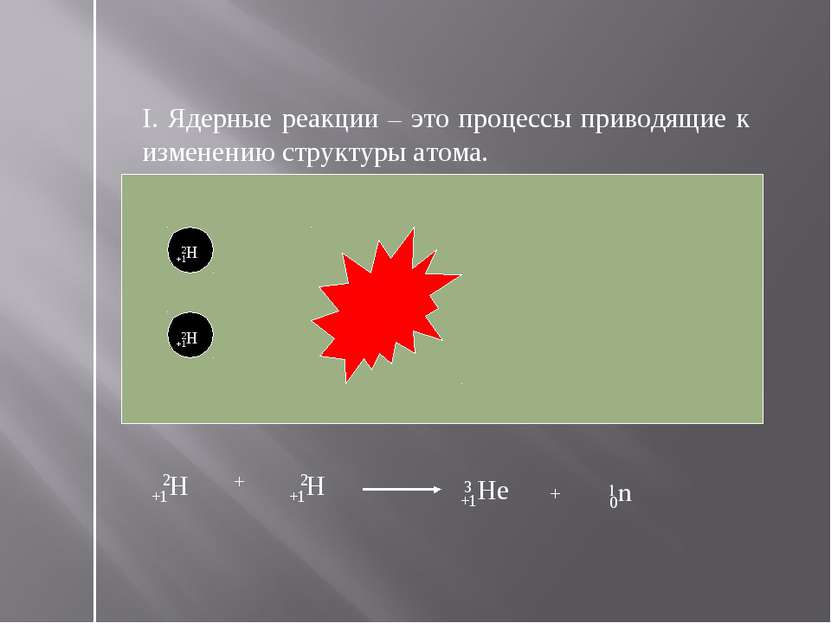
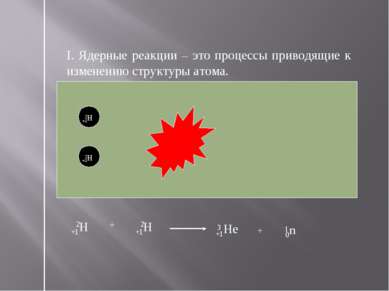 I. Ядерные реакции – это процессы приводящие к изменению структуры атома. +1Н 2 +1Н 2 +1Не 3 0n 1 +1Н 2 +1Н 2 + +1Не 3 0n 1 +
I. Ядерные реакции – это процессы приводящие к изменению структуры атома. +1Н 2 +1Н 2 +1Не 3 0n 1 +1Н 2 +1Н 2 + +1Не 3 0n 1 +
Cлайд 27
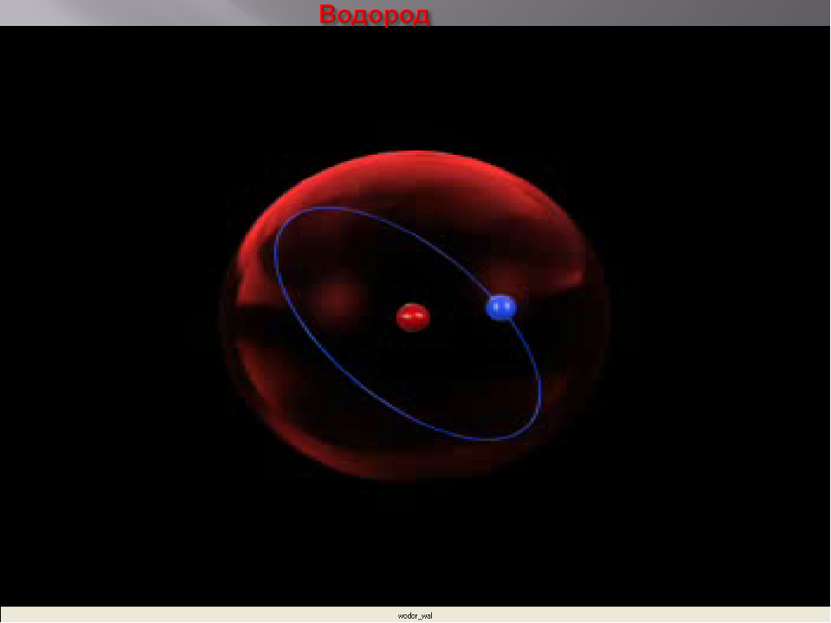
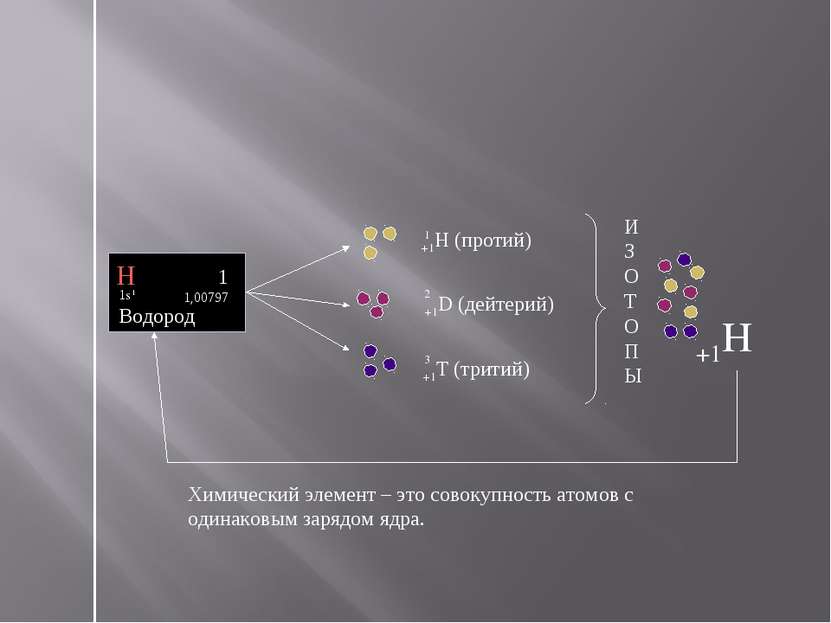
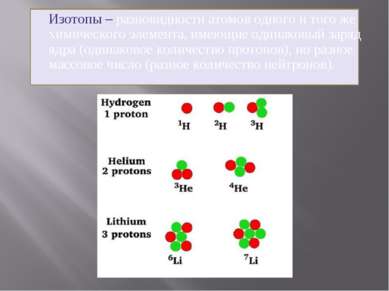
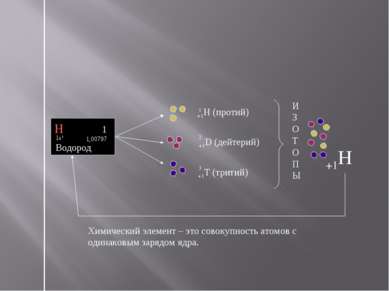 +1H (протий) +1D (дейтерий) +1T (тритий) Химический элемент – это совокупность атомов с одинаковым зарядом ядра. Н 1 1,00797 1s1 Водород 3 1 2 И З О Т О П Ы +1H
+1H (протий) +1D (дейтерий) +1T (тритий) Химический элемент – это совокупность атомов с одинаковым зарядом ядра. Н 1 1,00797 1s1 Водород 3 1 2 И З О Т О П Ы +1H