X
Код презентации скопируйте его
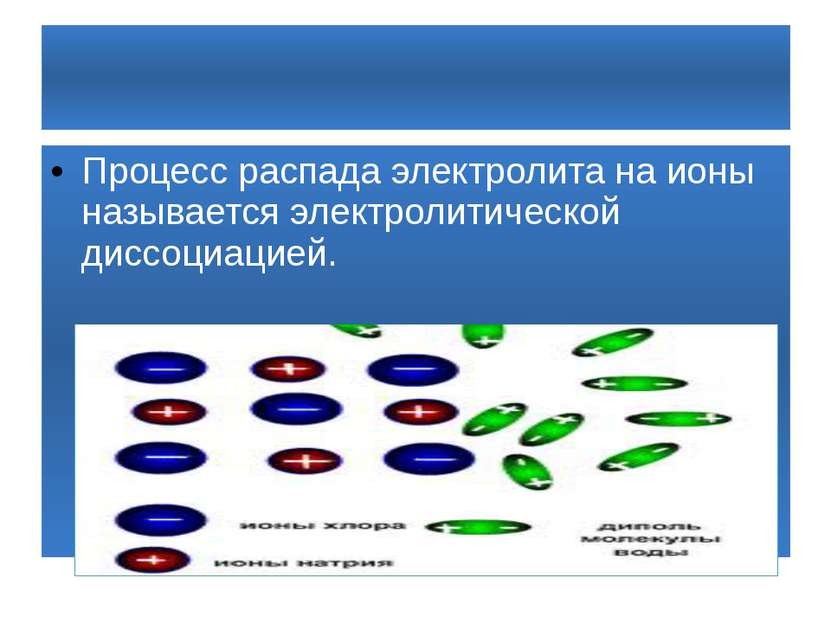
Электролитическая диссоциация (8 класс)
Скачать эту презентациюПрезентация на тему Электролитическая диссоциация (8 класс)
Скачать эту презентациюCлайд 8
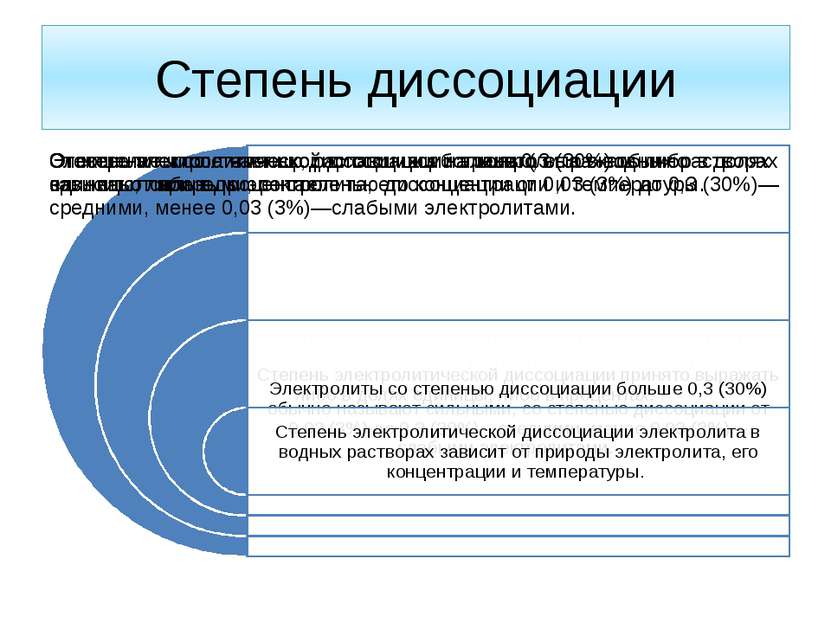
 Электролиты условно делятся: Сильные электролиты диссоциируют практически полностью (α = 1). Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами.
Электролиты условно делятся: Сильные электролиты диссоциируют практически полностью (α = 1). Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами.
Cлайд 10
 К слабым электролитам относятся: 1) неорганические кислоты (H2CO3, H2S, HNO2, H2SO3 , HCN, H3PO4, H2SiO3, HCNS, HСlO и др.); 2) вода (H2O); 3) гидроксид аммония (NH4OH); 4) большинство органических кислот (например, уксусная CH3COOH, муравьиная HCOOH); 5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов
К слабым электролитам относятся: 1) неорганические кислоты (H2CO3, H2S, HNO2, H2SO3 , HCN, H3PO4, H2SiO3, HCNS, HСlO и др.); 2) вода (H2O); 3) гидроксид аммония (NH4OH); 4) большинство органических кислот (например, уксусная CH3COOH, муравьиная HCOOH); 5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов
Cлайд 11
 Тест по теме "Электролитическая диссоциация. Реакции ионного обмена" 1. К неэлектролитам относится: 1) нитрат калия 2) гидроксид бария 3) хлорид кальция 4) оксид азота(II) 2. К хорошо растворимым электролитам относится: 1) бромид натрия 2) гидроксид цинка 3) карбонат кальция 4) гидроксид магния 3. В водном растворе наибольшее количество сульфат-анионов образуется при диссоциации 1 моль: 1) Al2(SO4)3 2)PbS 3) CaSO4 4) K2SO4
Тест по теме "Электролитическая диссоциация. Реакции ионного обмена" 1. К неэлектролитам относится: 1) нитрат калия 2) гидроксид бария 3) хлорид кальция 4) оксид азота(II) 2. К хорошо растворимым электролитам относится: 1) бромид натрия 2) гидроксид цинка 3) карбонат кальция 4) гидроксид магния 3. В водном растворе наибольшее количество сульфат-анионов образуется при диссоциации 1 моль: 1) Al2(SO4)3 2)PbS 3) CaSO4 4) K2SO4
Cлайд 12
 Тест по теме "Электролитическая диссоциация 4. Катионы металла и анионы кислотного остатка образуютя при диссоциации: 1) оксидов 2) кислот 3) солей 4) оснований 5. Выберите верную запись правой части уравнения диссоциации карбоната калия: 1) = K+ + CO3¯ 2) = K+ + CO32- 3) = 2K+ + CO32- 4) = 2K+ + HCO3¯ 6. Наибольшее количество анионов образуется при диссоциации 1 моль: 1) AlCl3 2) Zn(OH)2 3) Al(OH)3 4) Zn(NO3)2
Тест по теме "Электролитическая диссоциация 4. Катионы металла и анионы кислотного остатка образуютя при диссоциации: 1) оксидов 2) кислот 3) солей 4) оснований 5. Выберите верную запись правой части уравнения диссоциации карбоната калия: 1) = K+ + CO3¯ 2) = K+ + CO32- 3) = 2K+ + CO32- 4) = 2K+ + HCO3¯ 6. Наибольшее количество анионов образуется при диссоциации 1 моль: 1) AlCl3 2) Zn(OH)2 3) Al(OH)3 4) Zn(NO3)2