X
Код презентации скопируйте его
Коррозия металлов (11 класс)
Скачать эту презентациюПрезентация на тему Коррозия металлов (11 класс)
Скачать эту презентациюCлайд 1
 Коррозия (от лат. corrosio – «разъедать») - это самопроизвольно протекающий процесс разрушения металлов в результате взаимодействия с окружающей средой.
Коррозия (от лат. corrosio – «разъедать») - это самопроизвольно протекающий процесс разрушения металлов в результате взаимодействия с окружающей средой.
Cлайд 4
 По виду коррозионной среды газовая; жидкостная: - кислотная, щелочная, - солевая; атмосферная; почвенная.
По виду коррозионной среды газовая; жидкостная: - кислотная, щелочная, - солевая; атмосферная; почвенная.
Cлайд 12
 Изменение свойств агрессивной среды: – удаление из неё веществ, которые усиливают коррозию (например, кислород можно удалить кипячением); – добавление веществ, которые замедляют коррозию, – ингибиторов. Легирование металлов – получение сплавов, которые устойчивы к коррозии (например, нержавеющей стали, содержащей до 18% хрома и до 10% никеля). Изоляция металла от окружающей среды нанесением покрытий: – неметаллических (покрытие лаками, красками, эмалями); – химических (оксидные, фосфатные, нитридные и т. д.); – металлических покрытий (катодное и анодное покрытие). Защита металлов от коррозии
Изменение свойств агрессивной среды: – удаление из неё веществ, которые усиливают коррозию (например, кислород можно удалить кипячением); – добавление веществ, которые замедляют коррозию, – ингибиторов. Легирование металлов – получение сплавов, которые устойчивы к коррозии (например, нержавеющей стали, содержащей до 18% хрома и до 10% никеля). Изоляция металла от окружающей среды нанесением покрытий: – неметаллических (покрытие лаками, красками, эмалями); – химических (оксидные, фосфатные, нитридные и т. д.); – металлических покрытий (катодное и анодное покрытие). Защита металлов от коррозии
Cлайд 13
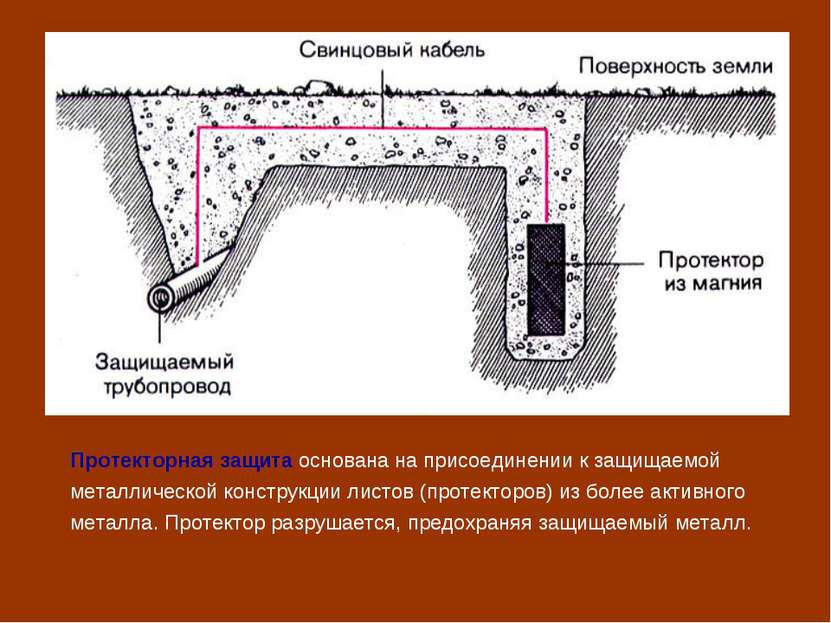
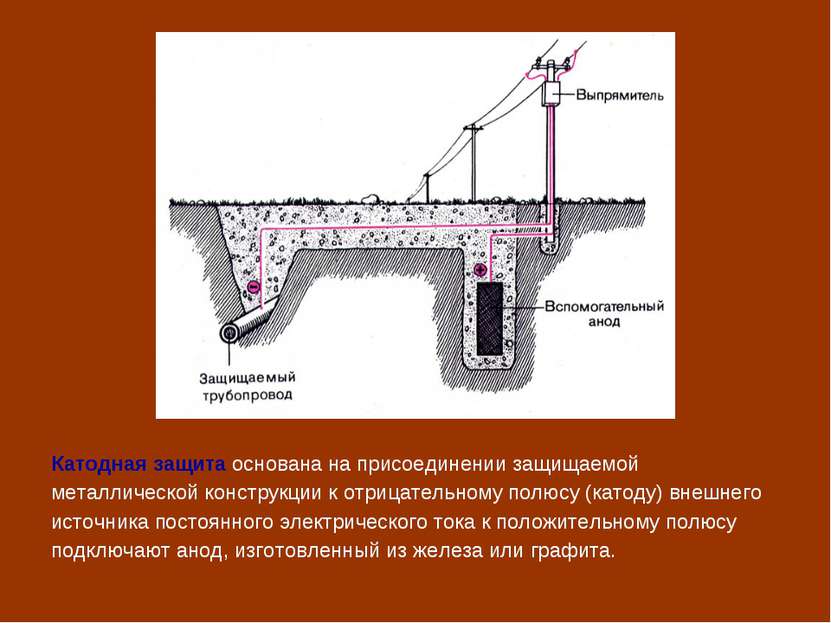
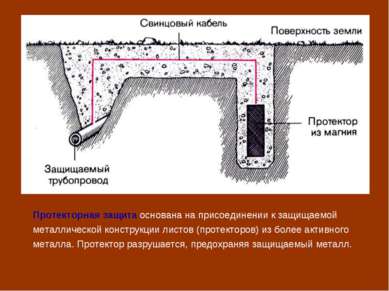 Протекторная защита основана на присоединении к защищаемой металлической конструкции листов (протекторов) из более активного металла. Протектор разрушается, предохраняя защищаемый металл.
Протекторная защита основана на присоединении к защищаемой металлической конструкции листов (протекторов) из более активного металла. Протектор разрушается, предохраняя защищаемый металл.