X
Код презентации скопируйте его
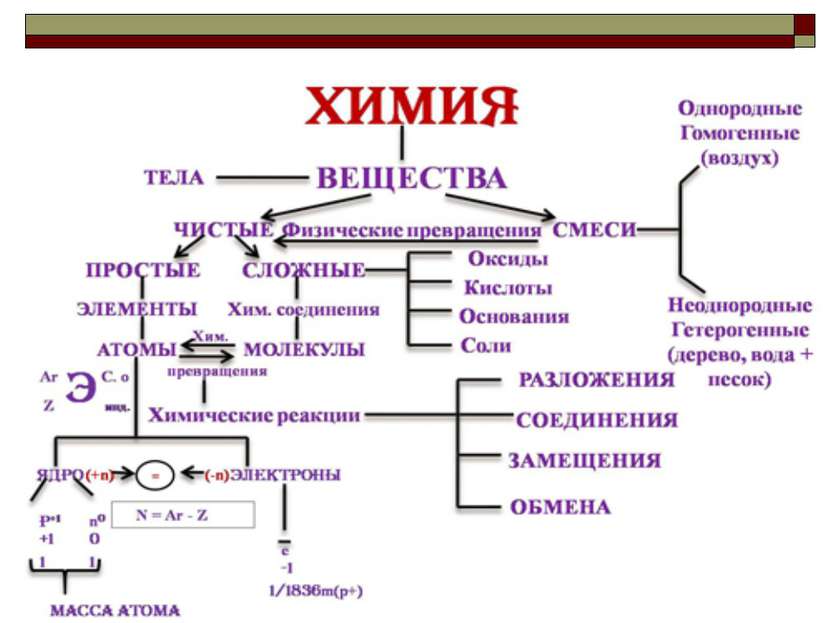
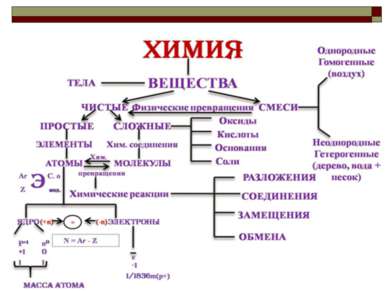
Характеристика элемента - металла
Скачать эту презентациюПрезентация на тему Характеристика элемента - металла
Скачать эту презентациюCлайд 5
 Особенности элементов металлов На внешнем уровне …. …Са + О2 =…СаО Металлы могут проявлять ….. свойства 3. Металлы проявляют общие физических свойства - …., которые обусловлены ….. 4. Металл → …. оксид → ….. гидрокид ( ….)
Особенности элементов металлов На внешнем уровне …. …Са + О2 =…СаО Металлы могут проявлять ….. свойства 3. Металлы проявляют общие физических свойства - …., которые обусловлены ….. 4. Металл → …. оксид → ….. гидрокид ( ….)
Cлайд 6
 Определите элемент, ион которого входит в состав поваренной соли: А) 2е, 8е, 8е, 2е Б) 2е, 8е, 1е В) 2е, 8е, 5е Охарактеризуйте элемент. Запишите формулы высших оксида и гидроксида, Запишите уравнения реакций, подтверждающих их характер.
Определите элемент, ион которого входит в состав поваренной соли: А) 2е, 8е, 8е, 2е Б) 2е, 8е, 1е В) 2е, 8е, 5е Охарактеризуйте элемент. Запишите формулы высших оксида и гидроксида, Запишите уравнения реакций, подтверждающих их характер.
Cлайд 7
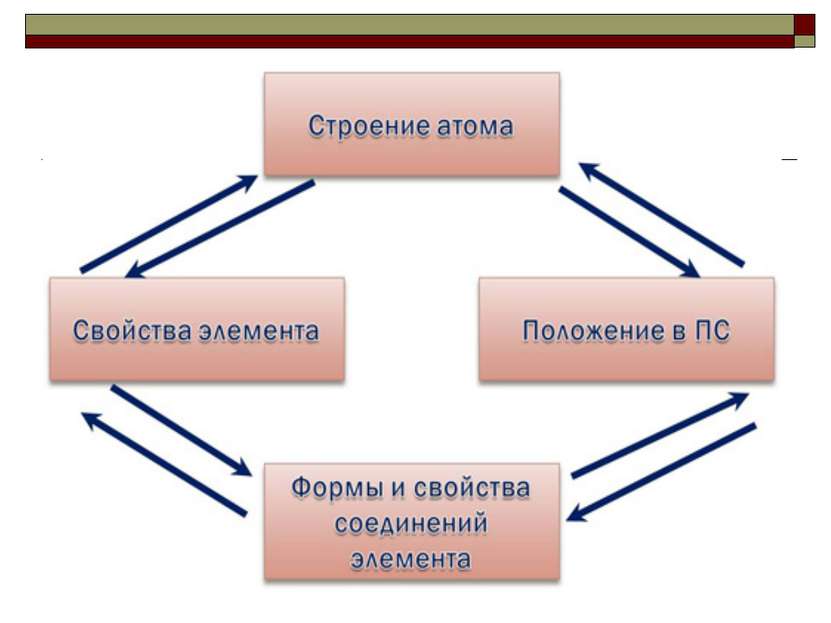
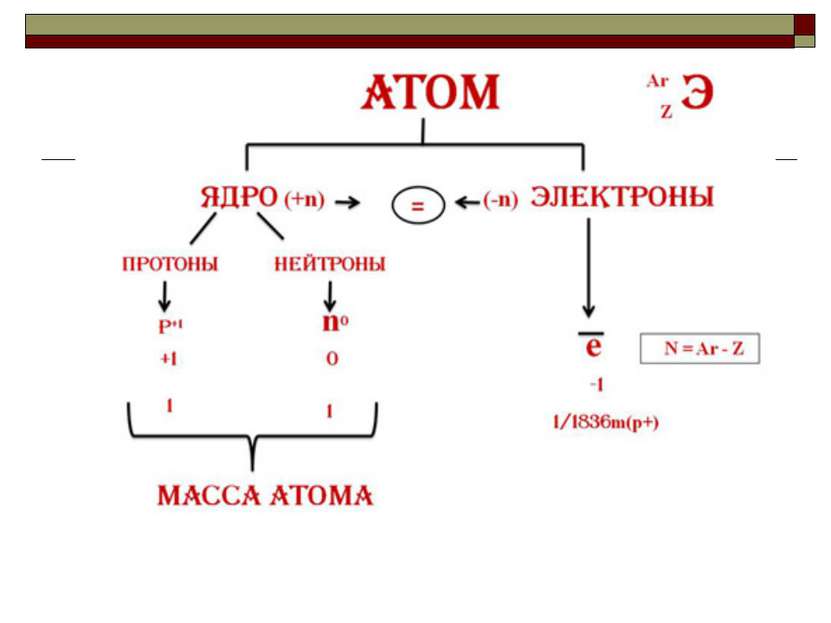
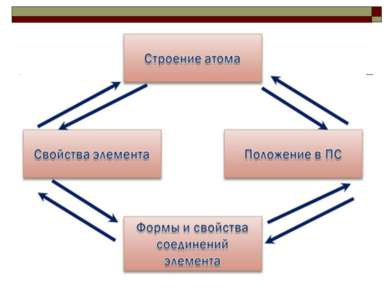
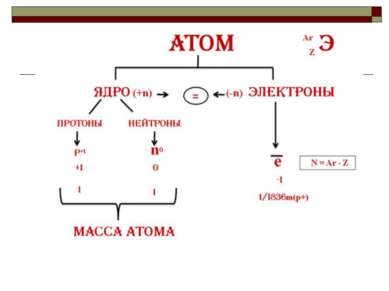
 Характеристика элемента-металла на основании его положения в ПС Д.И. Менделеева Положение элемента в Периодической системе. а) порядковый номер б) период в) группа, подгруппа г) 2.Строение атома и его свойства а) число протонов, электронов, нейтронов б) заряд ядра в) схема строения электронной оболочки е) окислительно - восстановительные свойства д) возможные степени окисления 3. Простое вещество
Характеристика элемента-металла на основании его положения в ПС Д.И. Менделеева Положение элемента в Периодической системе. а) порядковый номер б) период в) группа, подгруппа г) 2.Строение атома и его свойства а) число протонов, электронов, нейтронов б) заряд ядра в) схема строения электронной оболочки е) окислительно - восстановительные свойства д) возможные степени окисления 3. Простое вещество
Cлайд 8
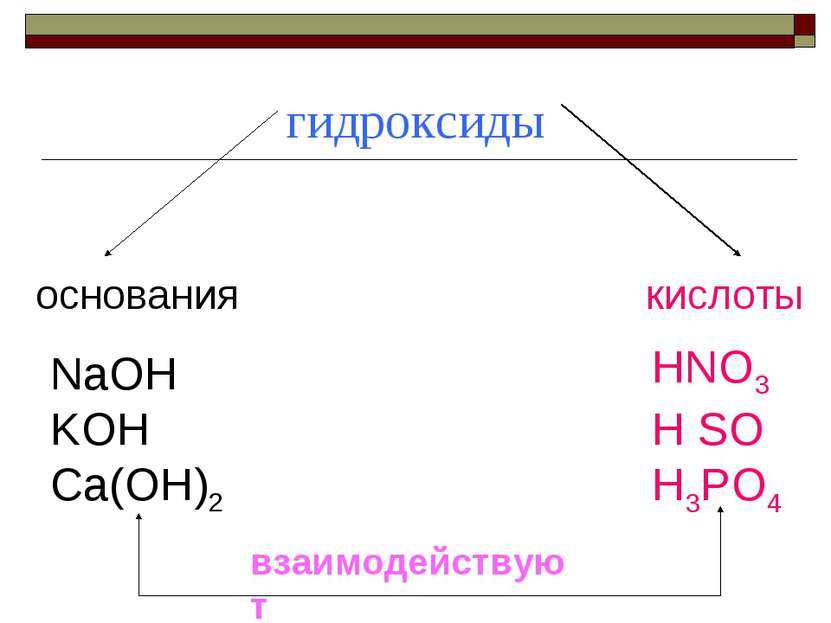
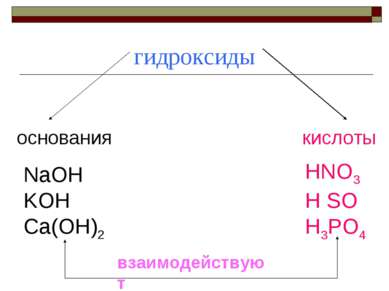
 Характеристика высшего оксида и гидроксида Формула высшего оксида и характер высшего оксида Уравнения реакций, подтверждающих характер оксида. Формула и характер высшего гидроксида. Уравнения реакций, подтверждающие свойства гидроксида.
Характеристика высшего оксида и гидроксида Формула высшего оксида и характер высшего оксида Уравнения реакций, подтверждающих характер оксида. Формула и характер высшего гидроксида. Уравнения реакций, подтверждающие свойства гидроксида.
Cлайд 9
 Расположите элементы 1) в порядке возрастания металлических свойств: К, Аl, Са 2) в порядке возрастания металлических свойств: Ca, Ba, Be, Mg
Расположите элементы 1) в порядке возрастания металлических свойств: К, Аl, Са 2) в порядке возрастания металлических свойств: Ca, Ba, Be, Mg