X
Код презентации скопируйте его
Изотопы
Скачать эту презентациюПрезентация на тему Изотопы
Скачать эту презентациюCлайд 3
 Изотопы Это разновидности данного химического элемента, различающиеся по массе атомных ядер. Это разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре.
Изотопы Это разновидности данного химического элемента, различающиеся по массе атомных ядер. Это разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре.
Cлайд 4
 История открытия изотопов Первое доказательство того, что вещества, имеющие одинаковое химическое поведение, могут иметь различные физические свойства, было получено при исследовании радиоактивных превращений атомов тяжёлых элементов. В 1906—07 выяснилось, что продукт радиоактивного распада урана — ионий и продукт радиоактивного распада тория — радиоторий, имеют те же химические свойства, что и торий, но отличаются от него атомной массой и характеристиками радиоактивного распада. Было обнаружено позднее, что у всех трёх продуктов одинаковы оптические и рентгеновские спектры.
История открытия изотопов Первое доказательство того, что вещества, имеющие одинаковое химическое поведение, могут иметь различные физические свойства, было получено при исследовании радиоактивных превращений атомов тяжёлых элементов. В 1906—07 выяснилось, что продукт радиоактивного распада урана — ионий и продукт радиоактивного распада тория — радиоторий, имеют те же химические свойства, что и торий, но отличаются от него атомной массой и характеристиками радиоактивного распада. Было обнаружено позднее, что у всех трёх продуктов одинаковы оптические и рентгеновские спектры.
Cлайд 5
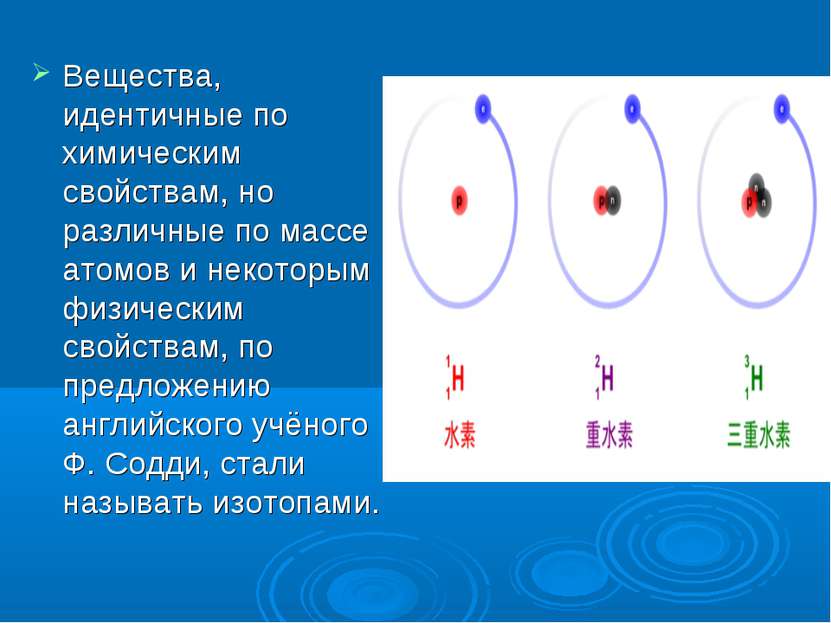
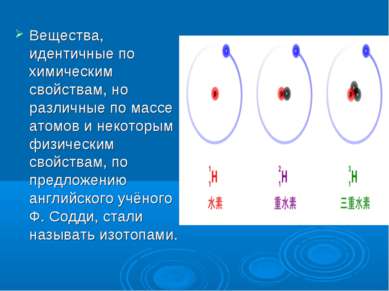 Вещества, идентичные по химическим свойствам, но различные по массе атомов и некоторым физическим свойствам, по предложению английского учёного Ф. Содди, стали называть изотопами.
Вещества, идентичные по химическим свойствам, но различные по массе атомов и некоторым физическим свойствам, по предложению английского учёного Ф. Содди, стали называть изотопами.
Cлайд 6
 Изотопы водорода Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1H — протий (Н), 2Н — дейтерий (D), 3Н — тритий (T; радиоактивный). Протий и дейтерий являются стабильными изотопами с массовыми числами 1 и 2. Содержание их в природе соответственно составляет 99,98% и 0,01 %. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода..
Изотопы водорода Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1H — протий (Н), 2Н — дейтерий (D), 3Н — тритий (T; радиоактивный). Протий и дейтерий являются стабильными изотопами с массовыми числами 1 и 2. Содержание их в природе соответственно составляет 99,98% и 0,01 %. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода..
Cлайд 7
 Изотопы водорода 3 Н — тритий (T) радиоактивный). Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет. Тритий содержится в природе в очень малых количествах.
Изотопы водорода 3 Н — тритий (T) радиоактивный). Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет. Тритий содержится в природе в очень малых количествах.
Cлайд 8
 изотопы находятся в одном и том же месте (в одной клетке) таблицы Менделеева. 16 17 18 O, O, O — три стабильных изотопа кислорода Все изотопы одного элемента имеют одинаковый заряд ядра ( у кислорода 8), отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число
изотопы находятся в одном и том же месте (в одной клетке) таблицы Менделеева. 16 17 18 O, O, O — три стабильных изотопа кислорода Все изотопы одного элемента имеют одинаковый заряд ядра ( у кислорода 8), отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число
Cлайд 9
 Радиоактивные изотопы — изотопы, ядра которых нестабильны и испытывают радиоактивный распад. Большинство известных изотопов радиоактивны (стабильными являются лишь около 300 из более чем 3000 нуклидов, известных науке). У любого химического элемента есть хотя бы несколько радиоактивных изотопов, в то же время далеко не у всех элементов есть хотя бы один стабильный изотоп; так, все известные изотопы всех элементов, которые в таблице Менделеева идут после свинца, радиоактивны.
Радиоактивные изотопы — изотопы, ядра которых нестабильны и испытывают радиоактивный распад. Большинство известных изотопов радиоактивны (стабильными являются лишь около 300 из более чем 3000 нуклидов, известных науке). У любого химического элемента есть хотя бы несколько радиоактивных изотопов, в то же время далеко не у всех элементов есть хотя бы один стабильный изотоп; так, все известные изотопы всех элементов, которые в таблице Менделеева идут после свинца, радиоактивны.