X
Код презентации скопируйте его
Герпес
Скачать эту презентациюПрезентация на тему Герпес
Скачать эту презентациюCлайд 1
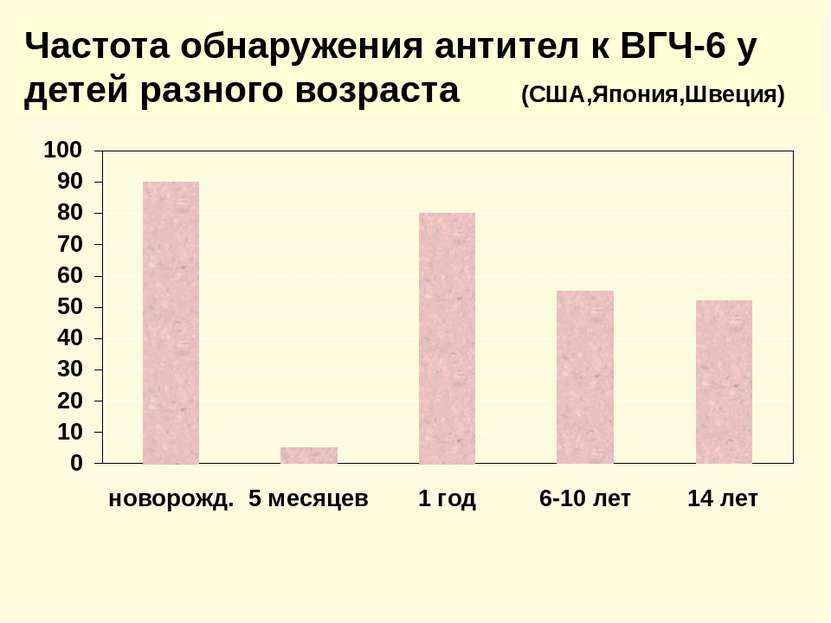
 Предполагается, что в стране 22 млн. человек страдают от герпеса; ежегодно переносят: не менее 3 тыс. человек – герпетические нейроинфекции (10% энцефалитов и 20% менингоэцефалитов – ВПГ этиологии) ; 300 тыс. – 500 тыс. – офтальмогерпес (60% кератитов – ВПГ этиологии); 8 млн. человек – генитальный герпес; 10 -12 млн. человек – орофациальный герпес. Каражас Н.В., Малиновская В.В. – 2011 год По данным ВОЗ: Смертность от диссемированных форм болезни, вызванной ВПГ, составляет 15,8% - II место после гриппа; ВПГ – инфекция - 35,8% - среди заболеваний вирусной этиологии; 60 – 90% населения в разные периоды жизни инфицируются одним или несколькими типами вирусов, у 50% из них отмечаются рецидивы заболевания. http://prezentacija.biz/
Предполагается, что в стране 22 млн. человек страдают от герпеса; ежегодно переносят: не менее 3 тыс. человек – герпетические нейроинфекции (10% энцефалитов и 20% менингоэцефалитов – ВПГ этиологии) ; 300 тыс. – 500 тыс. – офтальмогерпес (60% кератитов – ВПГ этиологии); 8 млн. человек – генитальный герпес; 10 -12 млн. человек – орофациальный герпес. Каражас Н.В., Малиновская В.В. – 2011 год По данным ВОЗ: Смертность от диссемированных форм болезни, вызванной ВПГ, составляет 15,8% - II место после гриппа; ВПГ – инфекция - 35,8% - среди заболеваний вирусной этиологии; 60 – 90% населения в разные периоды жизни инфицируются одним или несколькими типами вирусов, у 50% из них отмечаются рецидивы заболевания. http://prezentacija.biz/
Cлайд 2
 Классификация Международного комитета по таксономии вирусов (1995) Вирусы герпеса человека Herpes humanum virus HHV-I -Вирус простого герпеса 1 -ВПГ-1 HHV-II -Вирус простого герпеса 2 -ВПГ-2 HHV-III -Варицелла-Зостер вирус -ВВЗ - 3 HHV-IV -Эпштейна-Барр вирус -ЭБВ – 4 HHV-V - Цитомегаловирус -ЦМВ – 5 HHV-VI -Вирус герпеса человека 6 типа -ВГЧ – 6 HHV-VII -Вирус хронической усталости -ВГЧ – 7 HHV-VIII -Вирус ассоциированый с саркомой Капоши -ВГЧ-8
Классификация Международного комитета по таксономии вирусов (1995) Вирусы герпеса человека Herpes humanum virus HHV-I -Вирус простого герпеса 1 -ВПГ-1 HHV-II -Вирус простого герпеса 2 -ВПГ-2 HHV-III -Варицелла-Зостер вирус -ВВЗ - 3 HHV-IV -Эпштейна-Барр вирус -ЭБВ – 4 HHV-V - Цитомегаловирус -ЦМВ – 5 HHV-VI -Вирус герпеса человека 6 типа -ВГЧ – 6 HHV-VII -Вирус хронической усталости -ВГЧ – 7 HHV-VIII -Вирус ассоциированый с саркомой Капоши -ВГЧ-8
Cлайд 3
 Филогенетическая классификация герпесвирусов человека Альфа-вирусы (ВПГ- 1, 2 и ВВЗ) . Характеризуются быстрой репликацией 4-8 часов), способностью к цитолизу и бессимптомным персистированием в нейтрональных клетках. Бета-вирусы (ЦМВ, ВГЧ-6 и ВГЧ-7 ). Медленно реплицируются, вызывают цитомегалическую трансформацию клеток, а основными очагами латенции являются моноциты и их предшественники, эндотелиальные клетки сосудов микроциркуляторного русла, альвеолярные макрофаги, Т-лимфоциты и стромальные клетки костного мозга. Гамма-вирусы (ЭБВ и ВГЧ-8). Трансформирующие вирусы человека, способствующие развитию злокачественного перерождения клеток. Пожизненно персистируя в В-лимфоцитах или находясь в латентном состоянии, обладают способностью озлокачествлять их.
Филогенетическая классификация герпесвирусов человека Альфа-вирусы (ВПГ- 1, 2 и ВВЗ) . Характеризуются быстрой репликацией 4-8 часов), способностью к цитолизу и бессимптомным персистированием в нейтрональных клетках. Бета-вирусы (ЦМВ, ВГЧ-6 и ВГЧ-7 ). Медленно реплицируются, вызывают цитомегалическую трансформацию клеток, а основными очагами латенции являются моноциты и их предшественники, эндотелиальные клетки сосудов микроциркуляторного русла, альвеолярные макрофаги, Т-лимфоциты и стромальные клетки костного мозга. Гамма-вирусы (ЭБВ и ВГЧ-8). Трансформирующие вирусы человека, способствующие развитию злокачественного перерождения клеток. Пожизненно персистируя в В-лимфоцитах или находясь в латентном состоянии, обладают способностью озлокачествлять их.
Cлайд 4
 Формы взаимодействия герпесвирусов с организмом хозяина. 1. Острая форма - короткий инкубационный период с последующим развитием характерной клинической картины заболевания и обратной динамикой симптомов; 2. Хроническая форма – клинико-лабораторная симптоматика заболевания проявляется в течение длительного времени (более 6 месяцев); 3. Инаппарантная (бессимптомная) форма, когда клинические симптомы болезни не выражены, а инфекция документируется лабораторно (вирусологическими и серологическими методами исследования); 4. Форма медленной вирусной инфекции – длительный инкубационный период (месяцы и годы) и с последующим медленным прогрессирующим течением, с развитием тяжелых клинических симптомов и, в итоге, - смертью больного.
Формы взаимодействия герпесвирусов с организмом хозяина. 1. Острая форма - короткий инкубационный период с последующим развитием характерной клинической картины заболевания и обратной динамикой симптомов; 2. Хроническая форма – клинико-лабораторная симптоматика заболевания проявляется в течение длительного времени (более 6 месяцев); 3. Инаппарантная (бессимптомная) форма, когда клинические симптомы болезни не выражены, а инфекция документируется лабораторно (вирусологическими и серологическими методами исследования); 4. Форма медленной вирусной инфекции – длительный инкубационный период (месяцы и годы) и с последующим медленным прогрессирующим течением, с развитием тяжелых клинических симптомов и, в итоге, - смертью больного.
Cлайд 5
 Персистенция герпесвирусов представляет собой непрерывное и цикличное размножение (репликацию) вируса в инфицированных клетках тропных тканей, что является причиной развития инфекционного процесса. Латенция герпесвирусов клинически себя не проявляет, а диагностируется только при наличии специфических Ig G против вируса (серопозитивность) в невысоких титрах, а сам вирус в этот период в периферической крови не определяется (в ПЦР). В состоянии латенции нарушается полный цикл репродукции вируса, и он находится в клетках хозяина в виде субвирусных структур в ядре клетки.
Персистенция герпесвирусов представляет собой непрерывное и цикличное размножение (репликацию) вируса в инфицированных клетках тропных тканей, что является причиной развития инфекционного процесса. Латенция герпесвирусов клинически себя не проявляет, а диагностируется только при наличии специфических Ig G против вируса (серопозитивность) в невысоких титрах, а сам вирус в этот период в периферической крови не определяется (в ПЦР). В состоянии латенции нарушается полный цикл репродукции вируса, и он находится в клетках хозяина в виде субвирусных структур в ядре клетки.
Cлайд 6
 Факторы риска возникновения герпесвирусных инфекций Охлаждение Солнечная инсоляция УФ-облучение Нахождение в условиях резких колебаний температуры Эмоциональный стресс Психические расстройства Физическое перенапряжения Резкая смена климатических поясов Постоянное недосыпание Голодание Избыточное употребление алкоголя
Факторы риска возникновения герпесвирусных инфекций Охлаждение Солнечная инсоляция УФ-облучение Нахождение в условиях резких колебаний температуры Эмоциональный стресс Психические расстройства Физическое перенапряжения Резкая смена климатических поясов Постоянное недосыпание Голодание Избыточное употребление алкоголя
Cлайд 7
 Первое описание симптомов «простуды» на губах, сопровождающихся лихорадкой, было сделано римским врачом Геродотом в V веке до нашей эры. Слово герпес происходит от древнегреческого – герпейн (ερπυσμός) или ползучий. Так окрестил эту болезнь 2400 лет тому назад Гиппократ. Гиппократ Геродот Авиценна Парацельс
Первое описание симптомов «простуды» на губах, сопровождающихся лихорадкой, было сделано римским врачом Геродотом в V веке до нашей эры. Слово герпес происходит от древнегреческого – герпейн (ερπυσμός) или ползучий. Так окрестил эту болезнь 2400 лет тому назад Гиппократ. Гиппократ Геродот Авиценна Парацельс
Cлайд 8
 Источник инфекции – больные с различными формами болезни и вирусоносители. Пути передачи вируса: воздушно-капельный половой вертикальный контактно-бытовой парентеральный Факторы передачи вируса: кровь слюна моча везикулярный и вагинальный секрет сперма
Источник инфекции – больные с различными формами болезни и вирусоносители. Пути передачи вируса: воздушно-капельный половой вертикальный контактно-бытовой парентеральный Факторы передачи вируса: кровь слюна моча везикулярный и вагинальный секрет сперма
Cлайд 9
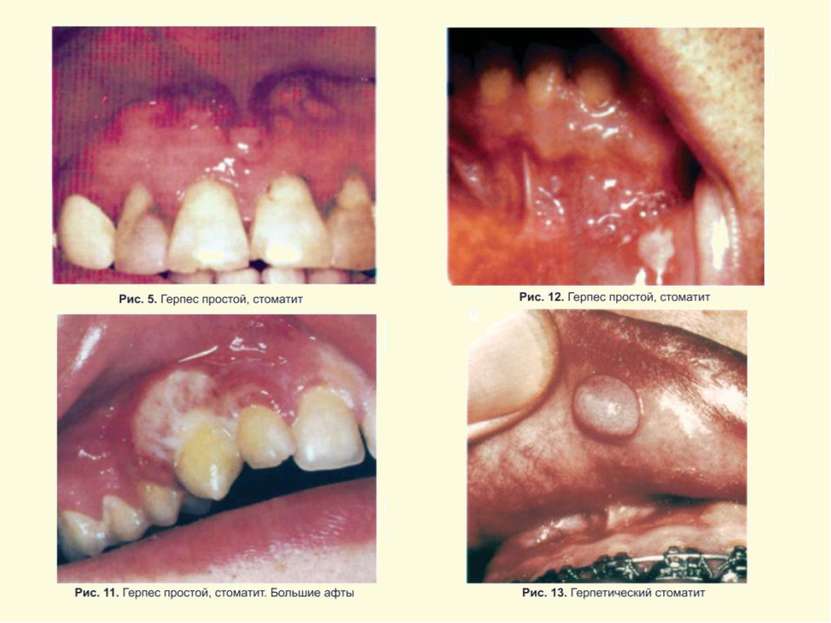
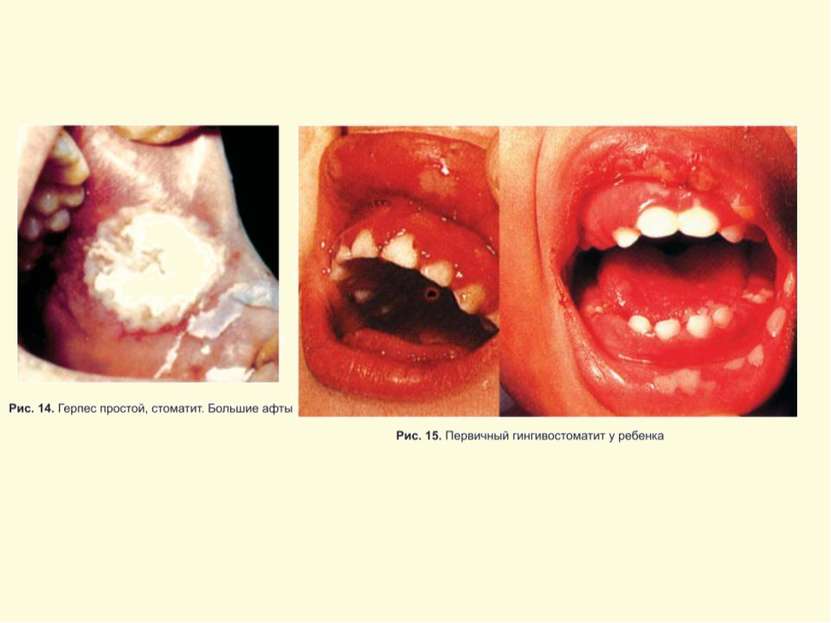
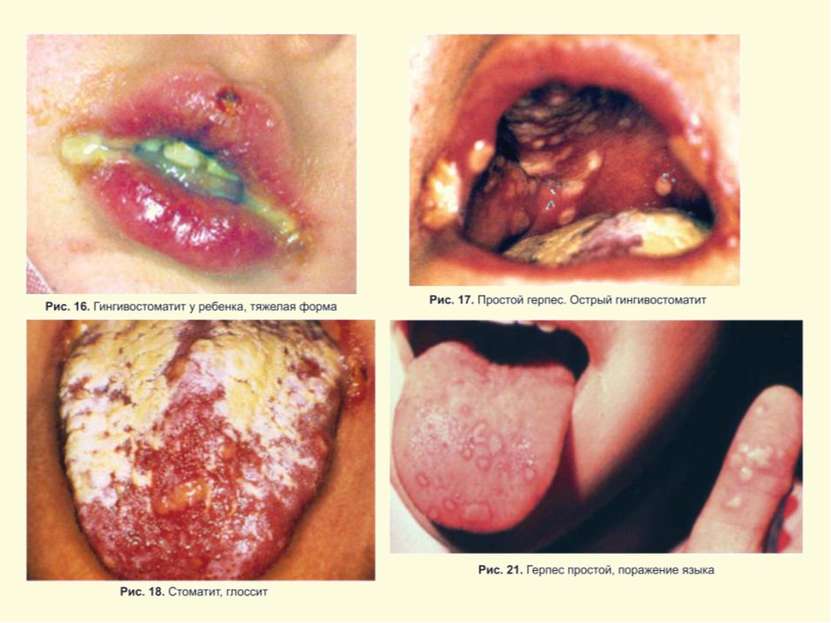
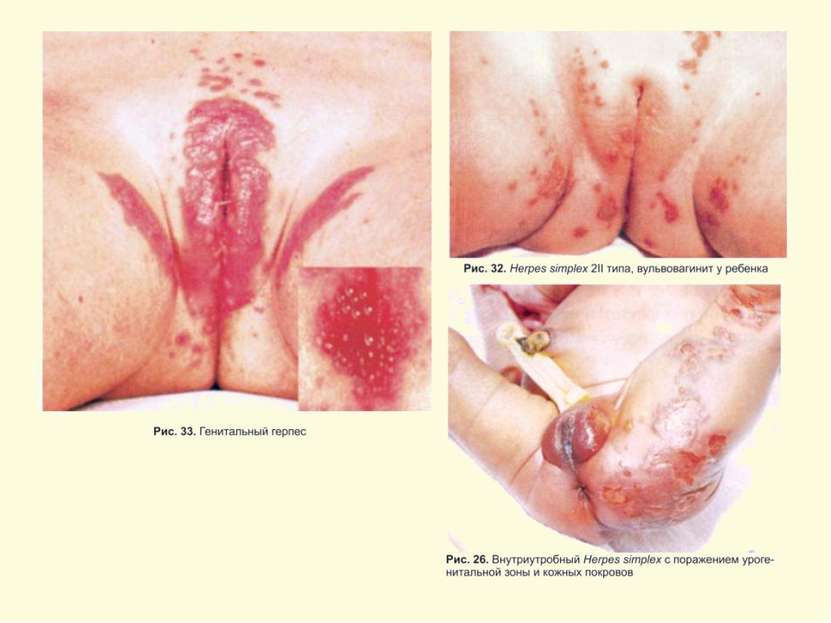
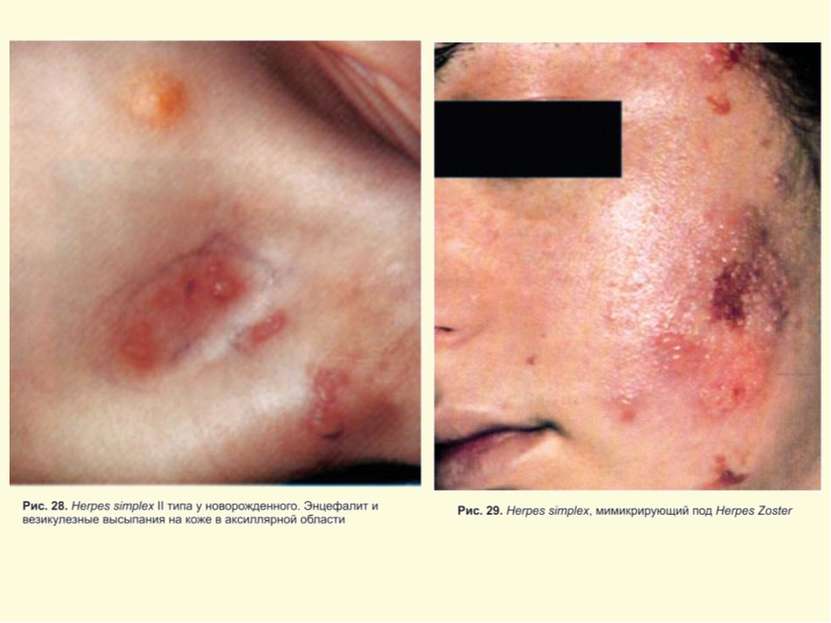
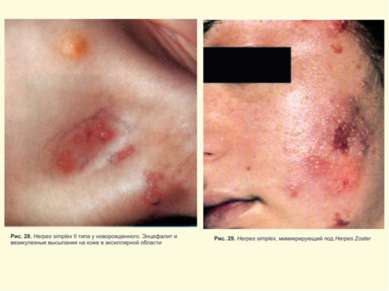
 Клинические проявления ВПГ-инфекции по МКБ-10. В00. Инфекции, вызываемые вирусом герпеса (herpes simplex). В00.0. Герпетическая экзема. В00.1. Герпетический везикулярный дерматит. В00.2. Герпетический гингивостоматит и фаринготонзиллит. В00.3. Герпетический менингит В00.4. Герпетический энцефалит В00.5. Герпетическая болезнь глаз. В00.7. Диссеминированная герпетическая болезнь В00.8.Другие формы герпетических инфекций В00.9 Герпетическая инфекция неуточненная. А60. Аногенитальная герпетическая вирусная инфекция (herpes simplex). А60.0. Герпетические инфекции половых органов и мочеполового тракта. А60.1. Герпетические инфекции перианальных кожных покровов и прямой кишки. А60.9. Аногенитальная герпетическая инфекция неуточненная.
Клинические проявления ВПГ-инфекции по МКБ-10. В00. Инфекции, вызываемые вирусом герпеса (herpes simplex). В00.0. Герпетическая экзема. В00.1. Герпетический везикулярный дерматит. В00.2. Герпетический гингивостоматит и фаринготонзиллит. В00.3. Герпетический менингит В00.4. Герпетический энцефалит В00.5. Герпетическая болезнь глаз. В00.7. Диссеминированная герпетическая болезнь В00.8.Другие формы герпетических инфекций В00.9 Герпетическая инфекция неуточненная. А60. Аногенитальная герпетическая вирусная инфекция (herpes simplex). А60.0. Герпетические инфекции половых органов и мочеполового тракта. А60.1. Герпетические инфекции перианальных кожных покровов и прямой кишки. А60.9. Аногенитальная герпетическая инфекция неуточненная.
Cлайд 11
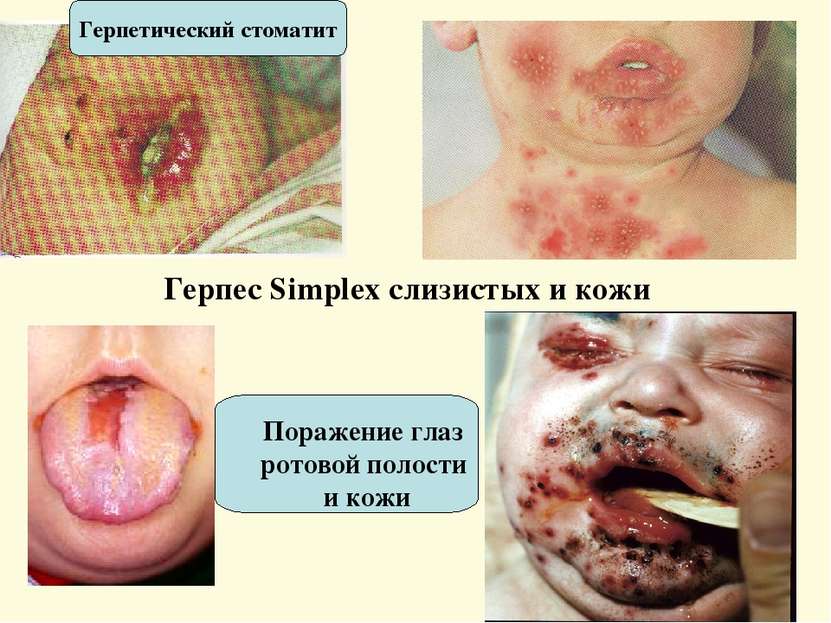
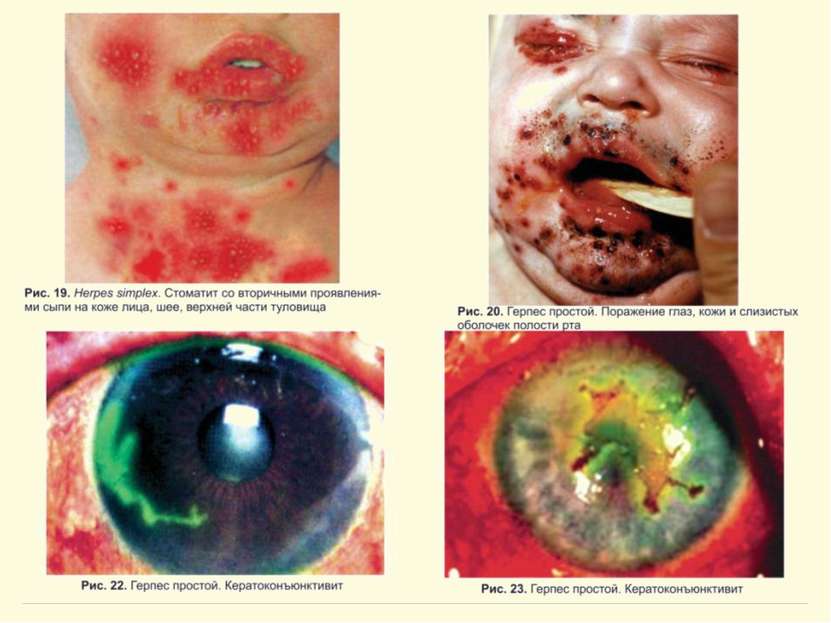
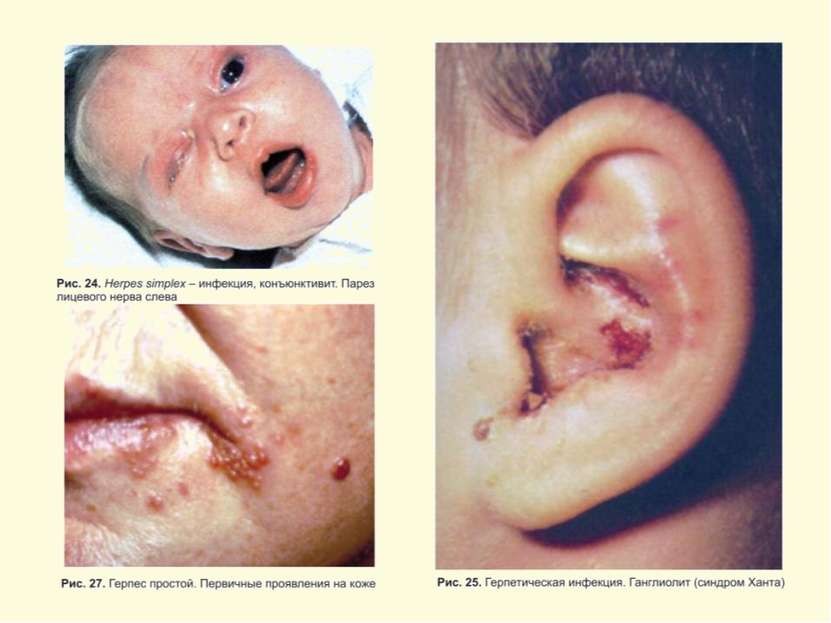
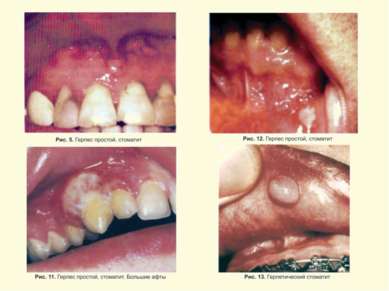
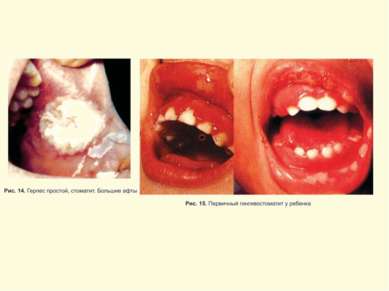
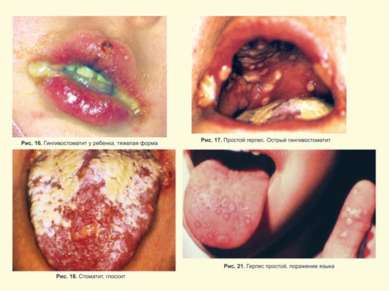
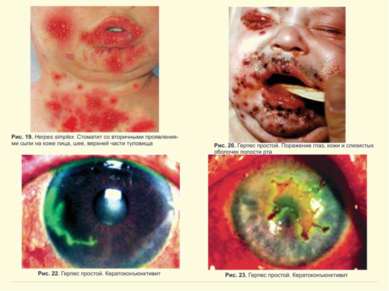
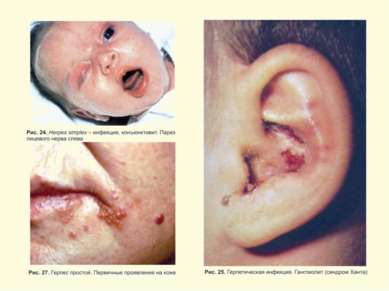
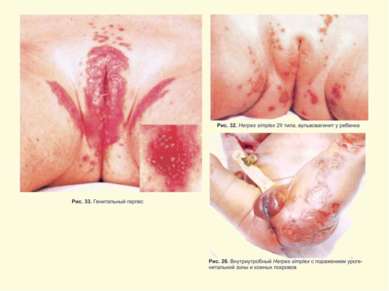
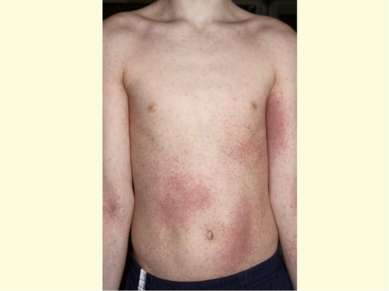
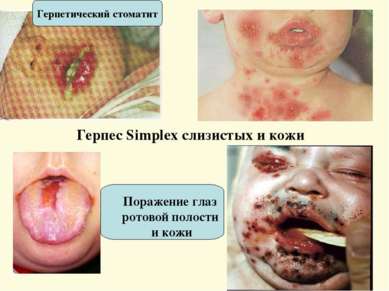 Герпес Simplex слизистых и кожи Поражение глаз ротовой полости и кожи Герпетический стоматит
Герпес Simplex слизистых и кожи Поражение глаз ротовой полости и кожи Герпетический стоматит
Cлайд 18
 Выявление антител к ВПГ - ИФА Важно знать: АТ к ВПГ выявляются у 90 – 97% у обследованных, не имеющих клинической симптоматики ГИ. Нарастание титров АТ к ВПГ происходит в поздние сроки, через несколько недель после заражения или реактивации вируса и может не наблюдаться у больных с ИДС. Титр АТ не всегда соответствует клиническим проявлениям инфекции: у части бессимптомных носителей выявляются АТ в высоких титрах, тогда как у части пациентов с выраженной симптоматикой титры АТ остаются низкими. АТ класса М-показатель активной инфекции после первичного инфицирования обнаруживаются в крови в течение нескольких месяцев или лет. Целесообразно исследовать парные сыворотки (интервал 7 -10 дней). 4-х кратное нарастание АТ к ВПГ класса IgG – показатель активной инфекции.
Выявление антител к ВПГ - ИФА Важно знать: АТ к ВПГ выявляются у 90 – 97% у обследованных, не имеющих клинической симптоматики ГИ. Нарастание титров АТ к ВПГ происходит в поздние сроки, через несколько недель после заражения или реактивации вируса и может не наблюдаться у больных с ИДС. Титр АТ не всегда соответствует клиническим проявлениям инфекции: у части бессимптомных носителей выявляются АТ в высоких титрах, тогда как у части пациентов с выраженной симптоматикой титры АТ остаются низкими. АТ класса М-показатель активной инфекции после первичного инфицирования обнаруживаются в крови в течение нескольких месяцев или лет. Целесообразно исследовать парные сыворотки (интервал 7 -10 дней). 4-х кратное нарастание АТ к ВПГ класса IgG – показатель активной инфекции.
Cлайд 19
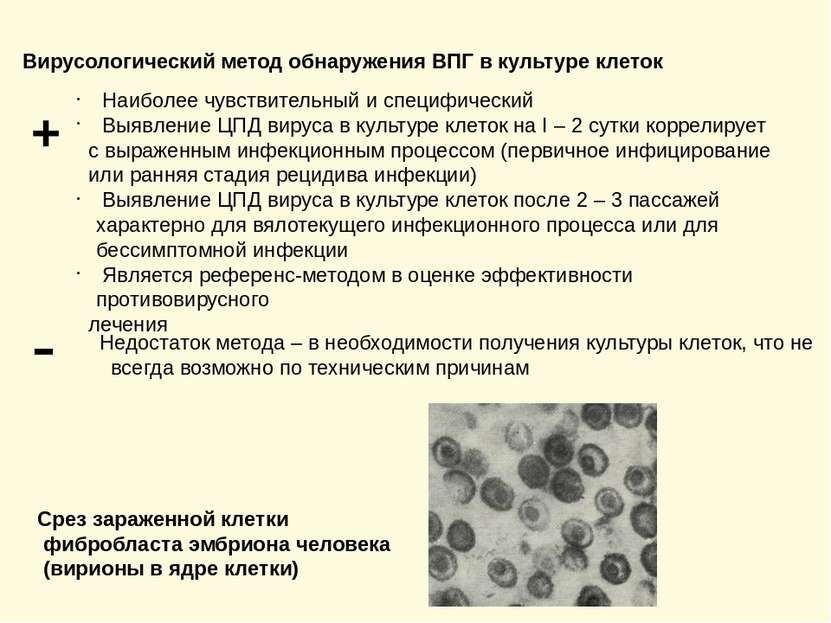
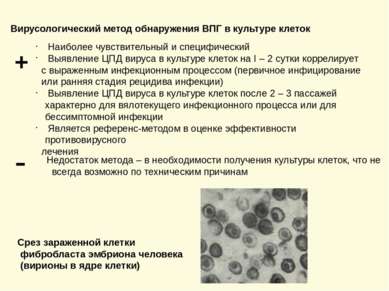 Вирусологический метод обнаружения ВПГ в культуре клеток + Наиболее чувствительный и специфический Выявление ЦПД вируса в культуре клеток на I – 2 сутки коррелирует с выраженным инфекционным процессом (первичное инфицирование или ранняя стадия рецидива инфекции) Выявление ЦПД вируса в культуре клеток после 2 – 3 пассажей характерно для вялотекущего инфекционного процесса или для бессимптомной инфекции Является референс-методом в оценке эффективности противовирусного лечения - Недостаток метода – в необходимости получения культуры клеток, что не всегда возможно по техническим причинам Срез зараженной клетки фибробласта эмбриона человека (вирионы в ядре клетки)
Вирусологический метод обнаружения ВПГ в культуре клеток + Наиболее чувствительный и специфический Выявление ЦПД вируса в культуре клеток на I – 2 сутки коррелирует с выраженным инфекционным процессом (первичное инфицирование или ранняя стадия рецидива инфекции) Выявление ЦПД вируса в культуре клеток после 2 – 3 пассажей характерно для вялотекущего инфекционного процесса или для бессимптомной инфекции Является референс-методом в оценке эффективности противовирусного лечения - Недостаток метода – в необходимости получения культуры клеток, что не всегда возможно по техническим причинам Срез зараженной клетки фибробласта эмбриона человека (вирионы в ядре клетки)
Cлайд 20
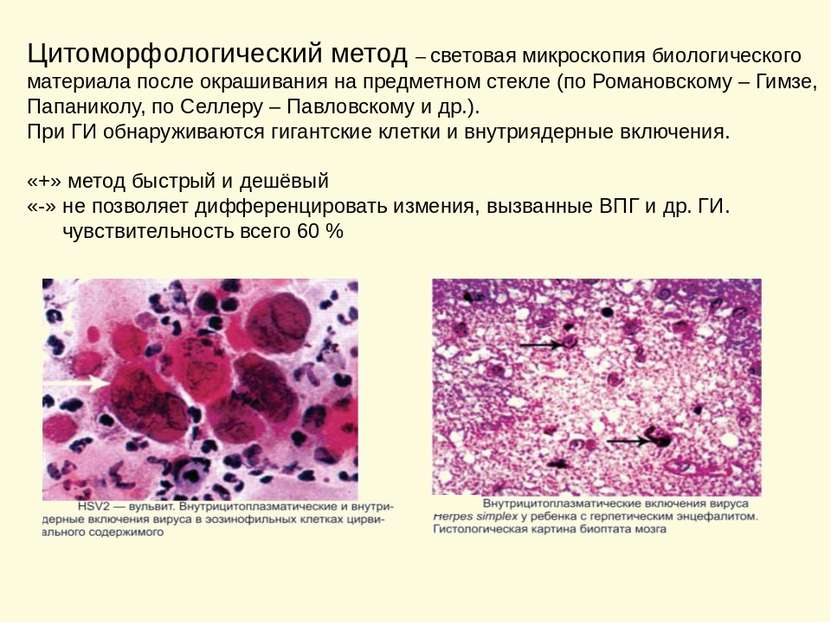
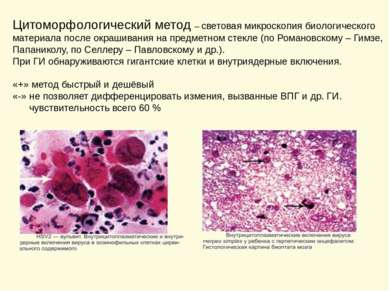 Цитоморфологический метод – световая микроскопия биологического материала после окрашивания на предметном стекле (по Романовскому – Гимзе, Папаниколу, по Селлеру – Павловскому и др.). При ГИ обнаруживаются гигантские клетки и внутриядерные включения. «+» метод быстрый и дешёвый «-» не позволяет дифференцировать измения, вызванные ВПГ и др. ГИ. чувствительность всего 60 %
Цитоморфологический метод – световая микроскопия биологического материала после окрашивания на предметном стекле (по Романовскому – Гимзе, Папаниколу, по Селлеру – Павловскому и др.). При ГИ обнаруживаются гигантские клетки и внутриядерные включения. «+» метод быстрый и дешёвый «-» не позволяет дифференцировать измения, вызванные ВПГ и др. ГИ. чувствительность всего 60 %
Cлайд 21
 Выявление ДНК ВПГ в ПЦР метод молекулярной биологии, позволяющий с помощью повторных циклов амплификации (копирования) добиться получения большого количества копий ДНК в биологическом материале .
Выявление ДНК ВПГ в ПЦР метод молекулярной биологии, позволяющий с помощью повторных циклов амплификации (копирования) добиться получения большого количества копий ДНК в биологическом материале .
Cлайд 22
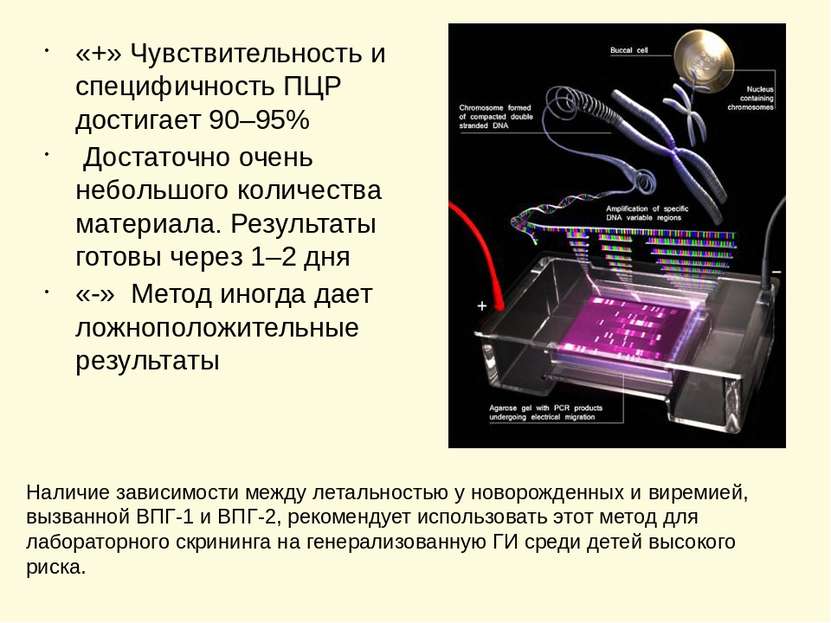
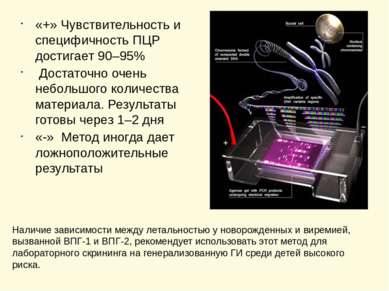 «+» Чувствительность и специфичность ПЦР достигает 90–95% Достаточно очень небольшого количества материала. Результаты готовы через 1–2 дня «-» Метод иногда дает ложноположительные результаты Наличие зависимости между летальностью у новорожденных и виремией, вызванной ВПГ-1 и ВПГ-2, рекомендует использовать этот метод для лабораторного скрининга на генерализованную ГИ среди детей высокого риска.
«+» Чувствительность и специфичность ПЦР достигает 90–95% Достаточно очень небольшого количества материала. Результаты готовы через 1–2 дня «-» Метод иногда дает ложноположительные результаты Наличие зависимости между летальностью у новорожденных и виремией, вызванной ВПГ-1 и ВПГ-2, рекомендует использовать этот метод для лабораторного скрининга на генерализованную ГИ среди детей высокого риска.
Cлайд 23
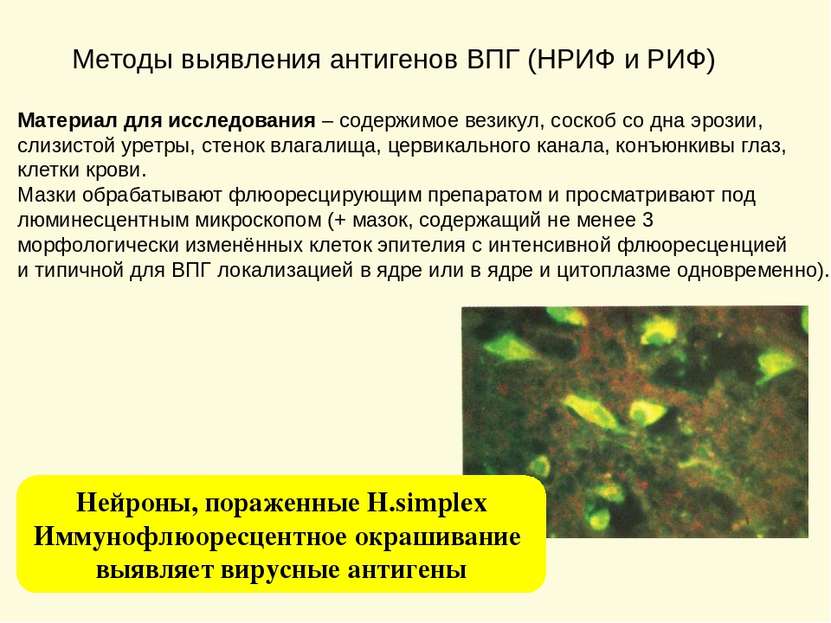
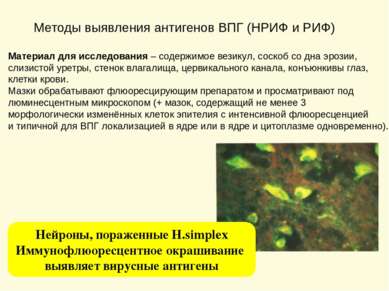 Методы выявления антигенов ВПГ (НРИФ и РИФ) Материал для исследования – содержимое везикул, соскоб со дна эрозии, слизистой уретры, стенок влагалища, цервикального канала, конъюнкивы глаз, клетки крови. Мазки обрабатывают флюоресцирующим препаратом и просматривают под люминесцентным микроскопом (+ мазок, содержащий не менее 3 морфологически изменённых клеток эпителия с интенсивной флюоресценцией и типичной для ВПГ локализацией в ядре или в ядре и цитоплазме одновременно). Нейроны, пораженные H.simplex Иммунофлюоресцентное окрашивание выявляет вирусные антигены
Методы выявления антигенов ВПГ (НРИФ и РИФ) Материал для исследования – содержимое везикул, соскоб со дна эрозии, слизистой уретры, стенок влагалища, цервикального канала, конъюнкивы глаз, клетки крови. Мазки обрабатывают флюоресцирующим препаратом и просматривают под люминесцентным микроскопом (+ мазок, содержащий не менее 3 морфологически изменённых клеток эпителия с интенсивной флюоресценцией и типичной для ВПГ локализацией в ядре или в ядре и цитоплазме одновременно). Нейроны, пораженные H.simplex Иммунофлюоресцентное окрашивание выявляет вирусные антигены
Cлайд 24
 Специфическая вакцинация против ВПГ-инфекции Санкт-Петербургская вакцина производится на клетках куриных фибробластов, московская - «Витагерпавак» - на стандартизированной в мировой практике линии клеток «Vero:B», более иммуногенна, содержит специфические антигены вируса герпеса 1 и 2 типов, которые стимулируют клеточные механизмы резистентности, восстанавливая функциональную активность лимфоцитов крови, а также обеспечивая высокую активность NK-1 клеток (нормальных киллеров). Форма выпуска Вакцину выпускают во флаконах емкостью 5 мл по 0,3 мл. Одна прививочная доза - 0,2 мл. В коробке - 5 флаконов и инструкция по применению. Способ применения и дозировка. Вакцинацию проводят в лечебных учреждениях (стационар, диспансер, поликлиника) под контролем врача. Вакцину применяют в стадии ремиссии, не ранее, чем через 5 дней после полного исчезновения клинических проявлений герпетической инфекции. Препарат вводят внутрикожно в область внутренней поверхности предплечья с помощью шприца в разовой дозе 0,2 мл (контроль - образование «лимонной корочки»). Курс вакцинации при герпетической инфекции кожи и слизистых состоит из 5 инъекций, которые проводят с интервалом в 7 дней - 10 дней (в зависимости от тяжести болезни). Больным, с осложненной герпетической инфекцией, 2-ю и последующие инъекции повторяют с интервалом в 10 дней. Через 6 месяцев проводят повторный курс вакцинации (5 инъекций).
Специфическая вакцинация против ВПГ-инфекции Санкт-Петербургская вакцина производится на клетках куриных фибробластов, московская - «Витагерпавак» - на стандартизированной в мировой практике линии клеток «Vero:B», более иммуногенна, содержит специфические антигены вируса герпеса 1 и 2 типов, которые стимулируют клеточные механизмы резистентности, восстанавливая функциональную активность лимфоцитов крови, а также обеспечивая высокую активность NK-1 клеток (нормальных киллеров). Форма выпуска Вакцину выпускают во флаконах емкостью 5 мл по 0,3 мл. Одна прививочная доза - 0,2 мл. В коробке - 5 флаконов и инструкция по применению. Способ применения и дозировка. Вакцинацию проводят в лечебных учреждениях (стационар, диспансер, поликлиника) под контролем врача. Вакцину применяют в стадии ремиссии, не ранее, чем через 5 дней после полного исчезновения клинических проявлений герпетической инфекции. Препарат вводят внутрикожно в область внутренней поверхности предплечья с помощью шприца в разовой дозе 0,2 мл (контроль - образование «лимонной корочки»). Курс вакцинации при герпетической инфекции кожи и слизистых состоит из 5 инъекций, которые проводят с интервалом в 7 дней - 10 дней (в зависимости от тяжести болезни). Больным, с осложненной герпетической инфекцией, 2-ю и последующие инъекции повторяют с интервалом в 10 дней. Через 6 месяцев проводят повторный курс вакцинации (5 инъекций).
Cлайд 25
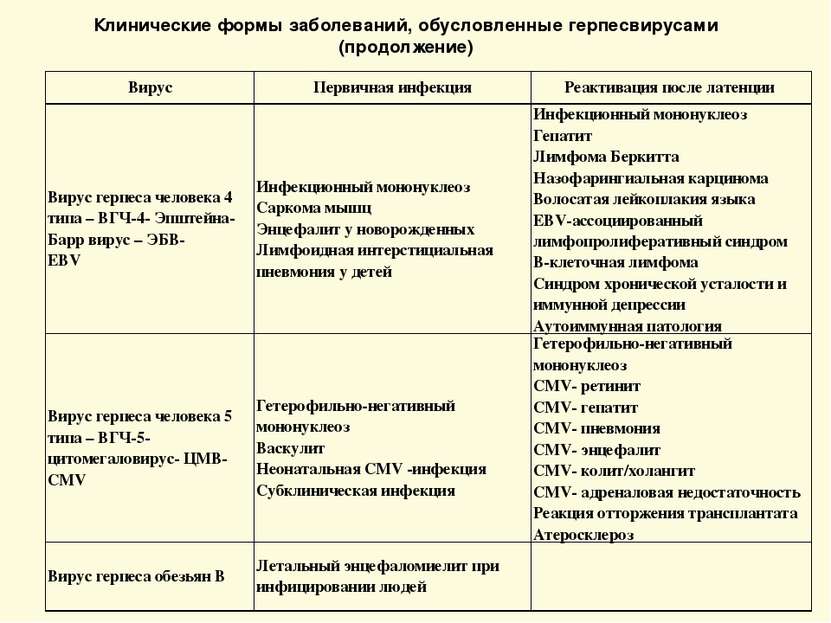
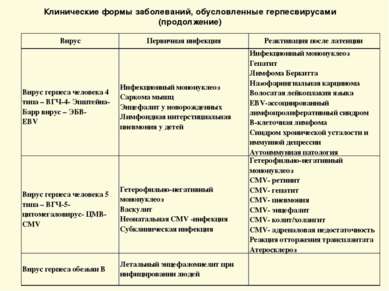 Клинические формы заболеваний, обусловленные герпесвирусами (продолжение) Вирус Первичная инфекция Реактивация после латенции Вирус герпеса человека 4 типа – ВГЧ-4- Эпштейна-Барр вирус – ЭБВ- EBV Инфекционный мононуклеоз Саркома мышц Энцефалит у новорожденных Лимфоидная интерстициальная пневмония у детей Инфекционный мононуклеоз Гепатит Лимфома Беркитта Назофарингиальная карцинома Волосатая лейкоплакия языка EBV-ассоциированный лимфопролиферативный синдром В-клеточная лимфома Синдром хронической усталости и иммунной депрессии Аутоиммунная патология Вирус герпеса человека 5 типа – ВГЧ-5-цитомегаловирус- ЦМВ-СMV Гетерофильно-негативный мононуклеоз Васкулит Неонатальная СMV -инфекция Субклиническая инфекция Гетерофильно-негативный мононуклеоз СMV- ретинит СMV- гепатит СMV- пневмония СMV- энцефалит СMV- колит/холангит СMV- адреналовая недостаточность Реакция отторжения трансплантата Атеросклероз Вирус герпеса обезьян В Летальный энцефаломиелит при инфицировании людей
Клинические формы заболеваний, обусловленные герпесвирусами (продолжение) Вирус Первичная инфекция Реактивация после латенции Вирус герпеса человека 4 типа – ВГЧ-4- Эпштейна-Барр вирус – ЭБВ- EBV Инфекционный мононуклеоз Саркома мышц Энцефалит у новорожденных Лимфоидная интерстициальная пневмония у детей Инфекционный мононуклеоз Гепатит Лимфома Беркитта Назофарингиальная карцинома Волосатая лейкоплакия языка EBV-ассоциированный лимфопролиферативный синдром В-клеточная лимфома Синдром хронической усталости и иммунной депрессии Аутоиммунная патология Вирус герпеса человека 5 типа – ВГЧ-5-цитомегаловирус- ЦМВ-СMV Гетерофильно-негативный мононуклеоз Васкулит Неонатальная СMV -инфекция Субклиническая инфекция Гетерофильно-негативный мононуклеоз СMV- ретинит СMV- гепатит СMV- пневмония СMV- энцефалит СMV- колит/холангит СMV- адреналовая недостаточность Реакция отторжения трансплантата Атеросклероз Вирус герпеса обезьян В Летальный энцефаломиелит при инфицировании людей
Cлайд 26
 По определению Инфекционный мононуклеоз – острое вирусное заболевание, характеризующееся: лихорадкой, увеличением лимфоузлов, гепато- и спленомегалией, появлением в крови атипичных мононуклеаров и гетерофильных антител.
По определению Инфекционный мононуклеоз – острое вирусное заболевание, характеризующееся: лихорадкой, увеличением лимфоузлов, гепато- и спленомегалией, появлением в крови атипичных мононуклеаров и гетерофильных антител.
Cлайд 27
 В Международной статистической классификации болезней и проблем, связанных со здоровьем десятого пересмотра (МКБ-10) ИМ включен в рубрику В 27. В понятие ИМ включены синонимы: железистая лихорадка, моноцитарная ангина, болезнь Пфейффера, существовавшие ранее. Далее по этиологическому признаку выделяются: В 27.0 Мононуклеоз, вызванный гамма-герпетическим вирусом. Мононуклеоз, вызванный вирусом Эпштейна-Барр В 27.1 Цитомегаловирусный мононуклеоз В 27.8 Другой инфекционный мононуклеоз В 27.9 Инфекционный мононуклеоз неуточненный. (ВОЗ. Женева, 1995 г.)
В Международной статистической классификации болезней и проблем, связанных со здоровьем десятого пересмотра (МКБ-10) ИМ включен в рубрику В 27. В понятие ИМ включены синонимы: железистая лихорадка, моноцитарная ангина, болезнь Пфейффера, существовавшие ранее. Далее по этиологическому признаку выделяются: В 27.0 Мононуклеоз, вызванный гамма-герпетическим вирусом. Мононуклеоз, вызванный вирусом Эпштейна-Барр В 27.1 Цитомегаловирусный мононуклеоз В 27.8 Другой инфекционный мононуклеоз В 27.9 Инфекционный мононуклеоз неуточненный. (ВОЗ. Женева, 1995 г.)
Cлайд 28
 - многие современные исследователи полагают, что ЦМВ-мононуклеоз чаще возникает после гемотрансфузий, наблюдается у детей старшего возраста и у беременных женщин вследствие реактивации латентного вируса. ( Белозеров Е.С. – 2005 г.; Гранитов В.М. – 2001 г.; Долгушина М.В.- 2004 г.; Кистенева Л.Б., Чешик С.Г.-2004 г; Прилуцкий А.С. – 2002 г.) зарубежные авторы описывают ЦМВ-мононуклеоз у подростков, детей и даже новорожденных. ( Lui, W.Y – 1972 г., Pannuti, C.S. et al – 1982 г, Ralph D. Feigin et al – 1998 г.) Первые сообщения о ЦМВ-мононуклеозе появились в Великобритании в 1965-1966 гг. в работах S.Lamb, E.Klemola, L.Kaariainen.
- многие современные исследователи полагают, что ЦМВ-мононуклеоз чаще возникает после гемотрансфузий, наблюдается у детей старшего возраста и у беременных женщин вследствие реактивации латентного вируса. ( Белозеров Е.С. – 2005 г.; Гранитов В.М. – 2001 г.; Долгушина М.В.- 2004 г.; Кистенева Л.Б., Чешик С.Г.-2004 г; Прилуцкий А.С. – 2002 г.) зарубежные авторы описывают ЦМВ-мононуклеоз у подростков, детей и даже новорожденных. ( Lui, W.Y – 1972 г., Pannuti, C.S. et al – 1982 г, Ralph D. Feigin et al – 1998 г.) Первые сообщения о ЦМВ-мононуклеозе появились в Великобритании в 1965-1966 гг. в работах S.Lamb, E.Klemola, L.Kaariainen.
Cлайд 29
 - это один из клинических вариантов острой фазы типичной ЦМВ-инфекции у иммунокомпетентного лица ( в другом варианте первичное заражение ЦМВ протекает бессимптомно). - или же следствие реактивации инфекции у иммуносупресси- рованных пациентов. Цитомегаловирусный мононуклеоз (Гранитов В.М. – 2001 г.; Самохин П.А. – 1987 г.; Чучалин А.Г. – 2006 г.; King K. Holmes et al – 1999 г; Ralpf D. Feigin – 1998 г.)
- это один из клинических вариантов острой фазы типичной ЦМВ-инфекции у иммунокомпетентного лица ( в другом варианте первичное заражение ЦМВ протекает бессимптомно). - или же следствие реактивации инфекции у иммуносупресси- рованных пациентов. Цитомегаловирусный мононуклеоз (Гранитов В.М. – 2001 г.; Самохин П.А. – 1987 г.; Чучалин А.Г. – 2006 г.; King K. Holmes et al – 1999 г; Ralpf D. Feigin – 1998 г.)
Cлайд 31
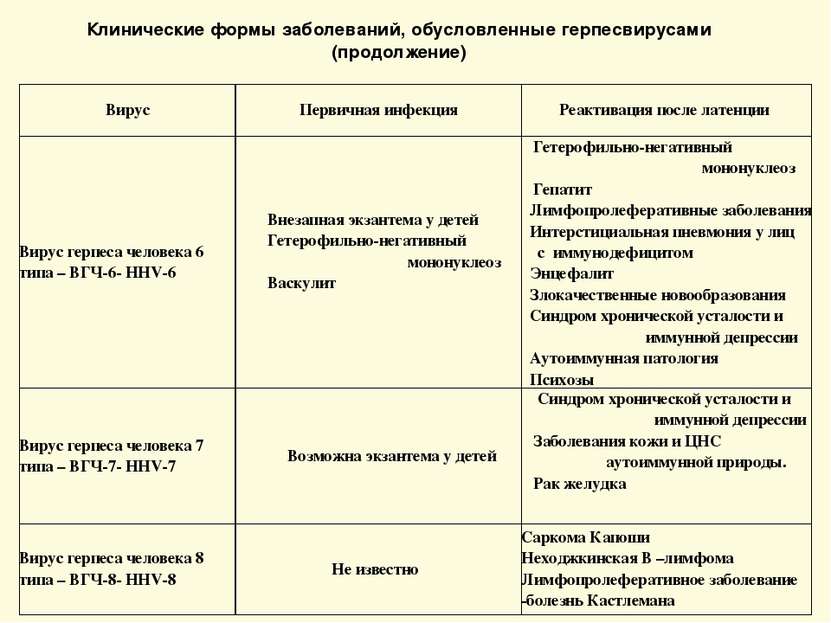
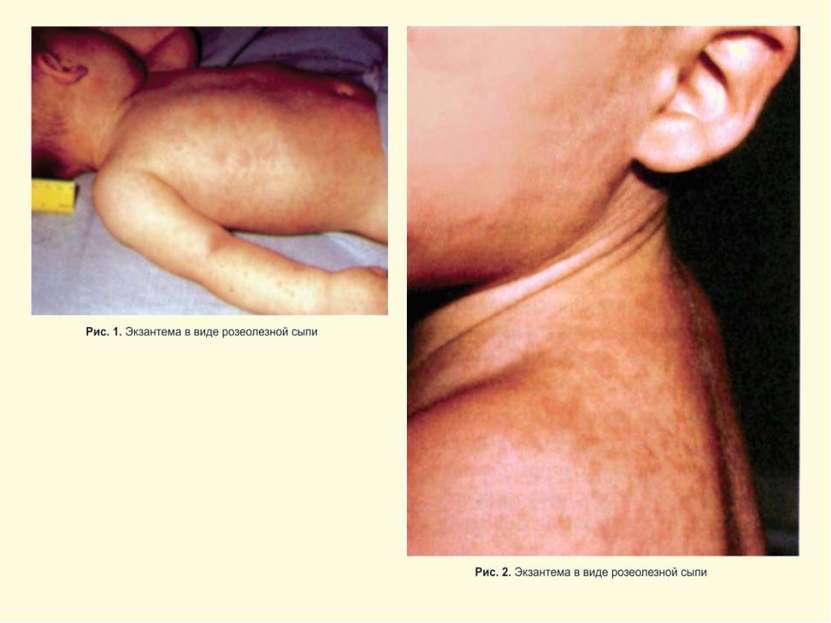
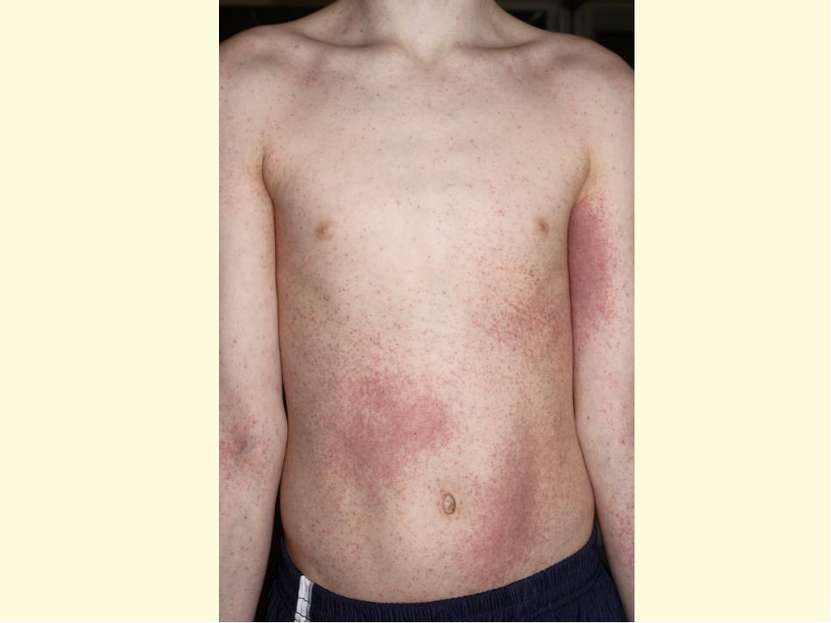
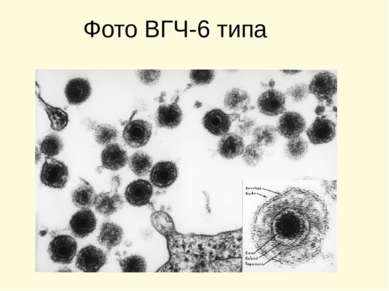
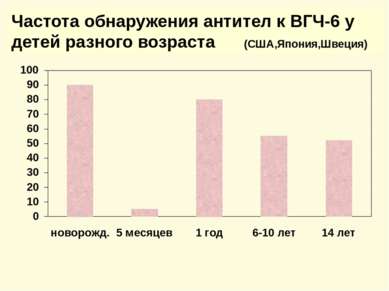
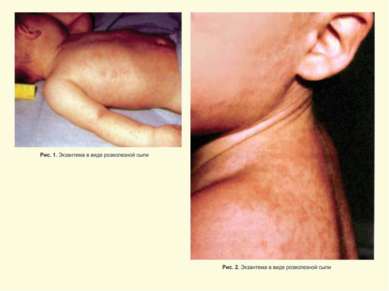
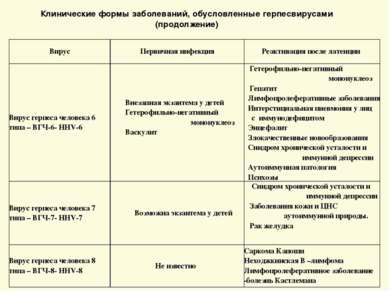 Клинические формы заболеваний, обусловленные герпесвирусами (продолжение) Вирус Первичная инфекция Реактивация после латенции Вирус герпеса человека 6 типа – ВГЧ-6- HHV-6 Внезапная экзантема у детей Гетерофильно-негативный мононуклеоз Васкулит Гетерофильно-негативный мононуклеоз Гепатит Лимфопролеферативные заболевания Интерстициальная пневмония у лиц с иммунодефицитом Энцефалит Злокачественные новообразования Синдром хронической усталости и иммунной депрессии Аутоиммунная патология Психозы Вирус герпеса человека 7 типа – ВГЧ-7- HHV-7 Возможна экзантема у детей Синдром хронической усталости и иммунной депрессии Заболевания кожи и ЦНС аутоиммунной природы. Рак желудка Вирус герпеса человека 8 типа – ВГЧ-8- HHV-8 Не известно Саркома Капоши Неходжкинская В –лимфома Лимфопролеферативное заболевание -болезнь Кастлемана
Клинические формы заболеваний, обусловленные герпесвирусами (продолжение) Вирус Первичная инфекция Реактивация после латенции Вирус герпеса человека 6 типа – ВГЧ-6- HHV-6 Внезапная экзантема у детей Гетерофильно-негативный мононуклеоз Васкулит Гетерофильно-негативный мононуклеоз Гепатит Лимфопролеферативные заболевания Интерстициальная пневмония у лиц с иммунодефицитом Энцефалит Злокачественные новообразования Синдром хронической усталости и иммунной депрессии Аутоиммунная патология Психозы Вирус герпеса человека 7 типа – ВГЧ-7- HHV-7 Возможна экзантема у детей Синдром хронической усталости и иммунной депрессии Заболевания кожи и ЦНС аутоиммунной природы. Рак желудка Вирус герпеса человека 8 типа – ВГЧ-8- HHV-8 Не известно Саркома Капоши Неходжкинская В –лимфома Лимфопролеферативное заболевание -болезнь Кастлемана
Cлайд 35
 ПАТОГЕНЕЗ ИНФЕКЦИОННОГО МОНОНУКЛЕОЗА ПЕРВИЧНАЯ РЕПЛИКАЦИЯ ВИРУСА В ЭПИТЕЛИИ РОТО- И НОСОГЛОТКИ и проникновение в В-лимфоциты (ЭБВ) и в Т-лимфоциты (ЦМВ и ВГЧ-6) ЛИМФОРЕТИКУЛЯРНАЯ СИСТЕМА - ДИССЕМИНАЦИЯ ВОЗБУДИТЕЛЯ РЕПЛИКАЦИЯ ВИРУСА С ИНТЕГРАЦИЕЙ ДНК В ГЕНОМ КЛЕТОК УВЕЛИЧЕНИЕ ЛИМФОУЗЛОВ, НОСОГЛОТОЧНОЙ МИНДАЛИНЫ, ТОНЗИЛОФАРИНГИТ, ГЕПАТО-, СПЛЕНОМЕГАЛИЯ, АТИПИЧНЫЕ МОНОНУКЛЕАРЫ (В и Т ЛИМФОЦИТЫ)
ПАТОГЕНЕЗ ИНФЕКЦИОННОГО МОНОНУКЛЕОЗА ПЕРВИЧНАЯ РЕПЛИКАЦИЯ ВИРУСА В ЭПИТЕЛИИ РОТО- И НОСОГЛОТКИ и проникновение в В-лимфоциты (ЭБВ) и в Т-лимфоциты (ЦМВ и ВГЧ-6) ЛИМФОРЕТИКУЛЯРНАЯ СИСТЕМА - ДИССЕМИНАЦИЯ ВОЗБУДИТЕЛЯ РЕПЛИКАЦИЯ ВИРУСА С ИНТЕГРАЦИЕЙ ДНК В ГЕНОМ КЛЕТОК УВЕЛИЧЕНИЕ ЛИМФОУЗЛОВ, НОСОГЛОТОЧНОЙ МИНДАЛИНЫ, ТОНЗИЛОФАРИНГИТ, ГЕПАТО-, СПЛЕНОМЕГАЛИЯ, АТИПИЧНЫЕ МОНОНУКЛЕАРЫ (В и Т ЛИМФОЦИТЫ)
Cлайд 36
 Диагностика инфекционного мононуклеоза у детей О- определение гетерофильных антител в крови О- определение антител к вирусам в крови О- определение вирусной ДНК в биологических средах П- определение вирусных антигенов в лейкоцитах крови (лимфоцитах и макрофагах)
Диагностика инфекционного мононуклеоза у детей О- определение гетерофильных антител в крови О- определение антител к вирусам в крови О- определение вирусной ДНК в биологических средах П- определение вирусных антигенов в лейкоцитах крови (лимфоцитах и макрофагах)
Cлайд 37
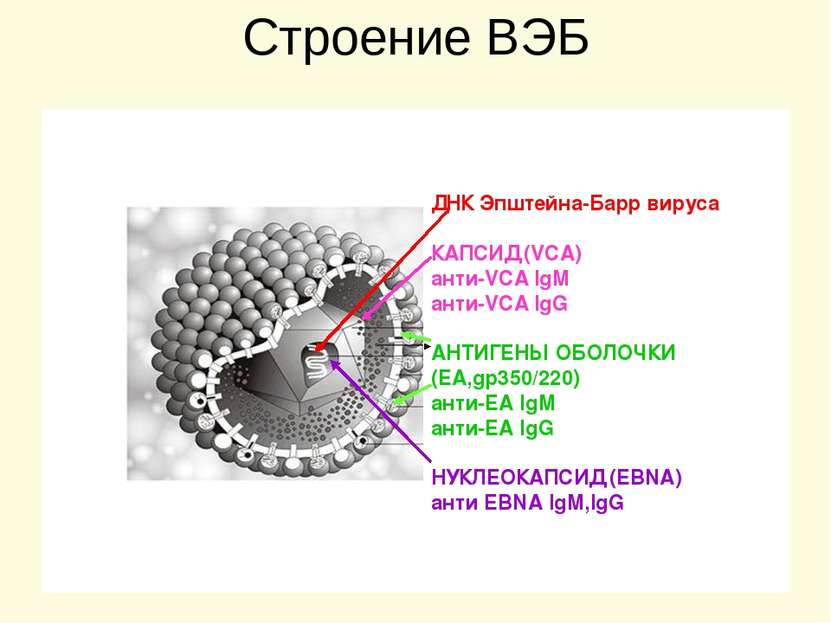
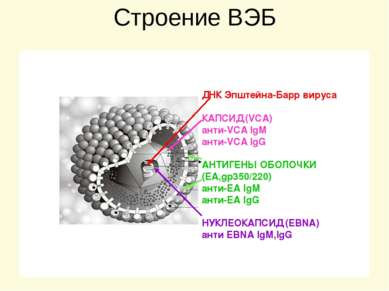 Строение ВЭБ ДНК Эпштейна-Барр вируса КАПСИД (VCA) анти-VCA IgM анти-VCA IgG АНТИГЕНЫ ОБОЛОЧКИ (ЕА,gp350/220) анти-ЕА IgM анти-ЕА IgG НУКЛЕОКАПСИД (EBNA) анти ЕBNА IgM,IgG
Строение ВЭБ ДНК Эпштейна-Барр вируса КАПСИД (VCA) анти-VCA IgM анти-VCA IgG АНТИГЕНЫ ОБОЛОЧКИ (ЕА,gp350/220) анти-ЕА IgM анти-ЕА IgG НУКЛЕОКАПСИД (EBNA) анти ЕBNА IgM,IgG
Cлайд 38
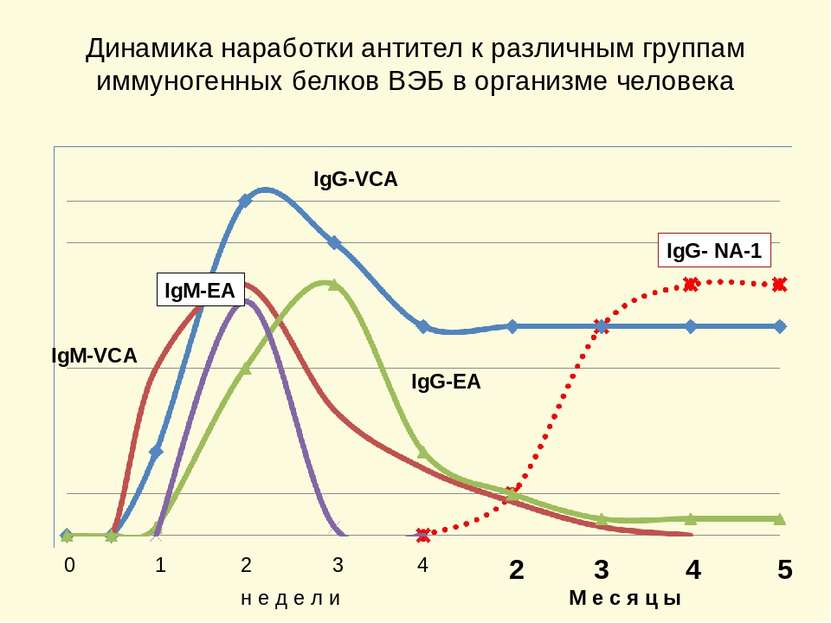
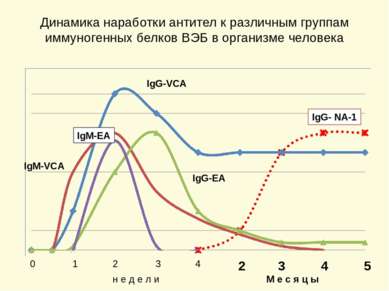 Динамика наработки антител к различным группам иммуногенных белков ВЭБ в организме человека 1 0 2 3 4 2 3 4 5 н е д е л и М е с я ц ы IgG-VCA IgM-VCA IgG-EA IgM-EA IgG- NA-1
Динамика наработки антител к различным группам иммуногенных белков ВЭБ в организме человека 1 0 2 3 4 2 3 4 5 н е д е л и М е с я ц ы IgG-VCA IgM-VCA IgG-EA IgM-EA IgG- NA-1
Cлайд 40
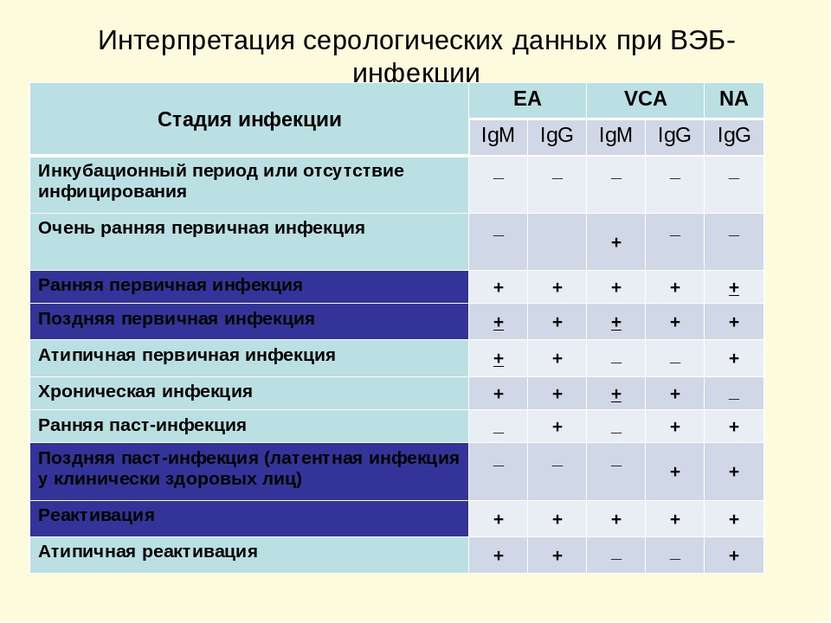
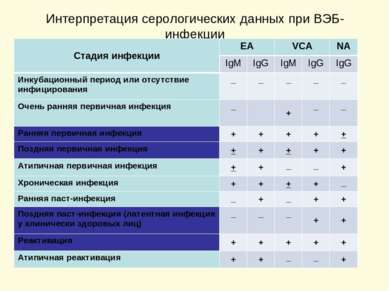 Интерпретация серологических данных при ВЭБ-инфекции Стадия инфекции EA VCA NA IgM IgG IgM IgG IgG Инкубационный период или отсутствие инфицирования _ _ _ _ _ Очень ранняя первичная инфекция _ + _ _ Ранняя первичная инфекция + + + + + Поздняя первичная инфекция + + + + + Атипичная первичная инфекция + + _ _ + Хроническая инфекция + + + + _ Ранняя паст-инфекция _ + _ + + Поздняя паст-инфекция (латентная инфекция у клинически здоровых лиц) _ _ _ + + Реактивация + + + + + Атипичная реактивация + + _ _ +
Интерпретация серологических данных при ВЭБ-инфекции Стадия инфекции EA VCA NA IgM IgG IgM IgG IgG Инкубационный период или отсутствие инфицирования _ _ _ _ _ Очень ранняя первичная инфекция _ + _ _ Ранняя первичная инфекция + + + + + Поздняя первичная инфекция + + + + + Атипичная первичная инфекция + + _ _ + Хроническая инфекция + + + + _ Ранняя паст-инфекция _ + _ + + Поздняя паст-инфекция (латентная инфекция у клинически здоровых лиц) _ _ _ + + Реактивация + + + + + Атипичная реактивация + + _ _ +
Cлайд 41
 Тесты выявления антигенов герпетических вирусов РИФ и НРИФ с использованием моноклональных антител к структурным антигенам вирусов в лимфоцитах крови, тест антигенемии, тест «кожное окно». БКМ - выявление структурных белков CMV в культуре клеток (ФЛЭЧ)
Тесты выявления антигенов герпетических вирусов РИФ и НРИФ с использованием моноклональных антител к структурным антигенам вирусов в лимфоцитах крови, тест антигенемии, тест «кожное окно». БКМ - выявление структурных белков CMV в культуре клеток (ФЛЭЧ)
Cлайд 42
 Методика антигенемии: Разделение лейкоцитов Приготовление мазков крови Фиксация Пероксидазное окрашивание используя моноклональные антитела к белку рр65 и рр72 Оценка результатов
Методика антигенемии: Разделение лейкоцитов Приготовление мазков крови Фиксация Пероксидазное окрашивание используя моноклональные антитела к белку рр65 и рр72 Оценка результатов
Cлайд 43
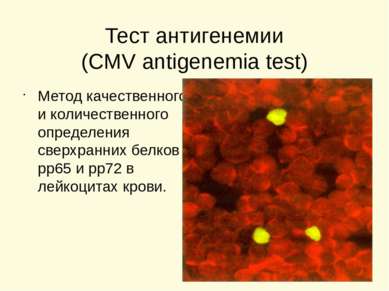 Тест антигенемии (CMV antigenemia test) Метод качественного и количественного определения сверхранних белков рр65 и рр72 в лейкоцитах крови.
Тест антигенемии (CMV antigenemia test) Метод качественного и количественного определения сверхранних белков рр65 и рр72 в лейкоцитах крови.
Cлайд 44
 БКМ (быстрый культуральный метод). Метод определения сверх ранних белков репликации ЦМВ рр65 и рр72, в культуре клеток фибробластов легкого эмбриона человека (ФЛЭЧ). Материалом для исследования служат слюна, кровь и моча больного. Плюсы. Метод позволяет определить инфекционноактивные вирусы в исследуемом материале, что исключает ложноположительные результаты. Минусы. Доступен только в хорошо оборудованных лабораториях.
БКМ (быстрый культуральный метод). Метод определения сверх ранних белков репликации ЦМВ рр65 и рр72, в культуре клеток фибробластов легкого эмбриона человека (ФЛЭЧ). Материалом для исследования служат слюна, кровь и моча больного. Плюсы. Метод позволяет определить инфекционноактивные вирусы в исследуемом материале, что исключает ложноположительные результаты. Минусы. Доступен только в хорошо оборудованных лабораториях.
Cлайд 45
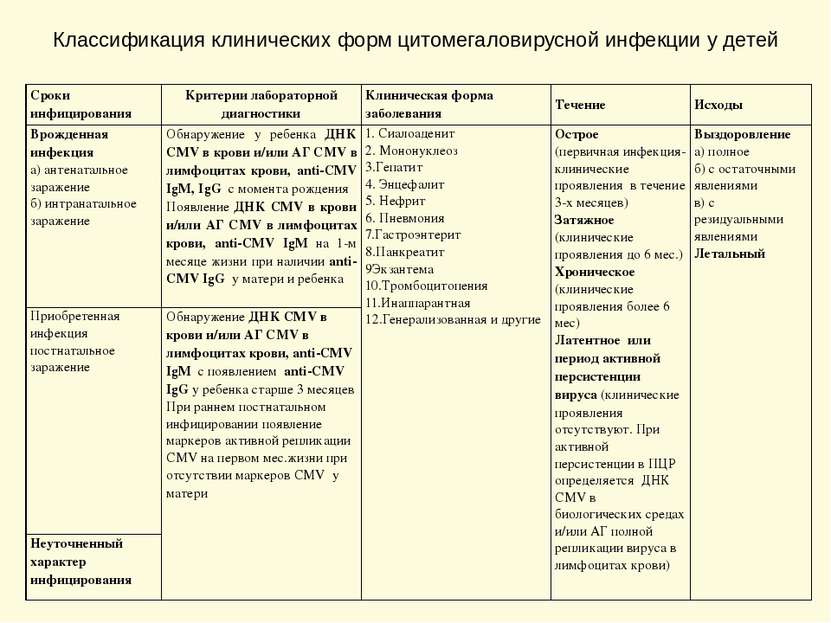
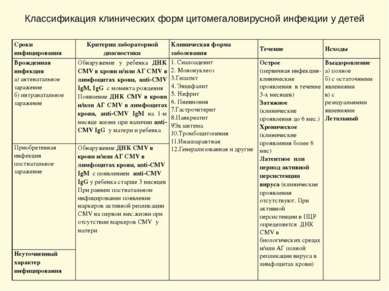 Классификация клинических форм цитомегаловирусной инфекции у детей Сроки инфицирования Критерии лабораторной диагностики Клиническая форма заболевания Течение Исходы Врожденная инфекция а) антенатальное заражение б) интранатальное заражение Обнаружение у ребенкаДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgM,IgGс момента рождения ПоявлениеДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgMна 1-м месяце жизни при наличииаnti-CMV IgGу матери и ребенка 1. Сиалоаденит 2. Мононуклеоз 3.Гепатит 4. Энцефалит 5. Нефрит 6. Пневмония 7.Гастроэнтерит 8.Панкреатит 9Экзантема 10.Тромбоцитопения 11.Инаппарантная 12.Генерализованная и другие Острое (первичная инфекция-клинические проявления в течение 3-х месяцев) Затяжное(клинические проявления до 6 мес.) Хроническое(клинические проявления более 6 мес) Латентное илипериод активной персистенции вируса(клинические проявления отсутствуют. При активной персистенции в ПЦР определяется ДНК СМVв биологических средах и/или АГ полной репликации вируса в лимфоцитах крови) Выздоровление а) полное б) с остаточными явлениями в) с резидуальными явлениями Летальный Приобретенная инфекция постнатальное заражение ОбнаружениеДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgMс появлениемаnti-CMV IgGу ребенка старше3 месяцев При раннем постнатальном инфицировании появление маркеров активной репликации СМVна первом мес.жизни при отсутствии маркеровCMVу матери Неуточненный характер инфицирования
Классификация клинических форм цитомегаловирусной инфекции у детей Сроки инфицирования Критерии лабораторной диагностики Клиническая форма заболевания Течение Исходы Врожденная инфекция а) антенатальное заражение б) интранатальное заражение Обнаружение у ребенкаДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgM,IgGс момента рождения ПоявлениеДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgMна 1-м месяце жизни при наличииаnti-CMV IgGу матери и ребенка 1. Сиалоаденит 2. Мононуклеоз 3.Гепатит 4. Энцефалит 5. Нефрит 6. Пневмония 7.Гастроэнтерит 8.Панкреатит 9Экзантема 10.Тромбоцитопения 11.Инаппарантная 12.Генерализованная и другие Острое (первичная инфекция-клинические проявления в течение 3-х месяцев) Затяжное(клинические проявления до 6 мес.) Хроническое(клинические проявления более 6 мес) Латентное илипериод активной персистенции вируса(клинические проявления отсутствуют. При активной персистенции в ПЦР определяется ДНК СМVв биологических средах и/или АГ полной репликации вируса в лимфоцитах крови) Выздоровление а) полное б) с остаточными явлениями в) с резидуальными явлениями Летальный Приобретенная инфекция постнатальное заражение ОбнаружениеДНКCMVв крови и/или АГ СМVв лимфоцитах крови, аnti-CMV IgMс появлениемаnti-CMV IgGу ребенка старше3 месяцев При раннем постнатальном инфицировании появление маркеров активной репликации СМVна первом мес.жизни при отсутствии маркеровCMVу матери Неуточненный характер инфицирования
Cлайд 46
 Лечение ИМ у детей Химиопрепараты, действующие непосредственно на вирусы Иммуномодуляторы Симптоматические средства Патогенетические средства
Лечение ИМ у детей Химиопрепараты, действующие непосредственно на вирусы Иммуномодуляторы Симптоматические средства Патогенетические средства
Cлайд 47
 Катамнез Дети подлежат диспансерному наблюдению в сроки 1, 3, 6 и 12 месяцев после выписки из стационара (контроль общего анализа крови, биохимии крови – (АлАТ, АсАТ, билирубин), ДНК EBV, CMV, HHV-6 в крови, слюне, и моче, АГ вирусов в лимфоцитах крови, АТ класса IgM и IgG к вирусам в крови, УЗИ органов брюшной полости).
Катамнез Дети подлежат диспансерному наблюдению в сроки 1, 3, 6 и 12 месяцев после выписки из стационара (контроль общего анализа крови, биохимии крови – (АлАТ, АсАТ, билирубин), ДНК EBV, CMV, HHV-6 в крови, слюне, и моче, АГ вирусов в лимфоцитах крови, АТ класса IgM и IgG к вирусам в крови, УЗИ органов брюшной полости).
Cлайд 48
 Клинический пример Полина З., 14.06.2007 г.р. В ноябре 2009 года – ОРВИ(?) (t до 39С, заложенность носа, увеличение лимфоузлов до 1 см, выраженная пастиозность лица) С 12.2009 – 5.2011 – 8 средних двусторонних гнойных отитов, протекающих на фоне нормальной температуры
Клинический пример Полина З., 14.06.2007 г.р. В ноябре 2009 года – ОРВИ(?) (t до 39С, заложенность носа, увеличение лимфоузлов до 1 см, выраженная пастиозность лица) С 12.2009 – 5.2011 – 8 средних двусторонних гнойных отитов, протекающих на фоне нормальной температуры
Cлайд 49
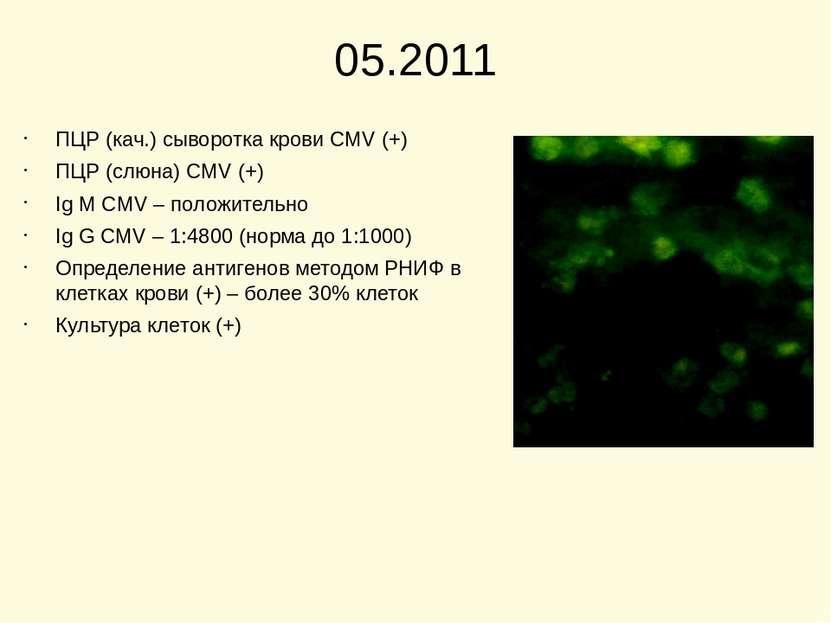
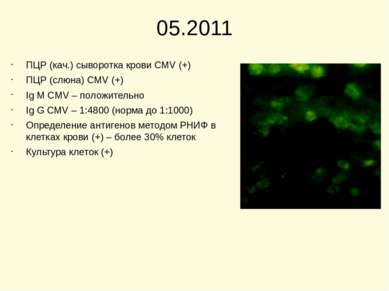 05.2011 ПЦР (кач.) сыворотка крови CMV (+) ПЦР (слюна) CMV (+) Ig M CMV – положительно Ig G CMV – 1:4800 (норма до 1:1000) Определение антигенов методом РНИФ в клетках крови (+) – более 30% клеток Культура клеток (+)
05.2011 ПЦР (кач.) сыворотка крови CMV (+) ПЦР (слюна) CMV (+) Ig M CMV – положительно Ig G CMV – 1:4800 (норма до 1:1000) Определение антигенов методом РНИФ в клетках крови (+) – более 30% клеток Культура клеток (+)