X
Код презентации скопируйте его
Железо – элемент побочной подгруппы
Скачать эту презентациюПрезентация на тему Железо – элемент побочной подгруппы
Скачать эту презентациюCлайд 4
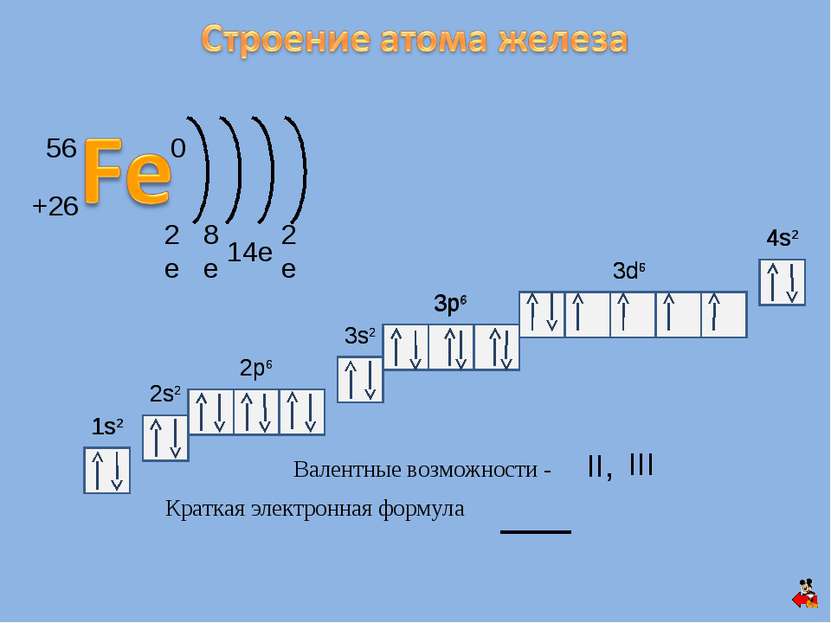
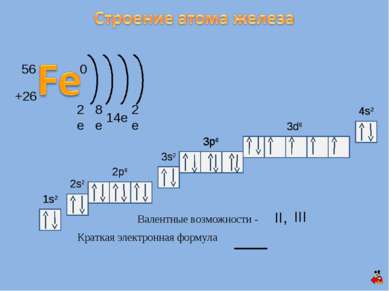 1s2 2s2 2p6 3s2 3p6 1s2 2s2 2p6 3s2 Краткая электронная формула Валентные возможности - II, III 3d6 4s2 +26 56 0 2e 8e 2e 14e 3p6 4s2 3d6 3d5
1s2 2s2 2p6 3s2 3p6 1s2 2s2 2p6 3s2 Краткая электронная формула Валентные возможности - II, III 3d6 4s2 +26 56 0 2e 8e 2e 14e 3p6 4s2 3d6 3d5
Cлайд 5
 Железо - сравнительно мягкий ковкий серебристо-серый металл. Температура плавления – 1535 0С Температура кипения около 2800 0С При температуре ниже 770 0С железо обладает ферромагнитными свойствами (оно легко намагничивается, и из него можно изготовить магнит). Выше этой температуры ферромагнитные свойства железа исчезают, железо «размагничивается».
Железо - сравнительно мягкий ковкий серебристо-серый металл. Температура плавления – 1535 0С Температура кипения около 2800 0С При температуре ниже 770 0С железо обладает ферромагнитными свойствами (оно легко намагничивается, и из него можно изготовить магнит). Выше этой температуры ферромагнитные свойства железа исчезают, железо «размагничивается».
Cлайд 7
 Восстановление из оксидов железа: Алюмотермия: 2Al + Fe2O3 = 2Fe + Al2O3 Водородом: 2Н2 + Fe3O4 = 3Fe + 4H2O
Восстановление из оксидов железа: Алюмотермия: 2Al + Fe2O3 = 2Fe + Al2O3 Водородом: 2Н2 + Fe3O4 = 3Fe + 4H2O
Cлайд 8
 Когда открыто железо никто не знает и не узнает, так как это было слишком давно. Но пользуются железом до сих пор, и в настоящее время железо не заменимо в промышленности и труде.
Когда открыто железо никто не знает и не узнает, так как это было слишком давно. Но пользуются железом до сих пор, и в настоящее время железо не заменимо в промышленности и труде.