X
Код презентации скопируйте его
Соли аммония
Скачать эту презентациюПрезентация на тему Соли аммония
Скачать эту презентациюCлайд 2
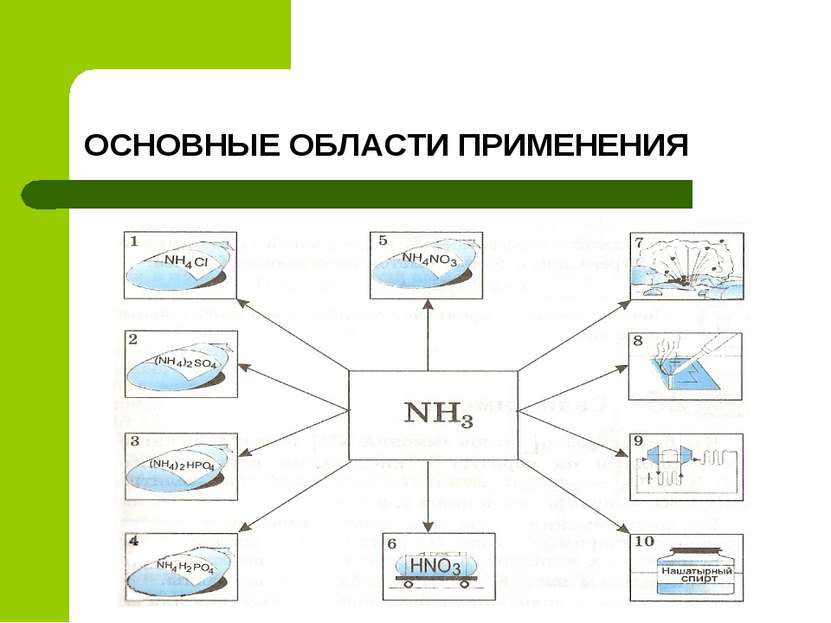
 КАТИОН АМОНИЯ Катион аммония NH4 играет роль катиона метала и образует с кислотными остатками соли: NH4NO3 – нитрат аммония, или аммиачная селитра. (NH4)2 SO4 – сульфат аммония.
КАТИОН АМОНИЯ Катион аммония NH4 играет роль катиона метала и образует с кислотными остатками соли: NH4NO3 – нитрат аммония, или аммиачная селитра. (NH4)2 SO4 – сульфат аммония.
Cлайд 3
 СОЛИ АММОНИЯ СОЛИ АММОНИЯ – ТВЁРДЫЕ КРИСТАЛИЧЕСКИЕ ВЕЩЕСТВА, ХОРОШО РАСТВОРИМЫЕ В ВОДЕ. по ряду свойств они похожи на соли щелочных металлов, и в первую очередь на соли калия, так как радиусы ионов калия и NH4 приблизительно равны. Соли аммония получают взаимодействием аммиака или его водного раствора с кислотами.
СОЛИ АММОНИЯ СОЛИ АММОНИЯ – ТВЁРДЫЕ КРИСТАЛИЧЕСКИЕ ВЕЩЕСТВА, ХОРОШО РАСТВОРИМЫЕ В ВОДЕ. по ряду свойств они похожи на соли щелочных металлов, и в первую очередь на соли калия, так как радиусы ионов калия и NH4 приблизительно равны. Соли аммония получают взаимодействием аммиака или его водного раствора с кислотами.
Cлайд 4
 Соли аммония обладают всеми свойствами солей, обусловленными наличием кислотных остатков. Карбонат аммония взаимодействует с кислотами, так как в результате реакции образуется углекислый газ. Ион аммония обусловливает другое, общее для всех солей аммония, свойство: его соли реагируют с щелочами при нагревании с выделением аммиака, например: NH4Cl+NaOH=NH3+H2O+NaCl
Соли аммония обладают всеми свойствами солей, обусловленными наличием кислотных остатков. Карбонат аммония взаимодействует с кислотами, так как в результате реакции образуется углекислый газ. Ион аммония обусловливает другое, общее для всех солей аммония, свойство: его соли реагируют с щелочами при нагревании с выделением аммиака, например: NH4Cl+NaOH=NH3+H2O+NaCl