X
Код презентации скопируйте его
Белирий, магний и щелочноземельные металлы
Скачать эту презентациюПрезентация на тему Белирий, магний и щелочноземельные металлы
Скачать эту презентациюCлайд 2
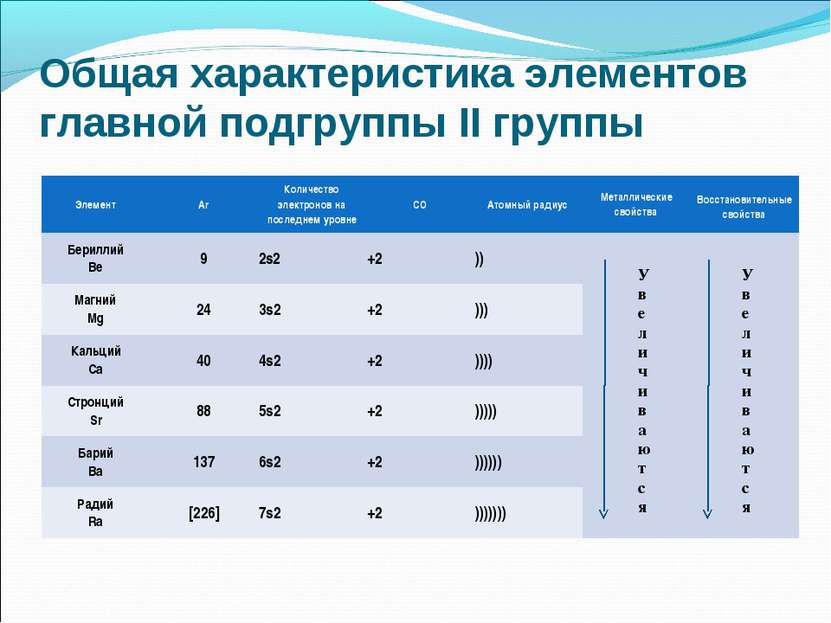
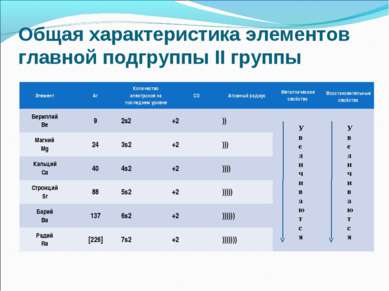 Общая характеристика элементов главной подгруппы II группы У в е л и ч и в а ю т с я У в е л и ч и в а ю т с я Элемент Ar Количество электронов на последнем уровне СО Атомный радиус Металлические свойства Восстановительные свойства Бериллий Be 9 2s2 +2 )) Магний Mg 24 3s2 +2 ))) Кальций Ca 40 4s2 +2 )))) Стронций Sr 88 5s2 +2 ))))) Барий Ba 137 6s2 +2 )))))) Радий Ra [226] 7s2 +2 )))))))
Общая характеристика элементов главной подгруппы II группы У в е л и ч и в а ю т с я У в е л и ч и в а ю т с я Элемент Ar Количество электронов на последнем уровне СО Атомный радиус Металлические свойства Восстановительные свойства Бериллий Be 9 2s2 +2 )) Магний Mg 24 3s2 +2 ))) Кальций Ca 40 4s2 +2 )))) Стронций Sr 88 5s2 +2 ))))) Барий Ba 137 6s2 +2 )))))) Радий Ra [226] 7s2 +2 )))))))
Cлайд 3
 Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент
Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент
Cлайд 4
 Общая характеристика элементов главной подгруппы II группы Одинаковое строение внешнего электронного слоя Элементы проявляют СО +2 Атомы элементов являются сильными восстановителями, т.к содержат 2 электрона на внешнем энергетическом уровне, которые отдают при взаимодействиями с другими элементами. С увеличением № элементов увеличивается атомный радиус, увеличивается число электронных слоев, следовательно возрастает легкость отдачи электронов. Восстановительные свойства увеличиваются в группе сверху вниз.
Общая характеристика элементов главной подгруппы II группы Одинаковое строение внешнего электронного слоя Элементы проявляют СО +2 Атомы элементов являются сильными восстановителями, т.к содержат 2 электрона на внешнем энергетическом уровне, которые отдают при взаимодействиями с другими элементами. С увеличением № элементов увеличивается атомный радиус, увеличивается число электронных слоев, следовательно возрастает легкость отдачи электронов. Восстановительные свойства увеличиваются в группе сверху вниз.
Cлайд 5
 Be – светло-серый, твердый, хрупкий Ca – твердый, пластичный Mg – относительно мягкий, пластичный, ковкий Sr – ковкий
Be – светло-серый, твердый, хрупкий Ca – твердый, пластичный Mg – относительно мягкий, пластичный, ковкий Sr – ковкий
Cлайд 7
 Химические свойства элементов II группы главной подгруппы 1.С кислородом 2M+O2=2MO (оксид) 2.С галогенами M+Cl2=MCl2 (хлорид) 3.С серой M+S=MS (сульфид) 4.С азотом 3M+N2=M3N2 (нитрид) 5.С водородом M+H2=MH2 (гидрид) 6.С водой M+2H2O=M(OH)2+H2
Химические свойства элементов II группы главной подгруппы 1.С кислородом 2M+O2=2MO (оксид) 2.С галогенами M+Cl2=MCl2 (хлорид) 3.С серой M+S=MS (сульфид) 4.С азотом 3M+N2=M3N2 (нитрид) 5.С водородом M+H2=MH2 (гидрид) 6.С водой M+2H2O=M(OH)2+H2
Cлайд 8
 Химические свойства оксидов BeO – амфотерный оксид MgO CaO SrO Основные оксиды BaO Оксид кальция СаО (негашеная известь)
Химические свойства оксидов BeO – амфотерный оксид MgO CaO SrO Основные оксиды BaO Оксид кальция СаО (негашеная известь)