X
Код презентации скопируйте его
Металлы
Скачать эту презентациюПрезентация на тему Металлы
Скачать эту презентациюCлайд 2
 Металлы (от лат. metallum – шахта, рудник): группа элементов, обладающая харак- терными металлическими свойствами, такими как высокие электро- и тепло- проводность, положительный тем- пературный коэффициент сопротив- ления, высокая пластичность и метал- лический блеск.
Металлы (от лат. metallum – шахта, рудник): группа элементов, обладающая харак- терными металлическими свойствами, такими как высокие электро- и тепло- проводность, положительный тем- пературный коэффициент сопротив- ления, высокая пластичность и метал- лический блеск.
Cлайд 3
 Химические свойства металлов Все металлы проявляют только восстановительные свойства Атомы металлов легко отдают электроны внешнего (а некоторые – и предвнешнего) электронного слоя, превращаясь в положительные ионы. Металлы имеют большой атомный радиус и малое число электронов (от 1 до 3) на внешнем слое. Исключение: Ge, Sn, Pb ─ 4 электрона; Sb, Bi ─ 5 электронов; Po ─ 6 электронов
Химические свойства металлов Все металлы проявляют только восстановительные свойства Атомы металлов легко отдают электроны внешнего (а некоторые – и предвнешнего) электронного слоя, превращаясь в положительные ионы. Металлы имеют большой атомный радиус и малое число электронов (от 1 до 3) на внешнем слое. Исключение: Ge, Sn, Pb ─ 4 электрона; Sb, Bi ─ 5 электронов; Po ─ 6 электронов
Cлайд 4
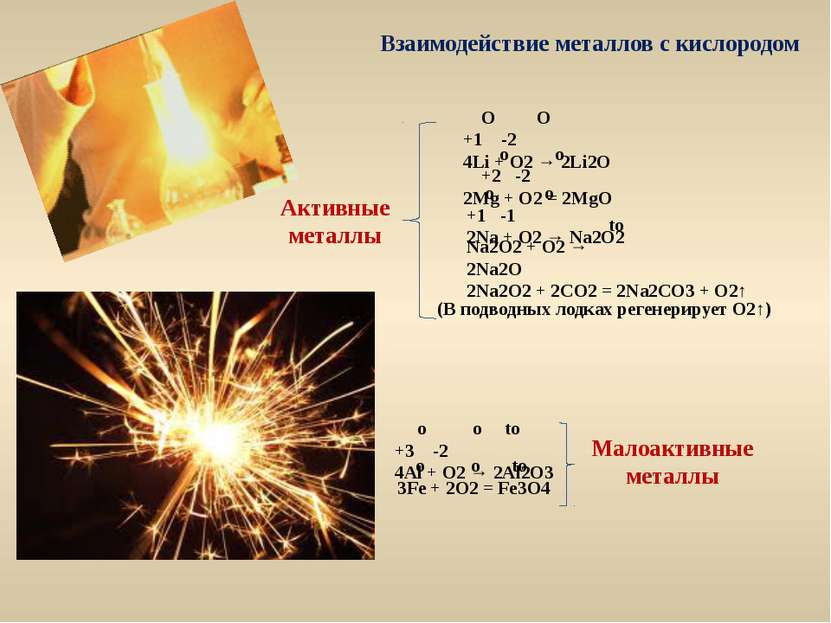
 Взаимодействие металлов с кислородом Активные металлы O O +1 -2 4Li + O2 → 2Li2O o o +2 -2 2Mg + O2 = 2MgO o o +1 -1 2Na + O2 → Na2O2 to Na2O2 + O2 → 2Na2O 2Na2O2 + 2CO2 = 2Na2CO3 + O2↑ (В подводных лодках регенерирует О2↑) Малоактивные металлы o o to +3 -2 4Al + O2 → 2Al2O3 o o to 3Fe + 2O2 = Fe3O4
Взаимодействие металлов с кислородом Активные металлы O O +1 -2 4Li + O2 → 2Li2O o o +2 -2 2Mg + O2 = 2MgO o o +1 -1 2Na + O2 → Na2O2 to Na2O2 + O2 → 2Na2O 2Na2O2 + 2CO2 = 2Na2CO3 + O2↑ (В подводных лодках регенерирует О2↑) Малоактивные металлы o o to +3 -2 4Al + O2 → 2Al2O3 o o to 3Fe + 2O2 = Fe3O4
Cлайд 5
 Взаимодействие металлов с галогенами o o +1 -1 2Na + Cl2 → 2NaCl o +3 -1 2Sb + 2Cl2 → 2SbCl3 o +5 -1 2Sb + 5Cl2 → 2SbCl5 o o +3 -1 2Fe + 3Cl2 → 2FeCl3 Поваренная соль Взаимодействие металлов с серой o o +2 -2 Fe + S → FeS o o H2O +3 -2 2Al + 3S → Al2S3 Взаимодействие металлов с водой o +1 +1 -1 o 2Me + 2H2O = 2MeOH + H2 (Щелочные и щелочно-земельные металлы) o +1 to 3Fe + 4H2O → Fe3O4 + 4H2↑ (малоактивные)
Взаимодействие металлов с галогенами o o +1 -1 2Na + Cl2 → 2NaCl o +3 -1 2Sb + 2Cl2 → 2SbCl3 o +5 -1 2Sb + 5Cl2 → 2SbCl5 o o +3 -1 2Fe + 3Cl2 → 2FeCl3 Поваренная соль Взаимодействие металлов с серой o o +2 -2 Fe + S → FeS o o H2O +3 -2 2Al + 3S → Al2S3 Взаимодействие металлов с водой o +1 +1 -1 o 2Me + 2H2O = 2MeOH + H2 (Щелочные и щелочно-земельные металлы) o +1 to 3Fe + 4H2O → Fe3O4 + 4H2↑ (малоактивные)
Cлайд 6
 o +1 -1 +2 -1 o Zn + 2HCl → ZnCl2 + H2 Взаимодействие металлов с кислотами o + +2 o Zn + 2H → Zn + H2 o + 2+ o 2CH3COOH + Zn → (CH3COO)2Zn + H2 o + 2+ o Zn + 2H → Zn + H2↑ o +1 o 2C2H5OH + 2Na → 2C2H5ONa + H2↑ +1 o +1 o 2C6H5OH + 2Na → 2C6H5ONa + H2 Взаимодействие металлов с солями Fe + CuSO4 → Cu↓ +FeSO4 o 2+ o 2+ Fe + Cu → Cu + Fe (окислительно-восстановительная реакция) o Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓ o + 2+ o Cu + 2Ag → Cu + Ag↓
o +1 -1 +2 -1 o Zn + 2HCl → ZnCl2 + H2 Взаимодействие металлов с кислотами o + +2 o Zn + 2H → Zn + H2 o + 2+ o 2CH3COOH + Zn → (CH3COO)2Zn + H2 o + 2+ o Zn + 2H → Zn + H2↑ o +1 o 2C2H5OH + 2Na → 2C2H5ONa + H2↑ +1 o +1 o 2C6H5OH + 2Na → 2C6H5ONa + H2 Взаимодействие металлов с солями Fe + CuSO4 → Cu↓ +FeSO4 o 2+ o 2+ Fe + Cu → Cu + Fe (окислительно-восстановительная реакция) o Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓ o + 2+ o Cu + 2Ag → Cu + Ag↓
Cлайд 7
 Металлотермия Некоторые активные металлы – литий, магний, кальций, алюминий – способны вытеснять другие металлы из их оксидов. Это свойство используют для получения некоторых металлов, а также для приготовления термитных смесей. o +3 +3 o 2Al + Cr2O3 = Al2O3 + 2Cr
Металлотермия Некоторые активные металлы – литий, магний, кальций, алюминий – способны вытеснять другие металлы из их оксидов. Это свойство используют для получения некоторых металлов, а также для приготовления термитных смесей. o +3 +3 o 2Al + Cr2O3 = Al2O3 + 2Cr
Cлайд 8
 Коррозия металлов Самопроизвольное разрушение металлов и сплавов под воздействием окружающей среды. (от лат. сorrosio - разъедать) Электрохимическая коррозия Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов o 2+ Fe – 2e → Fe + o 2H + 2e → H2 o + 2+ o Fe + 2H → Fe + H2↑ (на железе) (на меди) Химическая коррозия Взаимодействие поверхности металла с коррозионно-активной средой , не сопровождающееся возникновением электрохимических процессов на границе фаз 4Fe + 3O2 + 6H2O = 4Fe(OH)3↓
Коррозия металлов Самопроизвольное разрушение металлов и сплавов под воздействием окружающей среды. (от лат. сorrosio - разъедать) Электрохимическая коррозия Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов o 2+ Fe – 2e → Fe + o 2H + 2e → H2 o + 2+ o Fe + 2H → Fe + H2↑ (на железе) (на меди) Химическая коррозия Взаимодействие поверхности металла с коррозионно-активной средой , не сопровождающееся возникновением электрохимических процессов на границе фаз 4Fe + 3O2 + 6H2O = 4Fe(OH)3↓
Cлайд 9
 Защита от коррозии В зависимости от причин, вызывающих коррозию, различают следующие методы защиты: Защитные покрытия. Для изоляции металла от окружающей среды на него наносят различного рода покрытия: лаки, краски, эмали. Обработка внешней среды, в которой протекает коррозия. Для максимального замедления процесса коррозии в окружающую среду вводят ингибиторы. Электрохимическая защита – протекторная и катодная. Протекторная – защищаемое от коррозии изделие соединяют с металлическим ломом из более электроотрицательного металла (протекторная). Катодная – защищаемая конструкция, находящаяся в электролите (почвенная вода), подсоединяется к катоду внешнего источника тока. Покрытие слоем другого металла (Au, Ag, Cr, Ni, Zn. Sn- или Pb-лужение). Использование нержавеющих сплавов (хрома, никеля, титана). (Fe +H2SO4 – добавляют HNO3) Памятник Ю.А.Гагарину в Москве, выполненный из титана
Защита от коррозии В зависимости от причин, вызывающих коррозию, различают следующие методы защиты: Защитные покрытия. Для изоляции металла от окружающей среды на него наносят различного рода покрытия: лаки, краски, эмали. Обработка внешней среды, в которой протекает коррозия. Для максимального замедления процесса коррозии в окружающую среду вводят ингибиторы. Электрохимическая защита – протекторная и катодная. Протекторная – защищаемое от коррозии изделие соединяют с металлическим ломом из более электроотрицательного металла (протекторная). Катодная – защищаемая конструкция, находящаяся в электролите (почвенная вода), подсоединяется к катоду внешнего источника тока. Покрытие слоем другого металла (Au, Ag, Cr, Ni, Zn. Sn- или Pb-лужение). Использование нержавеющих сплавов (хрома, никеля, титана). (Fe +H2SO4 – добавляют HNO3) Памятник Ю.А.Гагарину в Москве, выполненный из титана
Cлайд 10
 Нельзя допустить, чтобы люди направляли на свое собственное уничтожение те силы природы, которые они сумели открыть и покорить. Ф. Жолио-Кюри Польза и вред металлов для человека + _ Кадмий – накапливаясь в почках, приводит к гипертонии, снижению иммунитета, слабоумию. Содержится в табачном дыме, питьевой воде, загрязненном воздухе Алюминий – старческое слабоумие, нарушение вазомоторных реакций, анемия, заболевание почек и печени. Пищевая фольга, посуда, пивные банки. Свинец - нарушение мозговой деятельности, раковые заболевания, нарушение детородной функции у женщин. Загрязненный воздух – выхлопные газы автомобилей Кальций – основа структурной костной ткани организма человека. Самое необходимое для человека минеральное вещество. Медь - играет важную роль в обеспечении иммунной защиты, в том числе противорадиационной и противораковой, участвует в энергетическом обмене и кроветворении, в образовании защитного пигмента кожи меланина Железо - необходимо для жизни, для образования гемоглобина (красных кровяных телец), миоглобина (красный пигмент в мышцах) и некоторых ферментов
Нельзя допустить, чтобы люди направляли на свое собственное уничтожение те силы природы, которые они сумели открыть и покорить. Ф. Жолио-Кюри Польза и вред металлов для человека + _ Кадмий – накапливаясь в почках, приводит к гипертонии, снижению иммунитета, слабоумию. Содержится в табачном дыме, питьевой воде, загрязненном воздухе Алюминий – старческое слабоумие, нарушение вазомоторных реакций, анемия, заболевание почек и печени. Пищевая фольга, посуда, пивные банки. Свинец - нарушение мозговой деятельности, раковые заболевания, нарушение детородной функции у женщин. Загрязненный воздух – выхлопные газы автомобилей Кальций – основа структурной костной ткани организма человека. Самое необходимое для человека минеральное вещество. Медь - играет важную роль в обеспечении иммунной защиты, в том числе противорадиационной и противораковой, участвует в энергетическом обмене и кроветворении, в образовании защитного пигмента кожи меланина Железо - необходимо для жизни, для образования гемоглобина (красных кровяных телец), миоглобина (красный пигмент в мышцах) и некоторых ферментов