X
Код презентации скопируйте его
Горение металлов
Скачать эту презентациюПрезентация на тему Горение металлов
Скачать эту презентациюCлайд 2
 Свойства летучих горючих металлов и их оксидов На способность металлов возгораться и гореть большое влияние оказывают химические и физические свойства металлов и их оксидов. Металлы Температура, оС Оксиды металлов Температура, оС плавления кипения воспламенения плавления кипения калий 64 760 69 K2O 527 1477 натрий 98 883 114 Na2O 920 1277 литий 179 1370 190 Li2O 1610 2500 магний 651 1107 623 MgO 2800 3600 кальций 851 1482 550 CaO 2585 3527
Свойства летучих горючих металлов и их оксидов На способность металлов возгораться и гореть большое влияние оказывают химические и физические свойства металлов и их оксидов. Металлы Температура, оС Оксиды металлов Температура, оС плавления кипения воспламенения плавления кипения калий 64 760 69 K2O 527 1477 натрий 98 883 114 Na2O 920 1277 литий 179 1370 190 Li2O 1610 2500 магний 651 1107 623 MgO 2800 3600 кальций 851 1482 550 CaO 2585 3527
Cлайд 3
 Свойства нелетучих горючих металлов и их оксидов Металлы Температура, оС Оксиды металлов Температура, оС плавления кипения воспламенения плавления кипения Нерастворимые оксиды алюминий 600 2500 1000 Al2O3 2050 3527 кремний 1412 3309 - SiO2 1610 2727 Растворимые оксиды титан 1677 3277 300 TiO2 1855 4227 цирконий 1852 4477 500 ZrO2 2687 4927
Свойства нелетучих горючих металлов и их оксидов Металлы Температура, оС Оксиды металлов Температура, оС плавления кипения воспламенения плавления кипения Нерастворимые оксиды алюминий 600 2500 1000 Al2O3 2050 3527 кремний 1412 3309 - SiO2 1610 2727 Растворимые оксиды титан 1677 3277 300 TiO2 1855 4227 цирконий 1852 4477 500 ZrO2 2687 4927
Cлайд 4
 Рассмотрим кинетические законы окисления и механизм самовоспламенения одиноких частиц металла. В пред нагревательном периоде (от Т0 до Т1) ведущая роль отводится процессу окисления металла. При окислении частиц образуется твердый оксид металла и поглощается большое количество тепла, которое препятствует горению. Большое влияние оказывает также толщина оксидной пленки и ее дисперсность. Пирофорные металлы – это металлы без оксидной пленки. Стадия образования оксидной пленки – диффузионное препятствие для процессов горения и взрывов, при этом увеличивается плотность кристаллической решетки оксидной пленки. Зависимость скорости окисления от времени; 1 – линейная; 2 – параболическая; 3 – кубическая; 4 – логарифмическая
Рассмотрим кинетические законы окисления и механизм самовоспламенения одиноких частиц металла. В пред нагревательном периоде (от Т0 до Т1) ведущая роль отводится процессу окисления металла. При окислении частиц образуется твердый оксид металла и поглощается большое количество тепла, которое препятствует горению. Большое влияние оказывает также толщина оксидной пленки и ее дисперсность. Пирофорные металлы – это металлы без оксидной пленки. Стадия образования оксидной пленки – диффузионное препятствие для процессов горения и взрывов, при этом увеличивается плотность кристаллической решетки оксидной пленки. Зависимость скорости окисления от времени; 1 – линейная; 2 – параболическая; 3 – кубическая; 4 – логарифмическая
Cлайд 8
 Классификация металлов по механизму горения: летучие (кальций, магний) – горящие в паро-фазном режиме; нелетучие: с растворимой оксидной пленкой (в самом расплавленном металле – цирконий); с нерастворимой, но легкокипящей пленкой (бор) воспламенение протекает уже сложнее; с нерастворимой и трудно- кипящей пленкой (алюминий, кремний) воспламенение этих металлов наиболее сложное. Процессы горения металла не зависят от первоначальной формы металла, металлы горят в шарообразной форме, поэтому ошибки в вычислениях почти нет. Если объем оксидной пленки больше объема металла, то оксидная пленка покрывает весь металл и является защитной; если объем оксидной пленки меньше объема металла, то оксидная пленка не является защитной. k ПБ– коэффициент Пиминга-Бевордса, если этот коэффициент ≥1, то оксидная пленка защитная. Например,Mg kПБ =0,8, Ca kПБ =0,6 .
Классификация металлов по механизму горения: летучие (кальций, магний) – горящие в паро-фазном режиме; нелетучие: с растворимой оксидной пленкой (в самом расплавленном металле – цирконий); с нерастворимой, но легкокипящей пленкой (бор) воспламенение протекает уже сложнее; с нерастворимой и трудно- кипящей пленкой (алюминий, кремний) воспламенение этих металлов наиболее сложное. Процессы горения металла не зависят от первоначальной формы металла, металлы горят в шарообразной форме, поэтому ошибки в вычислениях почти нет. Если объем оксидной пленки больше объема металла, то оксидная пленка покрывает весь металл и является защитной; если объем оксидной пленки меньше объема металла, то оксидная пленка не является защитной. k ПБ– коэффициент Пиминга-Бевордса, если этот коэффициент ≥1, то оксидная пленка защитная. Например,Mg kПБ =0,8, Ca kПБ =0,6 .
Cлайд 9
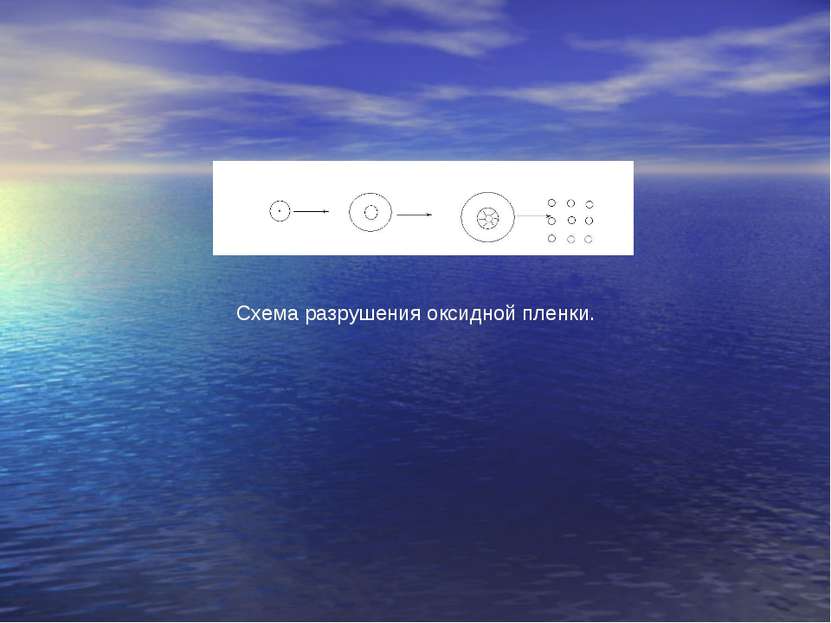
 При исследованиях было выявлено несколько механизмов потери защитных свойств оксидной пленки: общий механизм: у оксидной пленки и металлического ядра различные коэффициенты термического расширения (у оксидной пленки этот коэффициент меньше), при увеличении температуры возникают напряжения, которые ведут к растрескиванию оксидной пленки; растворение пленки в металле; при нагревании частички титана и циркония в вакууме или в атмосфере аргона, извлекают в среду и поджигают, при этом увеличивается воспламеняемость( кислород из поверхности частично диффундирует внутрь ядра); фазовые и агрегатные переходы в оксидной пленке и в металле; испарение (Mg), плавление (Al) металла – пленка лопается объем жидкости больше чем объем твердого вещества – пленка разрушается; при плавлении оксида увеличивается способность кислорода диффундировать через пленку внутрь металла; например, испарение оксида молибдена при переходе из α в β модификации (модификационный переход) изменяется объем оксидной пленки; химические превращения; в состав оксидной пленки входят гидроксиды, карбонаты; при достижении температуры распада, защитные свойства пленки теряются (рис. 36). Схема разрушения оксидной пленки. Инертные примеси; некоторые резко увеличивают скорость окисления и снижают температуру самовоспламенения; те добавки, которые дают с оксидом сплавы с низкой температурой плавления (сплав алюминия с фторидами).
При исследованиях было выявлено несколько механизмов потери защитных свойств оксидной пленки: общий механизм: у оксидной пленки и металлического ядра различные коэффициенты термического расширения (у оксидной пленки этот коэффициент меньше), при увеличении температуры возникают напряжения, которые ведут к растрескиванию оксидной пленки; растворение пленки в металле; при нагревании частички титана и циркония в вакууме или в атмосфере аргона, извлекают в среду и поджигают, при этом увеличивается воспламеняемость( кислород из поверхности частично диффундирует внутрь ядра); фазовые и агрегатные переходы в оксидной пленке и в металле; испарение (Mg), плавление (Al) металла – пленка лопается объем жидкости больше чем объем твердого вещества – пленка разрушается; при плавлении оксида увеличивается способность кислорода диффундировать через пленку внутрь металла; например, испарение оксида молибдена при переходе из α в β модификации (модификационный переход) изменяется объем оксидной пленки; химические превращения; в состав оксидной пленки входят гидроксиды, карбонаты; при достижении температуры распада, защитные свойства пленки теряются (рис. 36). Схема разрушения оксидной пленки. Инертные примеси; некоторые резко увеличивают скорость окисления и снижают температуру самовоспламенения; те добавки, которые дают с оксидом сплавы с низкой температурой плавления (сплав алюминия с фторидами).
Cлайд 11
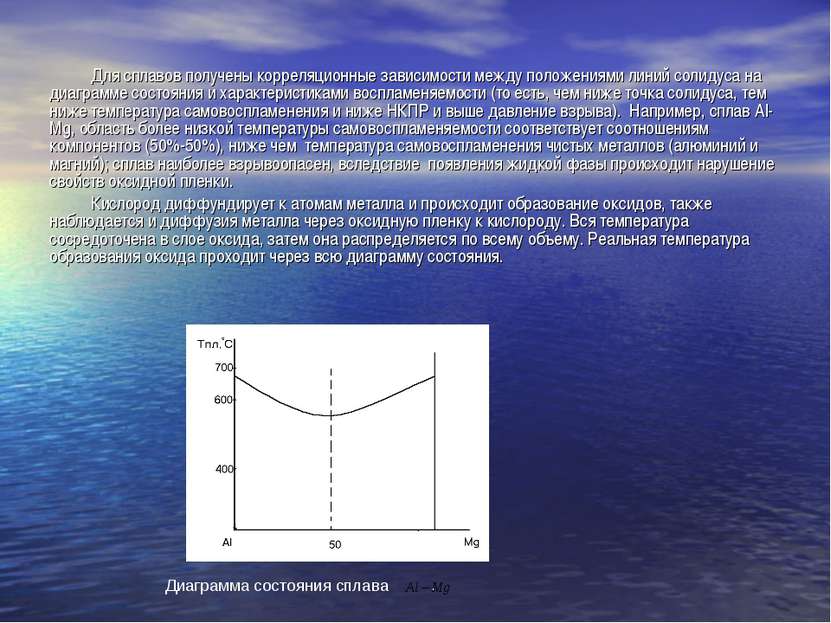
 Для сплавов получены корреляционные зависимости между положениями линий солидуса на диаграмме состояния и характеристиками воспламеняемости (то есть, чем ниже точка солидуса, тем ниже температура самовоспламенения и ниже НКПР и выше давление взрыва). Например, сплав Al-Mg, область более низкой температуры самовоспламеняемости соответствует соотношениям компонентов (50%-50%), ниже чем температура самовоспламенения чистых металлов (алюминий и магний); сплав наиболее взрывоопасен, вследствие появления жидкой фазы происходит нарушение свойств оксидной пленки. Кислород диффундирует к атомам металла и происходит образование оксидов, также наблюдается и диффузия металла через оксидную пленку к кислороду. Вся температура сосредоточена в слое оксида, затем она распределяется по всему объему. Реальная температура образования оксида проходит через всю диаграмму состояния. Диаграмма состояния сплава .
Для сплавов получены корреляционные зависимости между положениями линий солидуса на диаграмме состояния и характеристиками воспламеняемости (то есть, чем ниже точка солидуса, тем ниже температура самовоспламенения и ниже НКПР и выше давление взрыва). Например, сплав Al-Mg, область более низкой температуры самовоспламеняемости соответствует соотношениям компонентов (50%-50%), ниже чем температура самовоспламенения чистых металлов (алюминий и магний); сплав наиболее взрывоопасен, вследствие появления жидкой фазы происходит нарушение свойств оксидной пленки. Кислород диффундирует к атомам металла и происходит образование оксидов, также наблюдается и диффузия металла через оксидную пленку к кислороду. Вся температура сосредоточена в слое оксида, затем она распределяется по всему объему. Реальная температура образования оксида проходит через всю диаграмму состояния. Диаграмма состояния сплава .